Michael S. Rutenberg MD, PhD , Michael D. Chuong MD , Jessica M. Frakes MD , Reirradiation in the Management of Locally Recurrent Rectal Adenocarcinoma, Practical Radiation Oncology (2024), doi: https://doi.org/10.1016/j.prro.2024.11.008
Nội dung chính
Tóm lược
Ung thư trực tràng tái phát sau xạ trị hiện vẫn còn là thử thách khó khăn trong thực hành lâm sàng. Điều trị cứu vãn cũng có thể chữa khỏi được bệnh, tuy nhiên, thường đòi hỏi kết hợp đa mô thức đi kèm với gia tăng đáng kể về biến chứng và tác dụng phụ liên quan đến điều trị. Phẫu thuật vẫn là phương pháp điều trị chính mang tính triệt căn cho ung thư trực tràng tái phát tại chỗ sau xạ trị. Xạ trịlại tiền phẫu cải thiện tỷ lệ diện cắt R0, kiểm soát tại chỗ và kết quả kiểm soát bệnh. Tuy nhiên, lựa chọn này luôn đặt ra cho nhà xạ trị dấu hỏi lớn về việc làm sao để cân bằng hiệu quả cải thiện tỷ lệ kiểm soát và cơ hội điều trị triệt căn bệnh với nguy cơ gây ra các độc tính quá mức. Xạ trị với phân liều biến đổi và xạ trị trong mổ (IORT) thường được sử dụng với hy vọng cải thiện tỷ số điều trị (Therapeutic ratio) trong xạ trị lại ung thư trực tràng tái phát tại chỗ. Trong bài viết này, chúng tôi bàn luận về các dữ liệu bằng chứng ủng hộ chiến lược điều trị cứu vãn đa mô thức, trong đó nhấn mạnh vai trò quan trọng của phẫu thuật cứu vãn, lợi ích của xạ trị lại, các cách tiếp cận khác nhau trong xạ trị lại và các độc tính liên quan đến điều trị. Cuối cùng, chúng tôi đưa ra các khuyến nghị về cách tiếp cận trong xạ trị lại ung thư trực tràng tái phát tại chỗ.
Giới thiệu
Với những tiến bộ trong phẫu thuật và hiệu quả bổ trợ của hoá xạ trị, tái phát tại chỗ sau điều trị đã không còn phổ biến với ung thư trực tràng, tỷ lệ dưới 10%. Ung thư trực tràng (UTTT) tái phát tại chỗ vẫn có thể được chữa khỏi, nhưng với những bệnh nhân đã xạ trị trước đó, liệu trình điều trị cứu vãn luôn đi cùng lo ngại về độc tính của xạ trị lại. Tuy nhiên, những bệnh nhân này thường nhận được nhiều lợi ích từ xạ trị lại về kiểm soát bệnh tại chỗ. Bên cạnh một số báo cáo ghi nhận độc tính đáng chú ý và kết cục lâm sàng kém của xạ trị lại và phẫu thuật cho UTTT tái phát tại chỗ, chúng ta hiện có cơ sở dữ liệu phong phú hơn ủng hộ khả năng dung nạp và hiệu quả của điều trị cứu vãn.
Đến nay, dù vẫn chưa có một cách tiếp cận nào được đồng thuận là chuẩn mực trong điều trị cứu vãn cho UTTT tái phát tại chỗ, chủ đề này được không hiếm gặp trong y văn. Chúng tôi đã tiến hành khảo sát y văn về chủ đề này, tổng hợp dữ liệu hiện có về phẫu thuật và xạ trị lại. Phần cuối của bài viết này cũng sẽ mô tả cách thức tiếp cận trong xạ trị lại ung thư trực tràng tại trung tâm của chúng tôi.
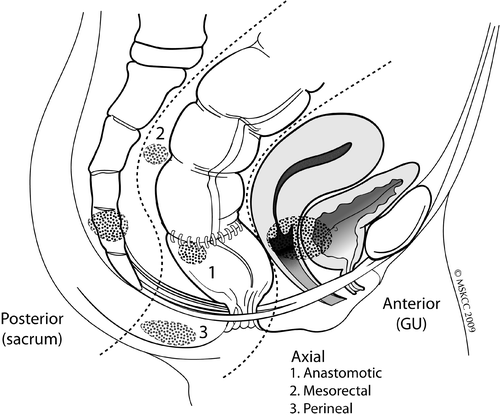
Một cơ hội để cắt là một cơ hội để chữa khỏi
Phẫu thuật cứu vãn với diện cắt âm tính là yếu tố quan trọng nhất ảnh hưởng đến kết cục lâm sàng của UTTT tái phát tại chỗ5-7. Một thử nghiệm đơn nhánh pha II, sử dụng hóa xạ trị cho UTTT tái phát tại chỗ ghi nhận thời gian sống thêm được cải thiện ở những bệnh nhân đạt diện cắt R0 so với những trường hợp có diện cắt R1/R2 hoặc không phẫu thuật, với sống thêm toàn bộ (OS) 5 năm lần lượt tương ứng là 67% và 22%8. Tỷ lệ kiểm soát tại chỗ (LC) và sống thêm không bệnh (DFS) 5 năm ở những bệnh nhân được phẫu thuật đạt R0 sau hóa xạ trị đồng thời lần lượt tương ứng là 69% và 69%. Lợi ích của diện cắt R0 về phương diện kiểm soát tại chỗ và thời gian sống thêm được thể hiện nhất quán trong gần như mọi dữ liệu hồi cứu lớn. Một nghiên cứu tại Hà Lan trên 135 bệnh nhân UTTT tái phát tại chỗ được điều trị với hóa xạ trị lại, sau đó phẫu thuật, khẳng định diện cắt âm tính là yếu tố tác động quan trọng nhất đối với DFS, OS, sống thêm không tái phát tại chỗ (LRFS) và sống thêm không di căn xa4. Một phân tích gộp trên 1460 bệnh nhân UTTT tái phát tại chỗ (có hoặc không có xạ trị) được phẫu thuật, cho thấy tỷ số nguy cơ (HR) tử vong là 2.0 với R1 và 3.4 với R2 khi so sánh với R0.
Đúng vậy, xạ trị lại có hiệu quả
Như với UTTT nguyên phát, trong tình huống bệnh tái phát tại chỗ, xạ trị lại giúp cải thiện kết quả phẫu thuật ở hai thông số: Tỷ lệ đạt diện cắt R0 và tỷ lệ kiểm soát tại chỗ. Với những trường hợp tổn thương tái phát tại chỗ có khả năng cắt bỏ, không kèm theo nguy cơ diện cắt tiệm cận hay dương tính, chỉ định xạ trị lại có thể được bỏ qua. Tuy nhiên, đặc tính xâm lấn của tổn thương tái phát cũng như tình trạng xơ hóa sau phẫu thuật và xạ trị trước đó, việc đạt được diện cắt âm tính có thể là mộtthử thách thật sự. Liệu có hợp lí không khi mong đợi tế bào ung thư tái phát sau xạ trị vẫn nhạy cảm với tia xạ? Với các dữ liệu hiện có, dường như không có khác biệt rõ rệt về mức độ đáp ứng với xạ trị của UTTT nguyên phát và tái phát (Đã xạ trị trước đó). Valentini và cộng sự đã báo cáo tỷ lệ đáp ứng một phần là 36% và đáp ứng toàn bộ trên mô bệnh học (pCR) là 9% ở những bệnh nhân được phẫu thuật sau khi xạ trị lại8. Dijkstra và cộng sự báo cáo pCR của 9% bệnh nhân được xạ trị lại 30-30.6Gy (1.8-2Gy/fx) kết hợp hóa trị. Một nghiên cứu tại trung tâm MD Anderson cũng đã ghi nhận tỷ lệ pCR14% với chiến lược xạ trị tăng tốc, tăng số phân liều10, 11. Những kết quả này có thể so sánh với tỷ lệ pCR được báo cáo với hóa xạ trước mổ cho UTTT điều trị lần đầu, vào khoảng 7-20%12, 13. Dù còn thiếu những thử nghiệm tiến cứu so sánh phẫu thuật cứu vãn có hoặc không có xạ trị lại, dựa vào những dữ liệu trên, lợi ích của xạ trị bổ trợ trước mổ trong việc tăng cơ hội đạt được R0 và cải thiện kiểm soát tại chỗ có thể là một lý lẽ phù hợp để ngoại suy cho chỉ định xạ trị lại. Một dữ liệu hồi cứu lớn trên 565 bệnh nhân UTTT tái phát tại chỗ, 256 bệnh nhân trong đó trải qua hóa xạ tiền phẫu, ghinhận phẫu thuật đạt được R0 cho 43% BN nhận xạ trị lại, so với 26% ở nhóm không xạ trị tiền phẫu. Một phân tích gộp đánh giá xạ trị lại cho UTTT tái phát tại chỗ, so sánh xạ trị lại tiền phẫu, hoá xạ tiền phẫu và hóa xạ bổ trợ cho thấy tỷ lệ đạt R0 và kiểm soát bệnh tại chỗ cao nhất ở nhóm hóa-xạ trị lại tiền phẫu14.
Kiểm soát nguy cơ độc tính của xạ trị lại
Nguy cơ xuất hiện các độc tính nghiêm trọng khi xạ trị vào các tổ chức mô lành đã nhận một liều xạ trị nhất định trong lần điều trị trước đó là khía cạnh được đặc biệt quan tâm khi cân nhắc chỉ định xạ trị lại. Tuy nhiên, các dữ liệu bằng chứng, đến hiện tại, cho thấy tỷ lệ độc tính là có thể chấp nhậnkhi xạ trị lại. Valentini và cộng sự, trong một nghiên cứu đã báo cáo tỷ lệ độc tính cấp độ 3 là 5,1% và không có trường hợp nào ghi nhận độc tính cấp độ 4-58. 12% bệnh nhận gặp độc tính muộn nghiêm trọng (“Có thể” do xạ trị lại) bao gồm xơ hóa da, bất lực ở nam giới, rối loạn tự chủ tiểu tiện, tắc ruột non và tiểu khó. Một nghiên cứu tiến cứu nhỏ trên các bệnh nhân đã được xạ trị vùng chậu trước đó (Vì bất kì nguyên nhân gì), chẩn đoán UTTT tái phát hoặc không cắt bỏ được, được điều trị xạ trị lại (1.3 Gy, BID – Hai phân liều/ngày, tổng liều 39 Gy) không ghi nhận trường hợp nào gặp độc tính cấp do xạ trị độ 4 trở lên và <25% bệnh nhân gặp độc tính cấp độ <= 3 15. Một phân tích tổng hợp trên cơ sở dữ liệu của hơn 700 bệnh nhân được xạ trị lại, báo cáo tỷ lệ gộp chung các độc tính cấp muộn độ >= 3 và độc tính muộn khi có và không phẫu thuật tương ứng lần lượt là 25,5% và 11.7%16. Đáng chú ý, trong một báo cáo trên một số lượng lớn ca bệnh của Mohiuddin và cộng sự, xạ trị lại với chiến lược tăng số phân liều (1.2Gy – 2 phân liều/ngày hay BID) có thể giảm độc tính muộn so với phân liều tiêu chuẩn.
Các phương thức xạ trị lại
Xạ trị lại có thể được thực hiện theo một số phương thức và cách tiếp cận khác nhau18. Xạ trị chiếu ngoài với phân liều biến đổi là một trong những thực hành phổ biến, nhằm cải thiện tỷ số điều trị giữa khả năng hồi phục của mô lành và hiện tượng tái lập quần thể tế bào u19, 20. Nghiên cứu từ đại học Kentucky đã thực hiện hoá – xạ trị lại với phác đồ tăng số phân liều (1,2 Gy BID) hoặc 1 phân liều/ngày (1,8 Gy) đến tổng liều 30 – 49,2 Gy (Trung vị 34,8 Gy), tỷ lệ OS 5 năm được báo cáo là 22% ở những bệnh nhân được hoá – xạ trị lại và phẫu thuật17. Thử nghiệm pha II tiến hành bởiValentini và cộng sự trên 59 bệnh nhân được hoá – xạ trị lại với phác đồ tăng số phân liều 40.8 Gy (1.2 Gy BID) và phẫu thuật, báo cáo tỷ lệ OS 5 năm là 66.8% ở nhóm bệnh nhân được hoá – xạ trị lại và phẫu thuật đạt diện cắt R08. Trung tâm MD Anderson đã công bố kết quả ứng dụng phác đồ tăng số phân liều – tăng tốc trong hoá – xạ trị lại, 1,5 Gy BID đến tổng liều 30 – 45 Gy, tỷ lệ OS 3 năm và kiểm soát tại chỗ tương ứng lần lượt là 62% và 49% ở những bệnh nhân được phẫu thuật. Như đã đề cập ở trên, Mohuiddin và cộng sự nhận định độc tính của xạ trị được giảm thiểu với phác đồ tăng sốphân liều, tuy nhiên các dữ liệu so sánh còn hạn chế17.
Xạ trị trong mổ (IORT) đã được ứng dụng trong điều trị cứu vãn cho các bệnh nhân UTTT tái phát tại chỗ, với phần lớn dữ liệu bằng chứng ủng hộ IORT kết hợp cùng xạ trị trước mổ21. IORT tăng cường một liều xạ lớn đến khối u/giường phẫu thuật trong khi các cơ quan nguy cấp (OARs) an toàn ngoài phạm vi tác động. IORT sử dụng electron (IOERT) hoặc kỹ thuật áp sát suất liều cao (HDR-IORT). Một báo cáo từ Mayo Clinic trên 248 bệnh nhân với tái phát trong trường chiếu, được điều trị cứu vãn sử dụng hoá – xạ trị lại trước mổ và IOERT. Trung vị của liều xạ ngoài là 27,5 Gy (5 – 39,5 Gy). IOERT đóng góp mức liều dao động từ 12,5 – 20 Gy tuỳ theo trạng thái diện cắt. Tỷ lệ tái phát tại chỗ và OS 5 năm tương ứng lần lượt là 37% và 46%6. Diện cắt phẫu thuật có liên quan đến kết quả kiểm soát bệnh tại chỗ khi tỷ lệ tái phát tại chỗ 5 năm với diện cắt R0, R1/R2 tương ứng lần lượt là 21% và 32%. Dữ liệu từ Hà Lan trên 135 bệnh nhân UTTT tái phát tại chỗ, được hoá – xạ trị lại mức liều 30 – 30,6 Gy, sau đó phẫu thuật và IOERT (10 – 15 Gy), so sánh với nhóm bệnh nhân UTTT tái phát tại chỗ chưa xạ trị trước đó, được hoá xạ trị trước mổ đủ liều (~ 50 Gy) và phẫu thuật cùng với IOERT, nhóm thứ 3 là các bệnh nhân UTTT tái phát tại chỗ chưa xạ trị trước đó nhưng được điều trị cứu vãn bằng phẫu thuật và IOERT4. 55% bệnh nhân hoá – xạ trị lại đạt được phẫu thuật R0 so với 63% và 42 % tương ứng lần lượt ở nhóm nhận hoá xạ trị trước mổ đủ liều và không xạ trị trước mổ. Tỷ lệ sống thêm không tái phát tại chỗ 5 năm là 45,9%, 58,7%, 35% tương ứng lần lượt ở nhóm hoá – xạ trị lại trước mổ, hoá xạ trị trước mổ đủ liều và không xạ trị trước mổ. Hyngstrom cùng cộng sự báo cáo kết quả của 70 bệnh nhân UTTT tái phát tại chỗ, được điều trị cứu vãn với xạ trị lại trước mổ (Có/không kết hợp hoá trị) đến 39 Gy (1,5 Gy BID), theo sau bởi HDR-IORT (10-15 Gy)22. Tỷ lệ kiểm soát tại chỗ 5 năm là 56%, không có sự khác biệt giữa nhóm được phẫu thuật R0 và R1. Kết quả này gợi mở rằng IORT có thể giúp giảm thiểu nguy cơ tái phát tại chỗ cho những trường hợp diện cắt dương tính.
Các phương thức xạ trị mới, với tiềm năng lợi ích từ các ưu thế về cấp liều xạ trị (Ví dụ: SBRT) và/hoặc thuộc tính vật lí (Ví dụ: Các bức xạ hạt), có thể cải thiện hiệu quản và khả năng dung nạp của xạ trị lại. Ứng dụng SBRT cho UTTT tái phát tại chỗ, không thể phẫu thuật đã được báo cáo trong một số dữ liệu hồi cứu23, 24. Liều SBRT trong xạ trị lại đã được lựa chọn trong khoảng 24 – 51 Gy với 3 – 5 phân liều, tỷ lệ kiểm soát tại chỗ trong 2 năm được ghi nhận khoảng 70%. Xạ trị hạt sử dụng proton và ion carbon (CIRT) cũng đã tham gia vào xạ trị lại cho các trường hợp bệnh tái phát, không thể phẫu thuật cắt bỏ25-27, đang chờ đợi được chứng tỏ lợi ích tiềm năng qua các thử nghiệm tiến cứu28.
Đâu là lựa chọn phương thức tối ưu cho xạ trị lại?
Thiếu các dữ liệu tiến cứu, bên cạnh bệnh cảnh lâm sàng cực kỳ đa dạng của UTTT tái phát tại chỗ, đa dạng các cách tiếp cận, tất cả các yếu tố trên dẫn đến khó có thể kết luận đâu là lựa chọn tối ưu cho xạ trị lại trong tình huống này. Tuy nhiên, dữ liệu bằng chứng hiện tại ủng hộ biến đổi cách thức trải liều trong xạ trị lại với phác đồ tăng số phân liều hoặc tăng tốc – tăng số phân liều8, 11, 17. Mức liều tối ưu cho xạ trị lại vẫn chưa được thống nhất, có xu hướng thấp hơn cho với mức liều được chọn khi xạ trị lần đầu. Xạ trị lại với một liều xạ tương đương với xạ trị lần đầu (Ví dụ: 50 Gy) có thể mang lại kết quả tốt hơn, dù có thể làm gia tăng nguy cơ độc tính. IORT hay các kỹ thuật khác (Như SBRT) có thể giúp nâng liều xạ mà không ảnh hưởng đến OARs, Bên cạnh đó, có thể có lợi ích của hoá trị cảm ứng hay dẫn đầu (Induction chemotherapy) khi kết hợp cùng hoá – xạ trị lại29.
Một số vấn đề khác
Nhiều yếu tố có giá trị tiên lượng đã được xác định trong điều trị cứu vãn UTTT tái phát tại chỗ. Khoảng thời gian từ điều trị ban đầu đến thời điểm bệnh tái phát dài hơn có tương quan chặt chẽ với kết quả điều trị tốt hơn và nguy cơ độc tính của xạ trị lại thấp hơn trong nhiều bệnh ác tính4, 8, 17. Cách thức xây dựng thể tích bia cho xạ trị lại rất thay đổi trên thực hành lâm sàng. Thông thường, bệnh tích u thô (GTV) được mở rộng 1 – 2 cm để xác định thể tích bia lâm sàng, dù một số nghiên cứu sử dụng một thể tích rộng rãi hơn với ý nghĩa dự phòng8, 30, 31. Lưu ý rằng, thể tích bia nên được cá thể hoá cho mỗi người bệnh, nhắm đến bệnh tích u thô (Tổn thương tái phát trên đại thể) và cố gắng bao phủ các vị trí mà phẫu thuật viên dự kiến gặp khó khăn để đạt diện cắt R0, bên cạnh đó, giảm thiểu tối đa thể tích chiếu xạ. Một số thử nghiệm đang được tiến hành nhằm giúp đỡ các nhà lâm sàng định hình rõ hơn cách tiếp cận tốt nhất trong điều trị trước mổ cho UTTT tái phát tại chỗ31,32.
Với dung lượng có hạn của bài viết, chúng tôi không thể thảo luận chi tiết hơn các vấn đề liên quan đến một tình huống khác, vô cùng thách thức trên thực hành lâm sàng, đó là UTTT đã xạ trị, tái phát tại chỗ và không thể phẫu thuật. Vấn đề quan trọng nhất cần xem xét là xác định mục tiêu điều trị, tạm thời hay triệt căn, và hiểu rằng dù mục tiêu triệt căn có thể khả thi mà không cần phẫu thuật, cơ hội đó bị giảm đi với cấp số 2 -3 lần. Để giảm nhẹ, xạ trị lại có thể chọn một mức liều an toàn trong số các phác đồ giảm nhẹ phổ biến (Ví dụ: 20 Gy trong 5 phân liều, 20 Gy trong 10 phân liều hoặc 30 Gy trong 10 phân liều). Khoảng thời gian giữa xạ trị lại và liệu trình xạ trị lần đầu, nguyện vọng của người bệnh và điều kiện sẵn có sẽ giúp xác định chiến lược giảm nhẹ nào phù hợp với từng trường hợp cụ thể. Khi xác định mục tiêu điều trị triệt căn, hoá – xạ trị lại đồng thời được khuyến cáo với mức liều tiến đến 50 Gy, dao động trong khoảng 45 – 51 Gy với 1,5 Gy BID, là cách tiến cận ưu tiên của chúng tôi. Một lựa chọn khác, cách thức trải liều tiêu chuẩn có thể được xem xét, cũng nhắm đến mức liều tiệm cận 50 Gy. Leo thang liều với các kỹ thuật xạ trị tiên tiến (Ví dụ: SBRT) hoặc bức xạ hạt có thể được cân nhắc cho các trường hợp tổn thương tái phát ngoài thành ống tiêu hoá (Ví dụ: Trước xương cùng, không xâm lấn ruột). Tối ưu đáp ứng tại u với hoá trị cảm ứng trước hoá – xạ trị lại cũng nên được thảo luận. Cuối cùng, quản lý tình huống UTTT tái phát tại chỗ đặc biệt đòi hỏi một ê kíp đa chuyên khoa và kinh nghiệm.
Tài liệu tham khảo
Vui lòng xem các tài liệu tham khảo được trích dẫn tại bài viết gốc: https://doi.org/10.1016/j.prro.2024.11.008
Bài viết được dịch bởi:
BS. Phan Thị Dịu – BS. Trần Trung Bách