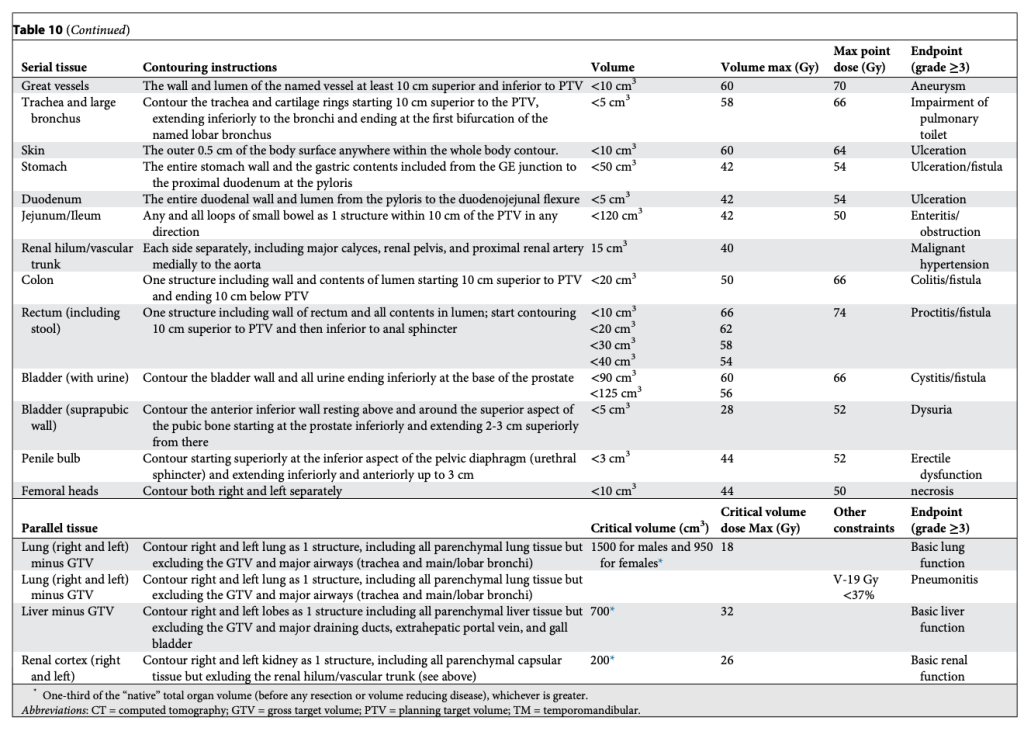
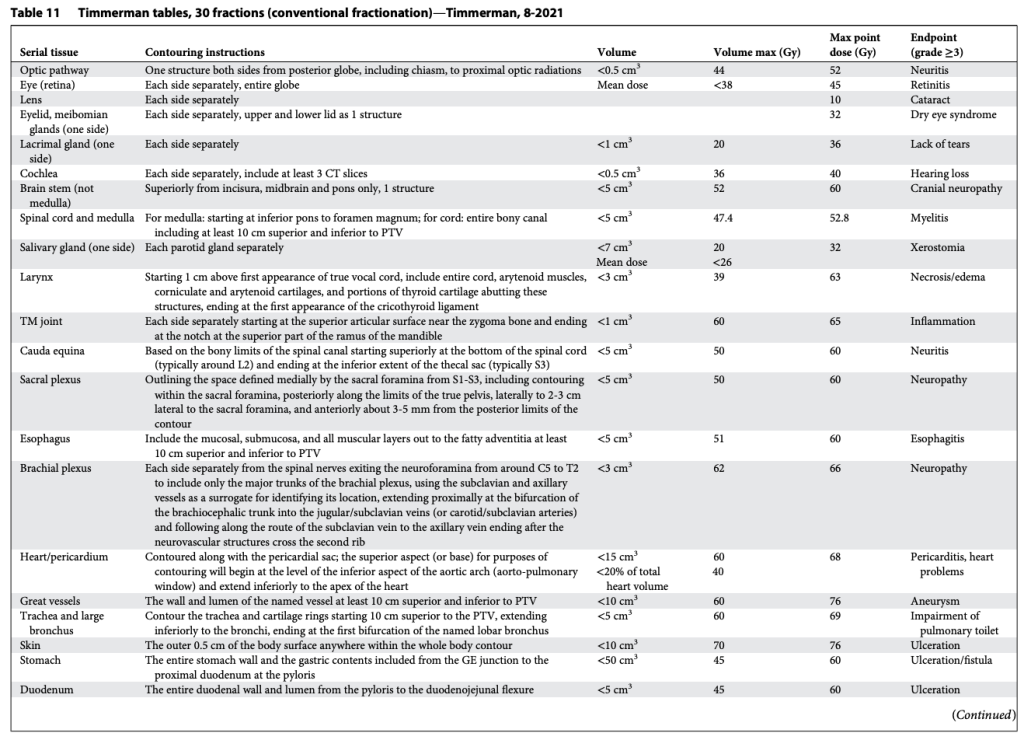
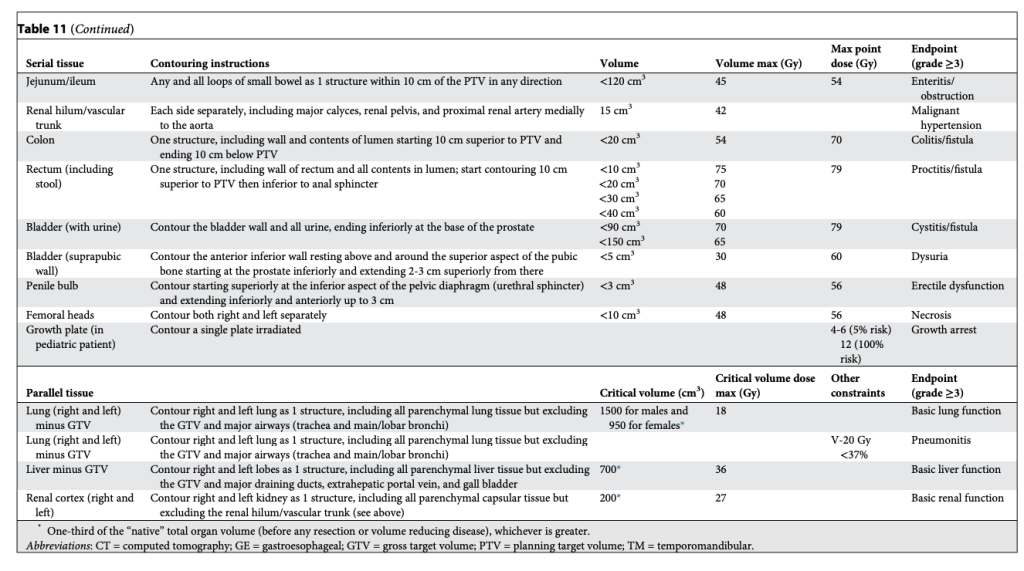
Bài viết dưới đây được lược dịch từ “A Story of Hypofractionation and the Table on the Wall” của Robert Timmerman, một nhà tiên phong trong xạ trị giảm số phân liều và SBRT, được đăng trên tạp chí Đỏ của Hội Xạ trị ung thư Hoa Kỳ (ASTRO) tháng 1 năm 2022. Nhân vật “Tôi” trong bài viết chính là tác giả Robert Timmerman.
Tôi, gần đây, nhận được thông báo rằng đã thắng một cuộc thi mà tôi, thực tế, chưa từng tham dự. Một thăm dò trên Twitter đã được tổ chức thông qua @Radiaton Nation bởi Sue Yom, tân tổng biên tập của tạp chí, đặt câu hỏi “Đâu được coi là tiêu chuẩn vàng cho lập kế hoạch xạ trị giảm số phân liều (Hypofractionated RT – HFRT)?”. Các lựa chọn trả lời bao gồm “HyTEC; AAPM TG-101; Bảng Timmerman; và các protocol NRG/RTOG”. Với hơn 100 lượt bình chọn trong 24 giờ, “Bảng Timmerman”, ở trường Đại học Tây Nam Texas chúng tôi gọi là “Bảng giới hạn liều”, đã chiến thắng với 37,5% lượt bình chọn. Không phải để đánh bóng thêm điều này, nhưng 2 trong những lựa chọn còn lại, “AAPM TG-101” và hầu hết các protocol của NRG/RTOG đã trích dẫn trực tiếp từ các phiên bản trước đây của các bảng giới hạn liều của chúng tôi. Vì vậy, thực tế chúng tôi đã có 78% tổng số lượt bình chọn. Ê kíp của chúng tôi đã phát triển phiên bản đầu tiên của các bảng này từ khoảng năm 2002. Các bảng này đã được lan toả không giới hạn thông qua các chương trình workshop, đào tạo, và qua email đến các bác sĩ lâm sàng, nội trú, kỹ sư, kỹ thuật viên tính liều. Tôi được biết rằng các phiên bản khác nhau của các bảng đã được sử dụng như một tài liệu tham khảo thường ngày tại nhiều phòng lập kế hoạch xạ trị trên toàn nước Mỹ và nhiều quốc gia.
Kết quả của cuộc thăm dò có thể gây ngạc nhiên. Sau tất cả, dự án HyTEC là một nỗ lực chính thức để cung cấp một hướng dẫn đồng thuận chi tiết về lập kế hoạch cho HFRT. Tôi đã soạn các bảng của tôi trong khi xem chương trình yêu thích trên tivi vào buổi tối, sau giờ làm. Vậy tại sao không phải HyTEC chiếm ưu thế trong cuộc thăm dò này? Câu trả lời rõ ràng là HyTEC chỉ mới được công bố gần đây, và các trung tâm gần như sẽ dần dần ứng dụng các khuyến cáo này và làm quen với việc sử dụng nó. Ngược lại, các bảng của chúng tôi đã tồn tại gần 20 năm, cho phép người lập kế hoạch cảm thấy thoải mái với định dạng của nó và ứng dụng. Các bảng ra đời từ những năm đầu của SABR và xạ trị giảm số phân liều thời kỳ hậu hiện đại. Trong bài xã luận này, tôi muốn kể về phiên bản của mình về hai câu chuyện đan xen.
SABR – cái tên tôi ưa dùng hơn thay cho cụm từ khô khan và kém mô tả “xạ trị định vị thân” (SBRT) – nay đã trở thành một phương pháp điều trị phổ biến, đến mức các trung tâm không triển khai có thể bị coi là “lạc hậu”, thiếu đi năng lực thiết yếu của xạ trị hiện đại. Thực tế, với sự xuất hiện của mô hình thanh toán thay thế (Alternative Payment Model) từ Medicare và Medicaid, tôi cho rằng xạ trị phân liều cổ điển sẽ nhanh chóng trở nên không còn khả thi, báo hiệu sự kết thúc của những phác đồ vốn kéo dài 6–9 tuần trong nhiều thập kỷ. Thay vào đó, theo quan điểm của tôi, khi không còn động lực chi trả, gần như tất cả các phương pháp xạ trị (trừ nhi khoa, u tế bào mầm và lymphoma) sẽ là ngắn ngày: SABR hoặc gần như SABR.
Tôi có chút tự mãn, nhưng cách đây chưa lâu, SABR từng bị coi là cực đoan, thậm chí bị xem nhẹ. Những “người khổng lồ” của ngành xạ trị, những người đã phát triển và cổ vũ cho phương pháp xạ trị phân liều cổ điển, như Henry Kaplan, Gilbert Fletcher, Isadore Lampe và Franz Buschke, đã có ảnh hưởng lớn trong việc khiến Medicare chi trả nhiều hơn cho nhiều buổi điều trị, bởi họ tin tưởng mạnh mẽ vào sinh học bức xạ của sự khác biệt trong khả năng sửa chữa giữa khối u và mô lành. Xạ trị phân liều cổ điển vốn rất “dễ chịu” về mặt sinh học, đến mức có thể áp dụng ngay cả cho những bệnh nhân yếu ớt nhất. Lập kế hoạch điều trị cho phương pháp này cũng tương đối dễ dàng vì hầu như mọi kế hoạch đều có thể tránh gây tổn thương mô, kể cả những trường chiếu khá “cẩu thả”, không đồng dạng với thể tích bia và chiếu vào một thể tích lớn mô lành (Ví dụ: Trường chiếu trước–sau, sau–trước hoặc cặp wedge). Các giới hạn liều mô lành dùng để hướng dẫn thể thức xạ trị này cũng rất đơn giản (Ví dụ: bảng Emami một trang mà tôi từng dán trên tường trước năm 2000).
Trong bài xã luận lúc nghỉ hưu, Fletcher đã cảnh báo mạnh mẽ chuyên ngành không nên sử dụng các phác đồ phân liều kích thước lớn, trừ khi bệnh nhân chỉ còn sống tính bằng ngày. Không nghi ngờ gì, ông đã có những trải nghiệm cá nhân tiêu cực về HFRT gây nên các tác dụng muộn đáng sợ. SABR – đại diện của HFRT, đối thủ lớn đối với xạ trị cổ điển – đã xuất hiện vào giữa những năm 1990 từ nhiều thử nghiệm nghiệm độc lập trên khắp thế giới. Tuy nhiên, tất cả đều bắt nguồn từ những tiến bộ công nghệ ngoạn mục – những công nghệ mà Kaplan, Fletcher, Lampe và Buschke khó có thể hình dung. Thay vì khai thác sự khác biệt tinh tế về sinh học của cơ chế sửa chữa tổn thương do bức xạ, SABR đơn giản sử dụng công nghệ để “tách biệt” khối u khỏi mô lành. Những công nghệ ấn tượng này có thể đã được dùng để trong xạ trị phân liều cổ điển (như với proton), nhưng may mắn là SABR không chỉ là xạ trị giảm số phân liều mà, như nhiều người nhấn mạnh đầy cảm xúc, còn là cực kỳ giảm số phân liều.
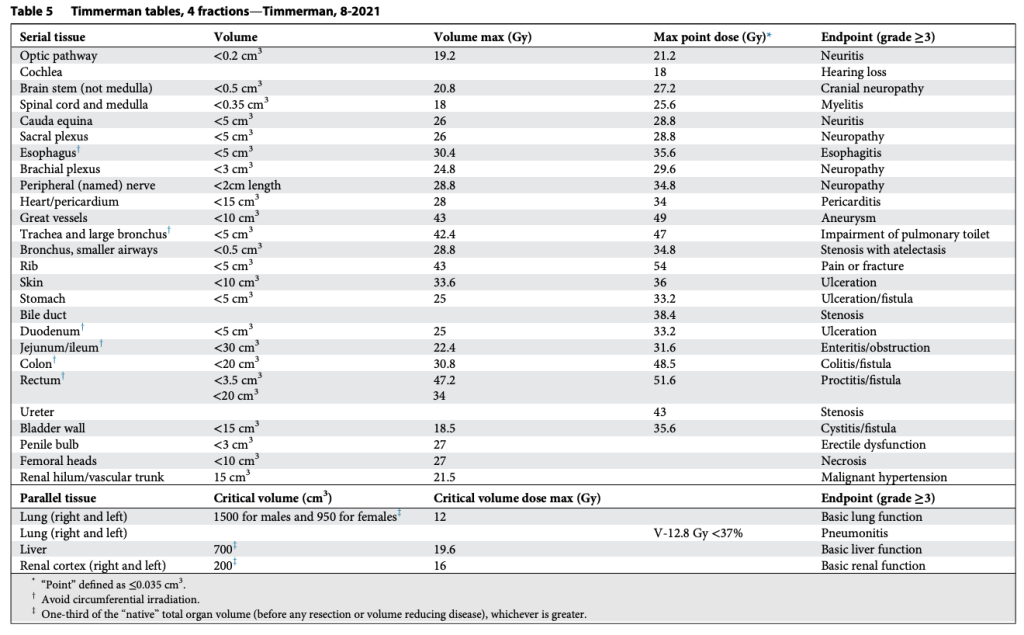
Dù hầu hết các kinh nghiệm ban đầu với SABR đều áp dụng cho bệnh nhân di căn giai đoạn cuối, đến năm 1998 chúng tôi đã thực hiện bước đi táo bạo: Bắt đầu điều trị cho bệnh nhân ung thư phổi giai đoạn sớm – những người có khả năng sống đủ lâu để thực sự gặp tác dụng muộn. Nghiên cứu thí điểm của chúng tôi cho kết quả tích cực và được các nhà lãnh đạo tư duy cởi mở đánh giá cao. Năm 2000, nhóm chúng tôi đề xuất một thử nghiệm cơ bản tái hiện nghiên cứu trước đó của Đại học Indiana, nhưng tuyển bệnh nhân trong một tập đoàn đa trung tâm lớn – Radiation Therapy Oncology Group (RTOG, nay là NRG). Dù mất nhiều năm mới kích hoạt được thử nghiệm hợp tác đầu tiên này – RTOG 0236 – song các ủy ban chuyên khoa của RTOG đã khéo léo thương lượng các điều khoản để các trung tâm tham gia có thể chấp thuận. Ví dụ, họ yêu cầu một danh sách các giới hạn liều cho mô lành trong phác đồ 3 phân liều, và một số hướng dẫn về cách xây dựng phân bố liều và đánh giá kế hoạch. Với đa số thành viên ủy ban, việc chiếu 20 Gy × 3 phân liều là điều khủng khiếp. Họ muốn có các bảng giới hạn liều được viết ra, để nếu tuân thủ, sẽ mang lại sự tin tưởng và an toàn. Mặc dù lúc đó chúng tôi đã điều trị cho vài trăm bệnh nhân, nhưng chưa hề có bảng giới hạn nào tồn tại. Chúng tôi đơn giản chỉ tạo các phân bố liều nhỏ gọn với độ sụt giảm liều nhanh chóng tối đa, đều theo mọi hướng. Trước những yêu cầu cứng rắn để kích hoạt thử nghiệm, và không thể chùn bước, tôi đã bắt tay vào phát triển bảng giới hạn liều đầu tiên cho SABR.
Là một bác sĩ thần kinh thực thụ, tôi vốn đã có chút kinh nghiệm về giới hạn liều trong xạ trị liệu trình ngắn. Trong xạ phẫu, tôi quen thuộc với đường cong Kjellberg isoeffect thường được sử dụng để mô tả liều kê an toàn cho một tổn thương có kích thước cụ thể (Ví dụ: 20 Gy cho tổn thương 2 cm chỉ đi kèm 1% nguy cơ hoại tử). Hãy thử nghĩ: Để báo cáo được nguy cơ 1% này cho cụ thể một tổn thương 2 cm, lẽ ra phải điều trị cho nhiều bệnh nhân, tất cả đều có tổn thương 2 cm, với nhiều mức liều khác nhau (17–18 Gy, 19–20 Gy, 21–22 Gy…) để xác định chuẩn liều an toàn là 20 Gy. Hãy tưởng tượng sự thất vọng khi tôi tìm hiểu kỹ các nguồn gốc khó tiếp cận của đường cong Kjellberg và nhận ra rằng rất ít dữ liệu từ người, chủ yếu là chuột, khỉ…, và chưa tới 50 điểm dữ liệu đã dựng nên cả đường cong. Thực ra, cơ sở cho đường cong Kjellberg danh giá đó… rất mong manh. Khi ấy, tất cả chúng tôi đều dùng đường cong đó để kê liều cho cả khối u và dị dạng động–tĩnh mạch. Và bất chấp nền tảng hạn chế, nó phần lớn vẫn “hoạt động” giúp các bác sĩ xạ phẫu tránh được các biến cố do độc tính.
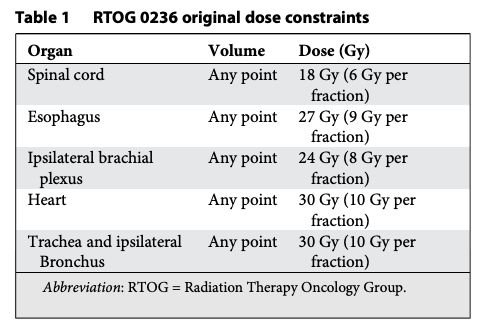
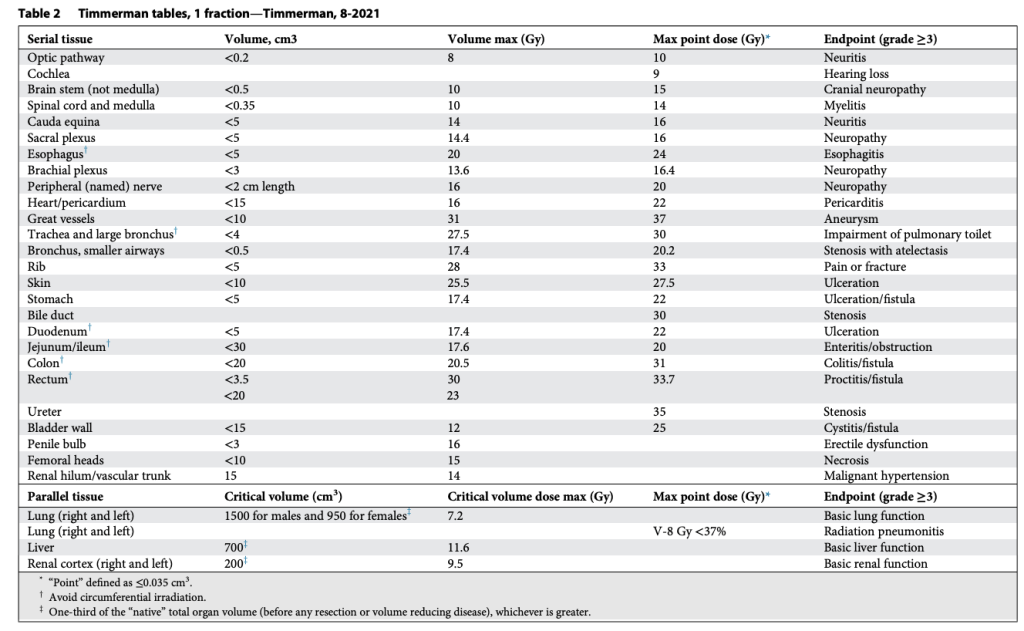
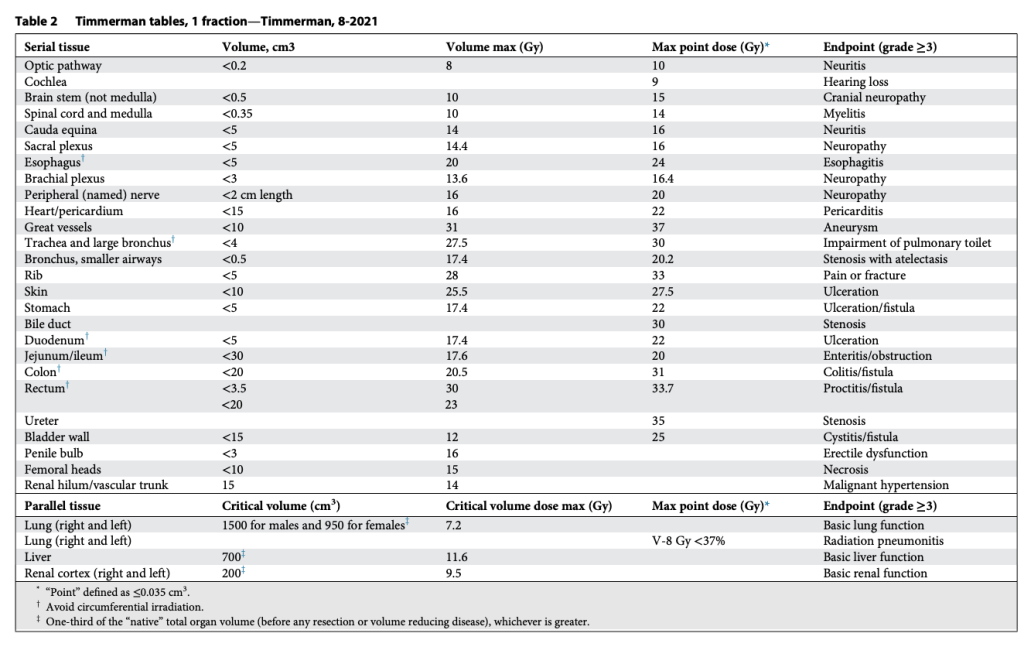
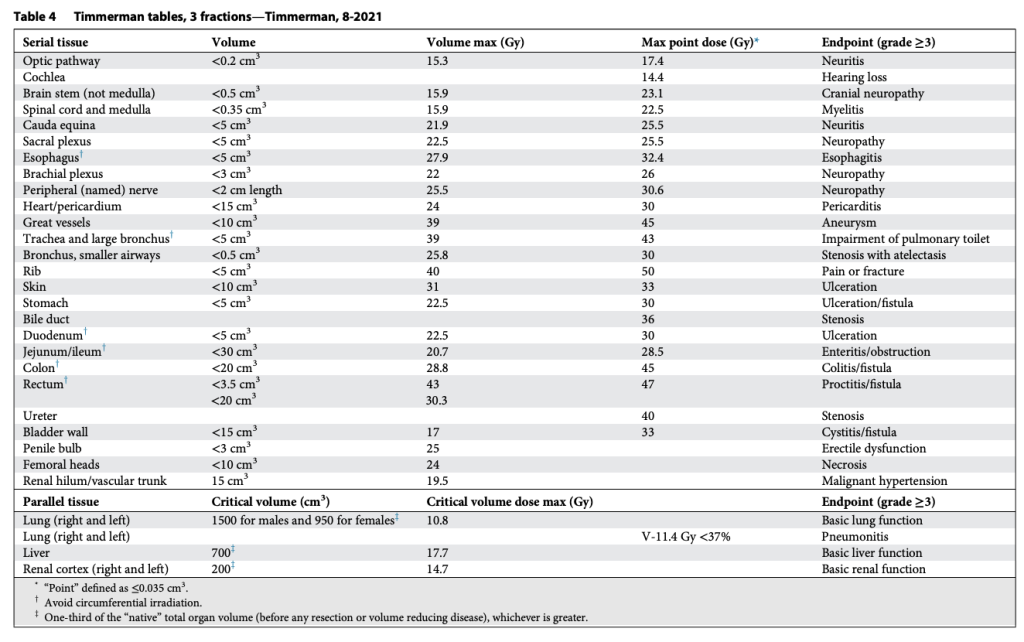
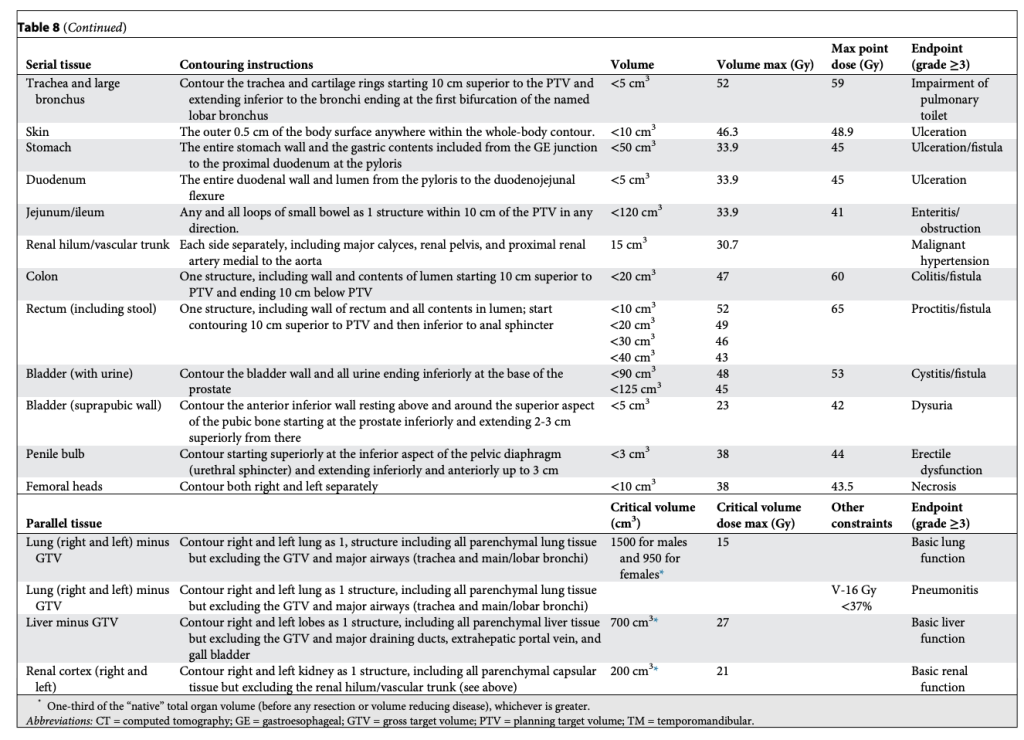
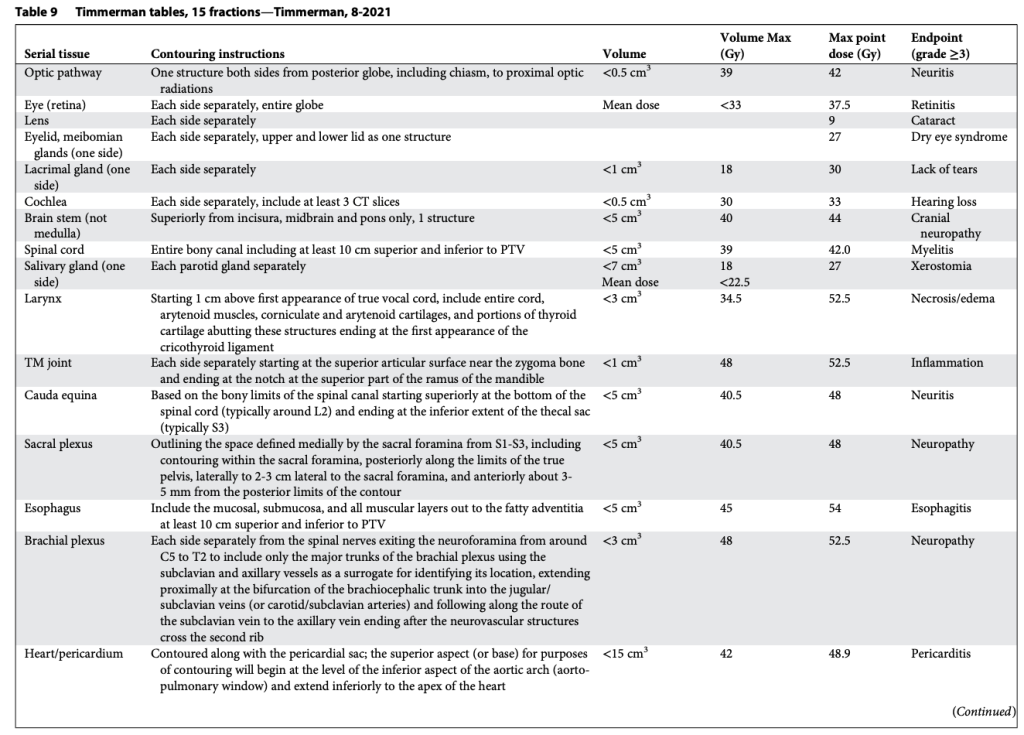
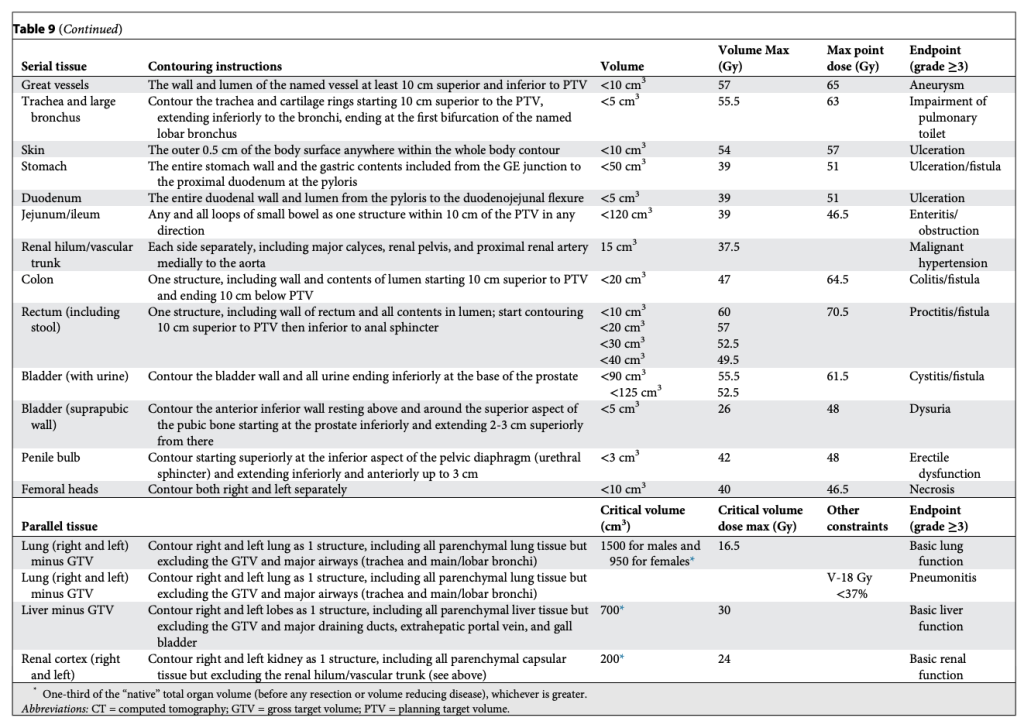
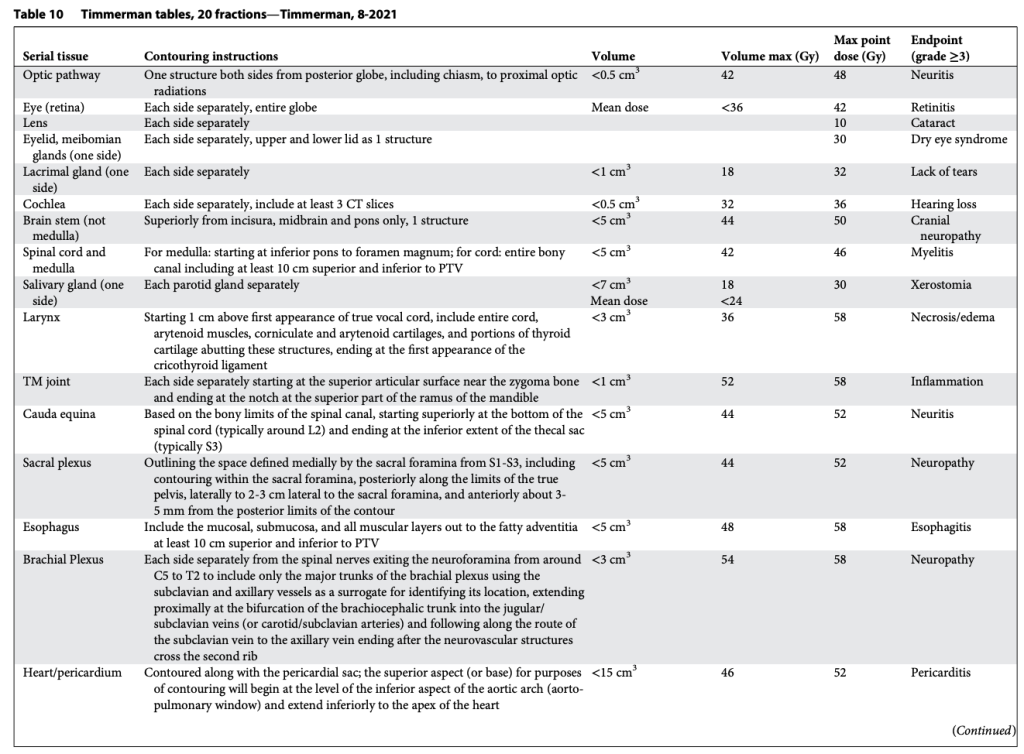
Trở lại với SABR. Một bảng giới hạn liều điểm tối đa (Maximum point dose) cho phác đồ 3 phân liều đã nhanh chóng được xây dựng cho tủy sống, thực quản, đám rối cánh tay, tim và khí quản, như trình bày trong Bảng 1. Thành thật mà nói, ngoại trừ tủy sống, tất cả các giới hạn khác trong bảng ban đầu đều chỉ là những “ước đoán có cơ sở” của tôi. Khi đó, tôi nhờ nhà sinh học phóng xạ nổi tiếng và đồng thành viên ủy ban, Jack Fowler, xem xét bảng này, và ông đã hồi âm tử tế rằng các giới hạn có vẻ hợp lý và không hỏi quá nhiều. Nhìn lại, giới hạn duy nhất từ protocol ban đầu đó đến nay không thay đổi nhiều là liều điểm tối đa 30 Gy cho tim. Các giới hạn khác ban đầu đều quá nghiêm ngặt (thận trọng), đến mức các giới hạn hiện tại, cũng như HyTEC, cho phép liều cao hơn mà không gây độc tính. Tôi không tự hào về việc “chế tạo” (Nghe có vẻ hay hơn là “bịa ra”) các giới hạn trong một protocol cấp quốc gia mà sau này lại thay đổi tiêu chuẩn điều trị ung thư phổi. Nhưng để biện minh, chính điều này đã khởi động một lĩnh vực vốn dĩ khá trì trệ. SABR không chỉ mang lại lựa chọn tốt cho bệnh nhân ung thư phổi giai đoạn sớm không mổ được, mà còn thúc đẩy xạ trị tiến vào những lĩnh vực mới như điều trị các khối u kháng xạ (Khi đó chúng tôi gọi là ung thư gan, hắc tố, và ung thư thận), điều trị di căn từ mọi khối u, và thôi thúc chuyên ngành xạ trị từ bỏ các phác đồ kéo dài vô lý (Ví dụ 9 tuần cho ung thư tuyến tiền liệt). SABR đã khởi xướng một “cuộc cách mạng giảm số phân liều” và mang lại niềm hứng khởi rằng ngành xạ trị còn có tương lai. Tất cả điều này sẽ không thể xảy ra nếu không có “sự ủng hộ”, và “sự ủng hộ” thì cần có các giới hạn mô lành.
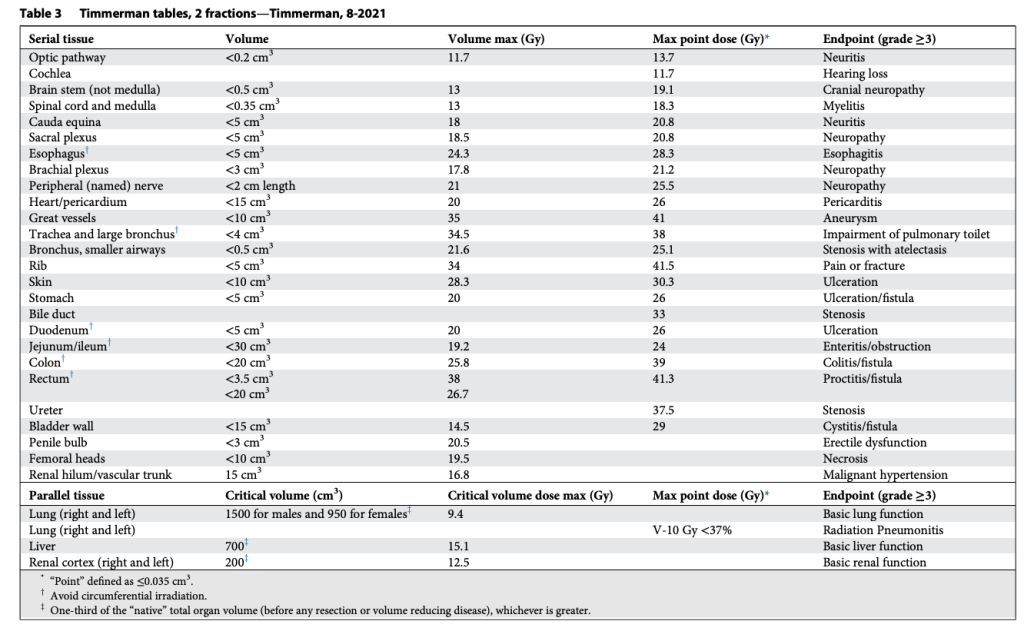
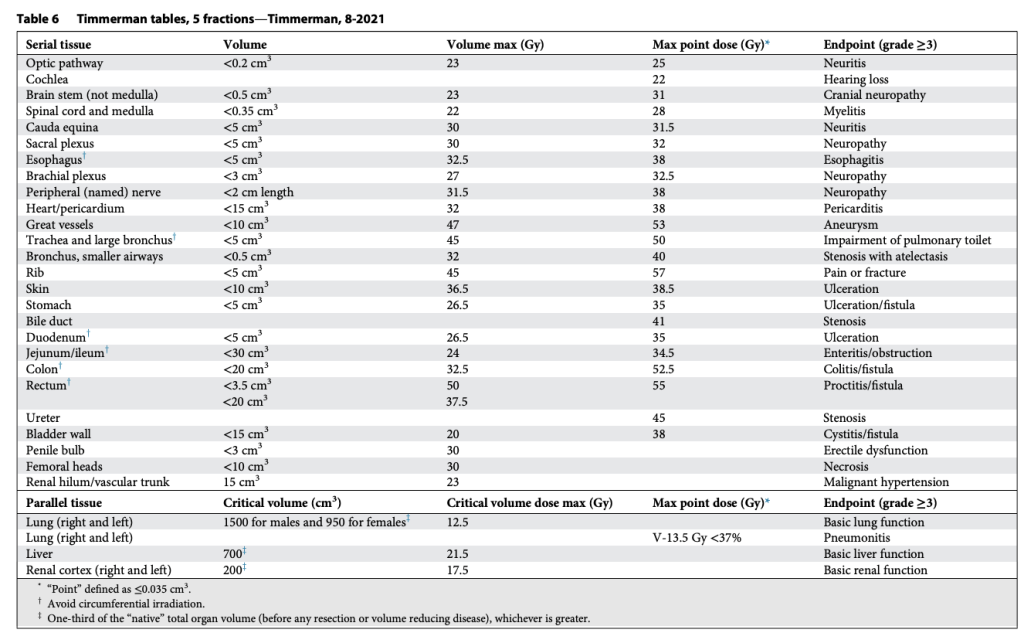
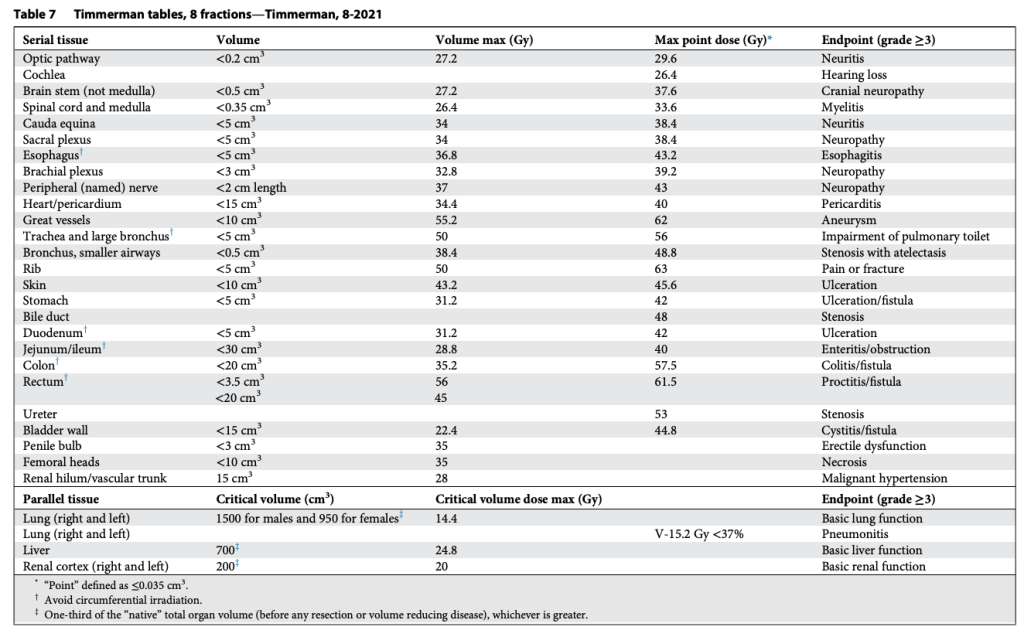
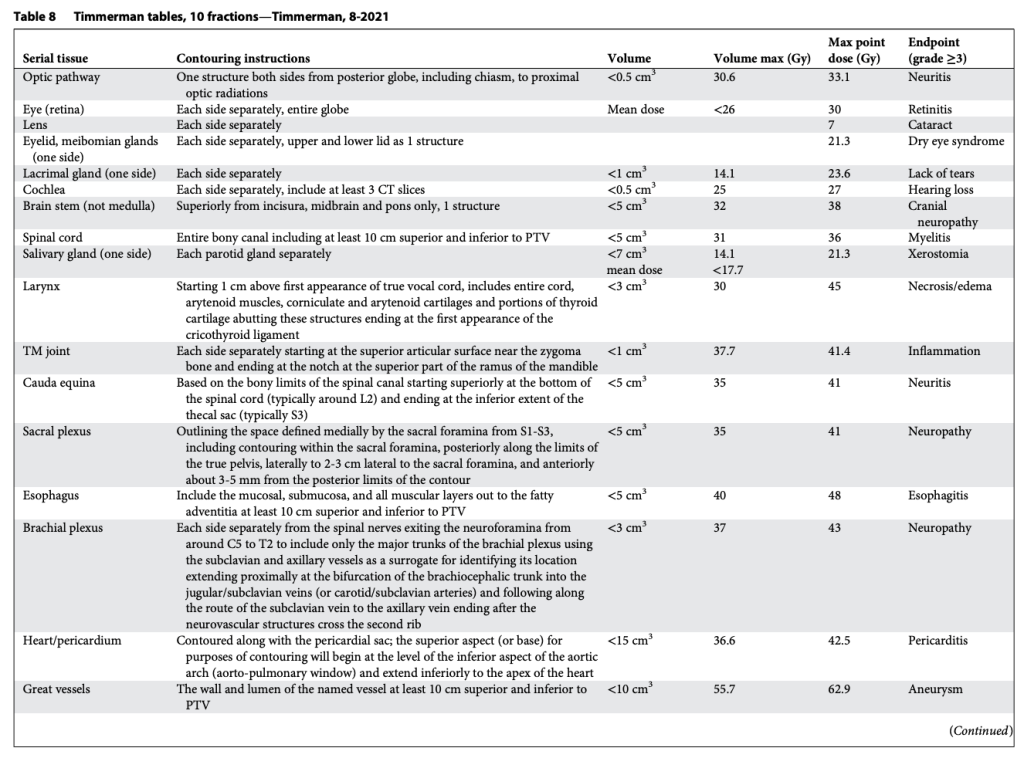
Tất nhiên, khả năng chịu đựng của mô lành thay đổi một cách phi tuyến tính theo số phân liều. Vì vậy, chúng tôi đã xây dựng bảng tương tự cho SABR 1, 4 và 5 phân liều, đồng thời bổ sung thêm giới hạn liều đến một phần thể tích. Lúc đó, chuyên ngành rất quan tâm tới việc mô hình hóa tác động điều trị, và chúng tôi quyết định thử sức. Nhiều người ủng hộ việc dùng mô hình Linear-quadratic (LQ) phổ biến để đơn giản chuyển bảng 3 phân liều thành các lựa chọn SABR khác. Tuy nhiên, việc này nhanh chóng bộc lộ vấn đề, vì mô hình LQ rõ ràng dự đoán quá mức hiệu quả của các điều trị 1 phân liều. Điều này không có gì bất ngờ, bởi LQ vốn được phát triển cho phân liều quy ước (Tức liều nhỏ phía trong “vai” của đường cong sống sót). Thế là chúng tôi thỏa hiệp bằng cách phát triển một mô hình “phổ quát”, kết hợp LQ với mô hình đa mục tiêu (multitarget) cổ điển hơn nhiều. Mô hình sau có khá nhiều dữ liệu sinh học hữu ích từ thập niên 1960–1970 mô tả cơ chế chết tế bào vượt qua vùng “vai”, và chúng ta đều biết rõ tỉ lệ alpha/beta liên quan đến LQ trong vùng này. Với mô hình phổ quát, chúng tôi xây dựng giới hạn cho 1, 3, 4, 5 và 8 phân liều. Lần này, chúng tôi thậm chí còn có thêm dữ liệu trưởng thành hơn cho khả năng dung nạp của tủy sống ở chuột và lợn từ van der Kogel và Medin, và cho đám rối cánh tay từ Forquer. Điều này cho phép chúng tôi nội suy hợp lý và ngoại suy chính xác hơn.
Chúng tôi đã “dại dột” quyết định công bố mô hình phổ quát trên International Journal of Radiation Oncology • Biology • Physics, và điều đó đã dẫn tới một cơn “náo loạn” thứ hai trong cộng đồng xạ trị. Điều mà chúng tôi nghĩ chỉ là một ứng dụng vô hại của các mô hình toán học vốn có lại gây ra lo lắng và thậm chí phẫn nộ. Khi mà chuyên ngành đã bắt đầu từ bỏ xạ trị phân liều cổ điển, nhiều người tin rằng chúng tôi đang từ bỏ luôn cả mô hình LQ đã được kiểm chứng qua thời gian. Chúng tôi yếu ớt bảo vệ mô hình phổ quát, trong khi nhấn mạnh rằng chìa khóa để đảm bảo an toàn cho SABR là phải tiến hành các thử nghiệm lâm sàng tăng liều một cách thận trọng trên người. May mắn thay, các nghiên cứu độc tính này đã được thực hiện, bao gồm cả trong RTOG, và đây thực sự là một chiến lược tốt hơn nhiều so với bất kỳ mô hình toán học nào để xác định mức dung nạp. Khi dữ liệu mới xuất hiện, chúng tôi đã đưa kết quả vào các bảng của mình, dù đôi khi chỉ dựa trên các báo cáo ca bệnh đơn lẻ.
Một câu hỏi hóc búa trong câu chuyện này là: Làm sao có thể công bố một bảng giới hạn liều vốn chủ yếu là do “chế tạo/mô phỏng” mà ra? Chẳng lẽ tạp chí sẽ không yêu cầu thẩm định hoặc tài liệu tham khảo? Đây là lúc một chút “tinh quái” xuất hiện. Joel Tepper đã mời tôi làm biên tập khách mời cho một số Seminars in Radiation Oncology với chủ đề Xạ trị giảm số phân liều. Tôi đồng ý và tập hợp được một nhóm chuyên gia hàng đầu, họ đã đóng góp những bài viết xuất sắc về chủ đề này. Với mỗi số Seminars, biên tập khách mời cần viết một bài giới thiệu, và bài này thực sự được lập chỉ mục trong Index Medicus. Tôi đã quyết định “lén” đưa các bảng giới hạn liều vào phần giới thiệu đó, vì tôi biết chúng sẽ không thể được xuất bản theo cách nào khác. Một bảng mở rộng các giới hạn trong bài được đặt tiêu đề: “Các giới hạn mô lành chủ yếu chưa được xác thực cho SBRT.” Khi đã được xuất bản và lập chỉ mục, tôi dễ dàng tái bản các phiên bản cập nhật của bảng này nhiều lần, chỉ cần viện dẫn lại phần giới thiệu trong Seminars. Ai bảo rằng “kẻ gian lận” thì không bao giờ thắng?
Các bảng này phân biệt hợp lý giữa cấu trúc nối tiếp (Ống, dây thần kinh) và cấu trúc song song (Nhu mô cơ quan), như trình bày trong Bảng 2–11. Sự phân biệt này quan trọng vì hai loại mô này có chiến lược hoàn toàn khác nhau để tránh rối loạn chức năng: Cấu trúc nối tiếp thì “sửa chữa” rất mạnh mẽ, còn cấu trúc song song thì dựa vào sự dư thừa và dự trữ lớn. Mặc dù giới hạn cho cấu trúc nối tiếp rất đơn giản (hiểu nôm na là “không được vượt qua vạch này”), các giới hạn cho cấu trúc song song lại tuân theo nguyên lý “thể tích tới hạn” và được Schefter và Ritter giải thích rất rõ. Rất hợp lý khi không có giới hạn liều trung bình trong các bảng này. Với các điều trị độ đồng dạng cao, nhắm trúng mục tiêu khối u và chỉ vừa “chạm” vào mô lành kề cận, giới hạn liều trung bình tỏ ra vô nghĩa trong việc dự đoán độc tính.
Cá nhân tôi tự hào rằng các bảng giới hạn liều của mình đã góp phần vào sự “vỹ đại” trở lại của HFRT, đặc biệt là SABR. Nhưng cũng cần cảnh báo: “constraints” (giới hạn), đúng như tên gọi, vừa là rào cản vừa là xiềng xích, đặc biệt khi chúng bị khoác thêm ý nghĩa y khoa/pháp lý. Bối cảnh năm 1995 trước khi có SABR đã bị trói buộc bởi quá nhiều giới hạn – ở đây, tôi muốn nói đến những giới hạn ngăn cản ý tưởng mới, nghiên cứu mới và cơ hội mới. Nỗi sợ phân liều kích thước lớn bắt nguồn từ một nhận thức sai lầm về liều và độc tính muộn của mô lành. Nếu nhìn về năm 2021, các giới hạn liều điểm tối đa, cả trong bảng của tôi và của HyTEC, chắc chắn là không còn đúng. Chúng chỉ hữu ích trong mối tương quan với công nghệ kỹ thuật và cách tiếp cận hiện tại. Với sự phát triển tương lai của công nghệ và phương pháp, ví dụ như chùm tia siêu mảnh, tôi dự đoán chúng ta có thể tăng gấp đôi liều tối đa mà tủy sống chịu đựng. Làm được như vậy sẽ mở ra cơ hội loại bỏ những khối u mà ngày nay hiếm khi kiểm soát được. Nhưng điều đó sẽ không xảy ra nếu chúng ta bóp nghẹt đổi mới, “còng tay” các nhà nghiên cứu vốn có thể khám phá ra phương pháp điều trị tốt hơn. Đó chính là nguy cơ của việc coi các giới hạn như một “tôn giáo” xuất phát từ đào tạo và kinh nghiệm hiện tại của chúng ta.
Tôi biết ơn rất nhiều bác sĩ và nhà vật lý đã gửi cho tôi các báo cáo độc tính, những dữ liệu này đã góp phần định hình các bảng qua nhiều năm. Tất nhiên, tôi chắc rằng HyTEC và những bản chỉnh sửa của nó cuối cùng sẽ thay thế bảng của chúng tôi, và điều đó là hoàn toàn đúng. Nhưng hiện tại, chúng tôi vẫn tận hưởng chiến thắng trong “cuộc thi ảo” mà mình chưa từng đăng ký.