Nội dung chính
Bối cảnh ra đời ý tưởng SFRT
Quản lý các khối u lớn, xâm lấn rộng và không thể cắt bỏ là một chủ đề được quan tâm trong điều trị giảm nhẹ. Các tổn thương ung thư lớn chèn ép, xâm lấn tổ chức, cơ quan kế cận, gây ra các triệu chứng ảnh hưởng đến chất lượng cuộc sống của người bệnh. Hơn nữa, người bệnh ung thư khi tiếp nhận điều trị giảm nhẹ, thường toàn trạng đã bị suy giảm bởi tình trạng bệnh tiến triển và độc tính, di chứng của các trị liệu trước đó. Vì vậy, trong trường hợp này, chiến lược quản lý cần được xem xét kỹ, cân bằng giữa hiệu quả điều trị và các tác dụng phụ.
Điều trị toàn thân phát huy hiệu quả hạn chế đối với các tổn thương ung thư lớn, kèm theo nguy cơ độc tính. Phẫu thuật thường là phương án kém khả thi do đòi hỏi cắt bỏ rộng rãi một tổn thương xâm lấn rộng, nguy cơ rủi ro và diễn biến hậu phẫu nặng nề khó có thể chấp nhận trong bối cảnh của điều trị giảm nhẹ.
Do đó, xạ trị giảm nhẹ (p-RT, Palliative Radiation Therapy) là giải pháp được ưu tiên cho mục tiêu kiểm soát triệu chứng và trì hoãn tốc độ tiến triển của bệnh. Liệu trình p-RT tiêu chuẩn được thực hiện với một phác đồ liều thấp đồng nhất, không xét đến thể mô bệnh học của khối u. Ưu tiên khả năng dung nạp hơn hiệu quả, p-RT thường không thể đạt được kết quả kiểm soát bệnh như kỳ vọng, đặc biệt với các khối u thể tích lớn. Xạ trị phân mảnh thể tích bia (Spatial Fractionated Radiation Therapy – SFRT) có thể là phương án giúp giải quyết vấn đề này. SFRT còn được gọi tên là GRID therapy (Liệu pháp xạ trị sử dụng dụng cụ GRID), một trong những hình thái kỹ thuật được giới thiệu sớm nhất của SFRT, từ đầu thế kỷ 20.
Khái niệm SFRT
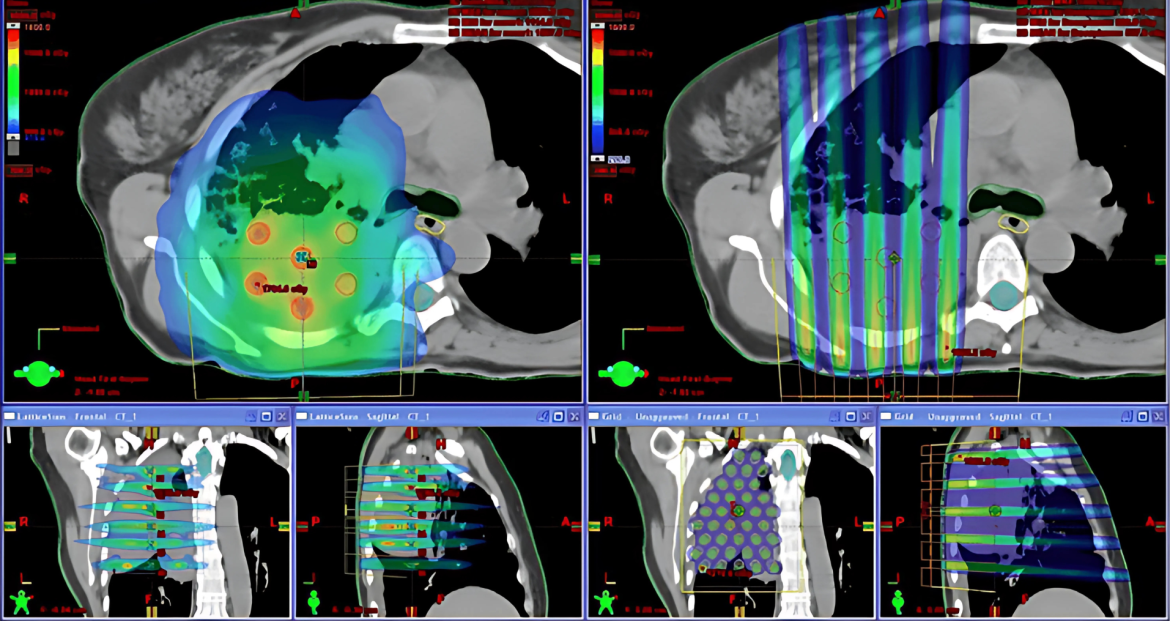
Xạ trị phân mảnh thể tích bia (SFRT) là kỹ thuật xạ trị sử dụng cách thức cấp liều độc đáo, khi đó, một liều xạ cao được phân bố không đồng nhất một cách có chủ đích, đến thể tích bia, với một số phân vùng thể tích bia được định nghĩa để nhận được liều cao hơn bằng cách cấp liều tăng cường đồng thời (Simultaneous Integrated Boost -SIB). Các điểm nóng (Hot Spots) được định vị bên trong thể tích bia và xa các cơ quan nguy cấp kế cận. Cách tiếp cận này nhằm cải thiện đáp ứng của khối u với độc tính liên quan đến xạ trị tối thiểu. Các thử nghiệm lâm sàng đã công bố, cho thấy các kết quả đáng khích lệ, tuy nhiên, các nghiên cứu ở quy mô nhỏ, hồi cứu và không đồng nhất.
Đôi nét về lịch sử
Ban đầu, SFRT được thực hiện với một dụng cụ dạng tấm chắn với các lỗ chuyên dụng (GRID), được Kohler giới thiệu từ năm 1909, sau đó trở nên phổ biến đến những năm 1930. GRID được sử dụng để tạo nên các chùm tia nhỏ có thể hình dung như một bó bút chì (Pencil Beams).

SFRT không nhằm mục đích bao phủ toàn bộ khối u với mức liều đạt được hiệu quả kiểm soát u tối ưu như các cách tiếp cận tiêu chuẩn. Thay vào đó, kỹ thuật này hướng đến cấp một mức liều đạt tới ngưỡng SRS/SBRT (10-20Gy trong 1 phân liều) tại các vùng thể tích nhỏ bên trong khối u, đặc biệt với khối u lớn, mà không gây ra các tổn thương, độc tính nghiêm trọng đến các tổ chức mô xung quanh.
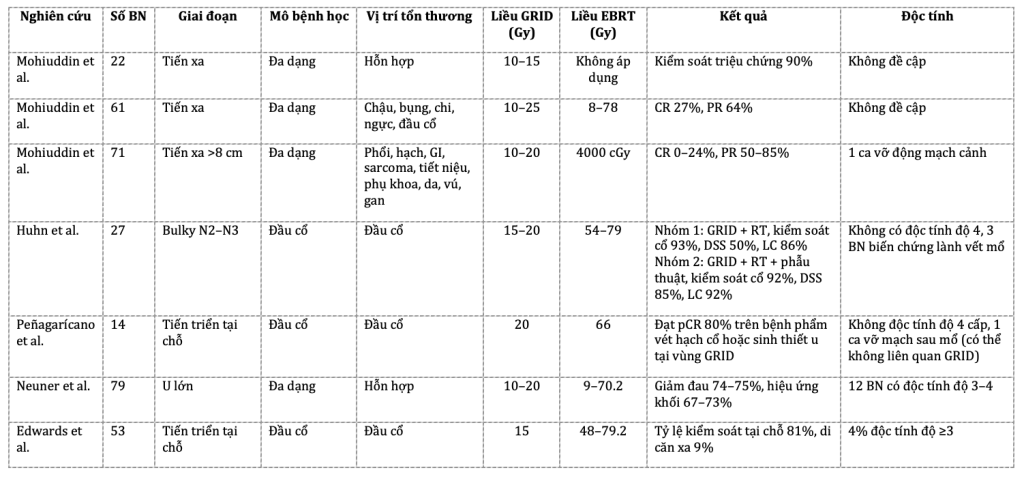
Đến những năm 1990, liệu pháp GRID được thực hiện với chùm tia photon mức năng lượng MV cho các khối u lớn hay tái phát, đã được xạ trị trước đó. Các dữ liệu lâm sàng được công bố chủ yếu tập trung ở các chỉ định điều trị giảm nhẹ. Với sự tiến bộ của các máy gia tốc tuyến tính hiện đại, hệ thống collimator đa lá (MultiLeaf Collimators – MLCs) được sử dụng để tạo nên kết quả phân bố liều tương đương GRID. So với GRID, SFRT dựa trên MLCs có một số ưu thế:
- Đầu máy LINAC đã được trang bị MLCs,
- Tiến trình tính liều (Dosimetry) dễ dàng thực hiện hơn trên hệ thống lập kế hoạch
- Linh hoạt thay đổi kết quả “lưới” phân bố liều
Tuy nhiên, có một vấn đề quan trọng khi thực hiện SFRT với MLCs, đó là hình dạng và kích thước của các chùm tia, do liên quan đến độ dày của các lá collimator, thường không nhỏ và sắc nét như khi dùng khối GRID vật lý. Bên cạnh đó, nguy cơ rò rỉ bức xạ qua khe giữa các lá MLCs có thể thay đổi kết quả phân bố liều.
Với các khối u lớn, nằm sâu, khoảng cách giữa bề mặt da và khối u trở nên đáng kể, kỹ thuật GRID kinh điển với 1 trường chiếu duy nhất hoặc hai trường chiếu không đối xứng, sẽ gặp trở ngại trong phân bố liều khi điểm nóng (Hot-spot) thường rơi vào mô lành. Từ đây, kỹ thuật GRID cải tiến sử dụng xạ trị cắt lớp xoắn ốc (Helical Tomotherapy) hay Điều biến theo thể tích hình cung (Volumetric Arc Therapy) đã được phát triển.
SFRT trong kỷ nguyên 3D hiện đại
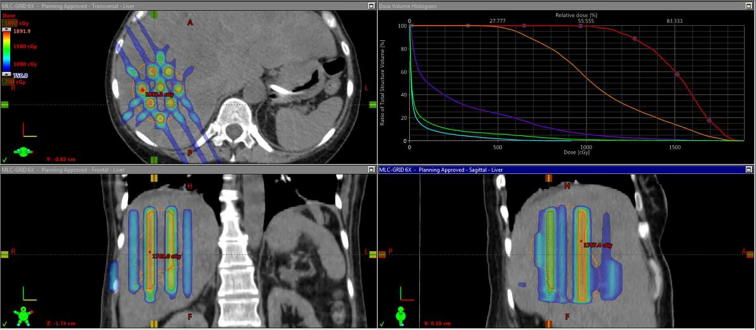
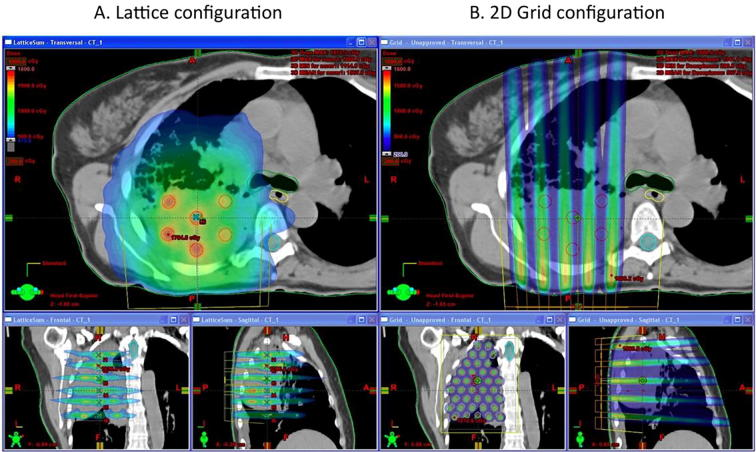
Wu và cộng sự (2010) đã phát triển khái niệm xạ trị LATTICE (LRT), nguyên lý cơ bản là tạo ra các thể tích nhỏ, hình cầu nằm bên trong thể tích u, cách nhau một khoảng nhất định, các thể tích này sẽ nhận một liều xạ cao được gọi là liều đỉnh (Vertice hay Peak), trong khi liều xạ đến vùng còn lại bên trong khối u xen giữa các hình cầu (Valley) và liều xạ đến ngoại vi khối u vẫn được kiểm soát ở mức thấp nhằm tránh các độc tính. LRT được xem là bước cải tiến 3D của kỹ thuật GRID 2D kinh điển. LRT dựa trên:
- Hiệu quả lâm sàng đã được chứng minh của liệu pháp GRID
- Những tiến bộ mới về vật lý và kỹ thuật xạ trị cho phép việc tạo nên các thể tích nhỏ nhận liều cao bên trong thể tích u trở nên khả thi.
LRT đã được ứng dụng trên lâm sàng cho các bệnh nhân có khối u lớn (“Bulky disease”) và chứng tỏ hiệu quả cải thiện kiểm soát tại chỗ mà không làm gia tăng thêm độc tính liên quan đến xạ trị. Amendola và cộng sự đã thực hiện LRT an toàn cho 10 bệnh nhân ung thư phổi không tế bào nhỏ giai đoạn tiến xa, giúp giảm thiểu kích thước u đáng kể và kéo dài thời gian sống thêm cho những người bệnh vốn là ứng viên cho chăm sóc giảm nhẹ cuối đời. Theo ghi nhận của Amendola và cộng sự, LRT không đi kèm với bất kỳ biến chứng đáng kể nào. Liều LRT được kê là 18 Gy đến các vertice, kích thước vertice thay đổi từ 1 – 2 cm, khoảng cách giữa các vertice (Trung tâm đến trung tâm) trung bình là 3,6 cm.
SBRT với SFRT-SBRT-PATHY
Xạ trị định vị lập thể thân (SBRT) sử dụng các hệ thống cố định và kiểm soát tư thế chuyên dụng để đảm bảo một liều xạ rất cao so với phân liều quy ước được phân bố chính xác đến khối u trong một số ít buổi chiếu xạ. Mức liều xạ cao cho thấy kết quả kiểm soát tại chỗ ấn tượng, vượt xa các phác đồ trải liều quy ước.
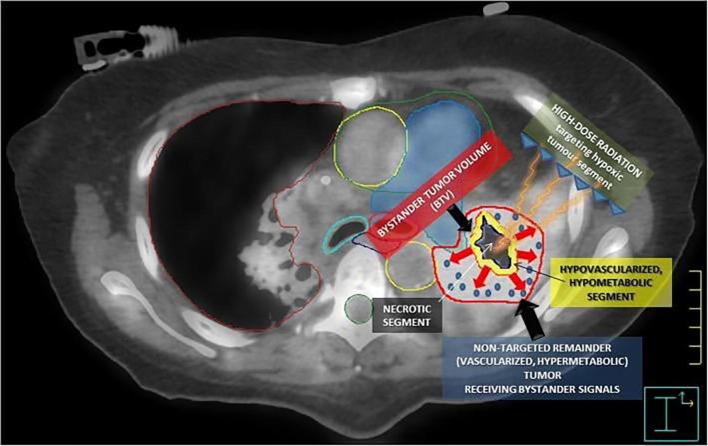
Các nghiên cứu về vai trò cảm ứng của Oxy cho thấy tình trạng thiếu oxy bên trong khối u dẫn đến gia tăng nồng độ các yếu tố HIF (Hypoxia-inducible factors), từ đó kích hoạt các con đường tín hiệu của tăng sinh mạch, giúp tế bào gốc ung thư sống sót, trốn tránh hệ miễn dịch và có khả năng đề kháng với xạ trị. Vì vậy, nếu phần lõi thiếu oxy của khối u trở thành mục tiêu của SBRT, điều này có thể gây ra các biến đổi thứ phát do bức xạ của vi môi trường khối u, góp phần cải thiện kết quả điều trị. Phương pháp phân tích đặc trưng hình ảnh y học (Radiomic) đã được sử dụng để đánh giá các tế bào CD8 thâm nhập vào mô u để dự báo kết cục đáp ứng với liệu pháp miễn dịch kháng PD-1. Vi môi trường u được xem là không đồng nhất, trong đó có khu vực mà tế bào u có khả năng đề kháng hay ác tính tính hơn so với ở khu vực khác. Vùng có tình trạng thiếu oxy trầm trọng hơn bên trong khối u sẽ đòi hỏi mức liều huỷ u (ablative dose) cao hơn so với vùng không thiếu oxy. Dựa trên lý lẽ đó, một số chiến lược tăng cường liều tại các thể tích nhỏ, khu trú bên trong khối u đã được đề xuất. Các chiến lược này tương đồng với triết lý của SFRT và có thể áp dụng cho nhiều vị trí khối u khác nhau. Một nghiên cứu gần đây vận dụng triết lý SFRT, thực hiện SBRT để chiếu xạ một phần u nhắm đến vùng thiếu oxy của các khối u bulky không thể cắt bỏ (Stereotactic Body Radiation Therapy of PArtial Tumor irradiation targeting exclusively the HYpoxic segment – SBRT-PATHY). Liệu pháp này khởi phát hiệu ứng bystander (Tại chỗ) và abscopal (Ở xa). SBRT-PATHY đơn thuần cho kết quả tỷ lệ đáp ứng toàn bộ (96%), không có độc tính (Độ 1 – 4: 0%) và 52% trường hợp ghi nhận hiệu ứng abscopal. Hình ảnh dưới đây biểu diễn cơ sở sinh học bức xạ của hiệu ứng bystander do SBRT-PATHY.
SFRT với liệu pháp hạt
GRID cũng đã được thực hiện với proton, tận dụng ưu thế nổi bật về mặt vật lý của bức xạ proton, đỉnh Bragg. So với photon, bên cạnh có thể tạo nên tỷ số liều nền – đỉnh (Valley to peak ratios) bên trong khối u, liệu pháp GRID với proton cho đường cong liều – độ sâu rơi xuống nhanh chóng phía sau thể tích bia và tạo nên chùm tia đồng nhất hơn. Proton PBS đã được kiểm chứng trên người bệnh, cho thấy có thể giảm liều đến các cơ quan kế cận khi điều trị khối u ở sâu. Ion carbon cũng đã được thử nghiệm với liệu pháp GRID, GRID với các chùm ion carbon rộng 0,5 đến 3 mm có đặc điểm tương tự GRID cổ điển.
Sự phát triển của SFRT với các chùm tia nhỏ hơn
Chùm tia siêu nhỏ (Microbeam) là một chùm bức xạ hẹp với kích thước được tính bằng micromét hoặc nhỏ hơn micromét. Vào những năm 1960, Woodley và cộng sự đã ghi nhận rằng việc mô phỏng các hạt nặng trong không gian có đường kính khoảng 25 micromét, một chùm tia siêu nhỏ có kích thước trong khoảng này có thể tăng đáng kể khả năng dung nạp của não chuột với bức xạ (4000 Gy so với 150 Gy). Sau đó, Slatkin và cộng sự đã nghiên cứu các chùm tia X siêu nhỏ được tạo nên bởi synchrotron và ghi nhận rằng mô não được bảo toàn nếu xạ trị liều cao được được thực hiện với các chùm tia siêu nhỏ. Cơ quan bức xạ Synchrotron châu Âu (ESRF) tại Grenoble (Pháp) đã xây dựng hệ thống phát chùm tia siêu nhỏ cho các thử nghiệm tiền lâm sàng và lâm sàng. Xạ trị với chùm tia siêu nhỏ (MRT) sử dụng các chùm tia X siêu nhỏ (Thường trong khoảng 50 – 600 keV) theo dạng mạng lưới chùm tia được chuẩn trực. MRT có đặc điểm nội tại tương tự với suất liều cao và độ phân kỳ chùm tia tối thiểu. Suất liều cao là cần thiết để có thể cung cấp một liều xạ cao ở ngưỡng điều trị đến các thể tích siêu nhỏ (Microscopic volume). Độ phân kỳ chùm tia tối thiểu giúp đạt được mức độ tập trung liều cao hơn tại thể tích bia. Thông thường, MRT sử dụng các mảng vi phẳng hẹp. MRT có thể cung cấp một liều xạ đầu vào trong khoảng vài trăm Grays, ưu tiên tiêu diệt khối u và không gây ra thêm các độc tính trên mô lành. Trên các thử nghiệm tiền lâm sàng, MRT cải thiện sống thêm trên chuột, tuy nhiên, cho đến nay chưa được báo cáo trên các động vật lớn hơn. Việc đưa MRT ứng dụng vào lâm sàng gặp 2 thách thức chủ yếu: Thiết lập hiệu quả vị trí của chùm tia và người bệnh; Sự chuyển đổi lớn về tư duy và khái niệm trong lĩnh vực xạ trị để chấp nhận cách tiếp cận phân bố liều không đồng nhất trong điều trị và chuẩn hoá trong thực hành đối với một kỹ thuật mới.
Cơ sở sinh học bức xạ của SFRT
Những phát hiện về sinh học bức xạ từ liệu pháp GRID
Những hiểu biết hiện nay về cơ sở sinh học bức xạ đằng sau liệu pháp GRID liên quan đến hiệu ứng bystander, tổn thương mạch máu và đáp ứng miễn dịch kháng u.
Thuật ngữ “Hiệu ứng Bystander” mô tả hiện tượng các tế bào chịu tác động bởi tia xạ truyền đạt các biểu hiện tổn thương đến các tế bào khác không phải là mục tiêu trực tiếp của xạ trị. Trong liệu pháp GRID, hiệu ứng bystander chủ yếu liên quan đến những thay đổi xảy ra tại các tế bào nằm ở vùng nhận liều thấp (Valley dose). Griffin và cộng sự đã chứng minh bystander đã gây chết các tế bào nằm lân cận các thể tích nhận liều cao trong liệu pháp GRID. Hơn nữa, hiện tượng chết tế bào ở những vùng không phải là mục tiêu trực tiếp của xạ trị được phát hiện là phổ biến hơn so với chết tế bào gây ra do liều nền hoặc liều phân tán, ghi nhận này cho thấy chiếu xạ GRID liều cao (10 Gy) thật sự đã kích hoạt hiệu ứng bystander gây độc tế bào và cũng có thể một liều xạ thấp đã tạo hiệu ứng thu hút sự thâm nhập các tế bào T CD8 đến những khu vực này, trong khi liều xạ cao hơn lại gây chết các tế bào miễn dịch mới thâm nhập đến trong quá trình xạ trị.
Hiệu ứng bystander không được quan sát ở xạ trị với phân liều quy ước đến toàn bộ khối u. TNF-α và TRA IL đã được đề cập đến với một vai trò trong hiệu ứng bystander. Các yếu tố này đươc hình thành tại các tế bào ở khu vực nhận liều cao của liệu pháp GRID, về mặt lý thyết, chúng có thể kích hoạt hiệu ứng bystander tại các tế bào ở vùng kế cận.
Các dữ liệu trên cho thấy liệu pháp GRID có thể khởi phát một cơ chế gây chết tế bào khác biệt, đặc biệt ở các khối u bulky hay có các vùng lõi thiếu oxy. Nghiên cứu của Garcia-Barros và cộng sự đã gợi ý rằng chiếu xạ một liều cao 15 Gy tạo ra một vùng môi trường “Tổn thương gây chết tiềm tàng” khiến các tế bào ở đây trở nên nhạy cảm hơn với liều chiếu xạ tiếp theo, đặc biệt là các tế bào nội mô của hệ thống vi mạch của khối u. Ceramide được tạo ra từ sphingomyelin bằng SMase, được chứng minh có liên quan đến cơ chế tăng nhạy cảm của các tế bào nội mô vi mạch với xạ trị, dẫn đến chết tế bào theo chương trình. Khi hoạt động SMase và nồng độ của ceramide được định lượng ở các bệnh nhân nhận điều trị SFRT với GRID, sự gia tăng hoạt động SMase và nồng độ ceramide chỉ được ghi nhận ở những bệnh nhân có đáp ứng hoàn toàn hoặc một phần với SFRT, trái ngược với nhóm không đáp ứng. Dựa trên những hiểu biết hiện tại, mỗi tế bào nội mô trong hệ thống mạch máu của khối u sẽ cung cấp máu cho một phân mảnh hay đơn vị gồm hàng ngàn tế bào u. Do đó, tiêu diệt tế bào nội mô hay gây tắc các nhánh mao mạch nhỏ bên trong khối u có thể dẫn đến hiệu ứng gây chết hàng loạt tế bào u. Dữ liệu của các thử nghiệm trên chuột cho thấy xạ trị với phân liều lớn hơn 10 Gy có thể gây ra tổn thương trầm trọng mạch máu và giảm hiệu quả cấp máu. Hiện tượng chết tế bào u thứ phát, xảy ra sau chiếu xạ 15 – 30 Gy ở động vật do những biến đổi của vi môi trường bên trong khối u sau khi các mạch máu bị tắc do xạ trị. Đây sẽ là lời lý giải hợp lý cho tác dụng debulking (Giảm thiểu khối lượng u) của liệu pháp GRID.
SFRT và các đáp ứng miễn dịch
Hiệu ứng abscopal — hiện tượng khối u ngoài vùng chiếu xạ cũng thoái triển sau khi xạ trị vào một khối u khác — được ghi nhận là có liên quan đến hoạt hóa hệ miễn dịch. Trong những năm gần đây, sự kết hợp giữa xạ trị và liệu pháp miễn dịch đã được xem là một hướng đi triển vọng nhằm gia tăng tần suất xuất hiện của hiệu ứng này.
Nhiều bằng chứng tiền lâm sàng cho thấy rằng liều xạ trong khoảng 8–10 Gy mỗi phân liều, đặc biệt khi áp dụng 1–3 phân liều, có thể tối ưu hóa việc giải phóng các sản phẩm phân giải tế bào ung thư (tumor lysates) và neoantigen, từ đó kích hoạt miễn dịch đặc hiệu. Trong nghiên cứu của Peters và cộng sự, việc áp dụng kỹ thuật GRID/SFRT liều cao đã tạo ra đáp ứng abscopal mạnh hơn ở khối u không được chiếu xạ trực tiếp, so với xạ trị toàn bộ tổn thương với trường chiếu mở rộng. Điều này cho thấy SFRT không chỉ kiểm soát tại chỗ mà còn có tiềm năng kích hoạt miễn dịch hệ thống.
Các mô hình chuột mang khối mô ghép cho thấy SFRT một phân liều duy nhất có thể làm chậm đáng kể sự phát triển của khối u ở vị trí xa, không được chiếu xạ. Phân tích mô học cho thấy sự gia tăng rõ rệt của tế bào T và các cytokine của phản ứng viêm tại khối u đối bên sau khi khối u bên còn lại được xạ trị 50% thể tích bằng SFRT. Những quan sát này củng cố vai trò của miễn dịch tế bào trong hiện tượng abscopal được kích hoạt bởi SFRT.
Trên lâm sàng, dữ liệu sơ bộ cho thấy các khối u được xạ trị một phần có thể trở nên “miễn dịch hóa”. Một ví dụ là việc sử dụng liều xạ cao duy nhất nhắm vào vùng thiếu oxy của khối u dưới hướng dẫn hình ảnh, có thể gây hiệu ứng abscopal. Đáng chú ý, một thử nghiệm pha II ngẫu nhiên trên bệnh nhân ung thư phổi không tế bào nhỏ (NSCLC) đã chứng minh rằng SBRT có thể “chuyển hóa” khối u lạnh thành khối u nóng. Hiệu quả điều trị cải thiện đáng kể ở nhóm bệnh nhân có biểu hiện PD-L1 thấp khi được kết hợp pembrolizumab với SBRT, so với pembrolizumab đơn thuần.
Các típ u có thể nhận được lợi ích của SFRT
Meigooni và cộng sự đã tổng hợp các kết quả lâm sàng từ nhiều nghiên cứu đã được báo cáo trong y văn, phân tích hiệu quả của liệu pháp GRID trên các loại u khác nhau về mô bệnh học và vị trí tổn thương. Tỷ lệ đáp ứng toàn bộ trên lâm sàng được ghi nhận như sau:
- U xương và phần mềm: Osteosarcoma (100%), Liposarcoma (50%), Leiomyosarcoma (100%), Sarcoma nói chung (83–94%).
- Ung thư biểu mô vảy (SCC): đạt 92–94%
- Các loại khác: Melanoma (50–83%), Adenocarcinoma (69%), Ung thư đại trực tràng (100%).
- Đặc biệt ở vùng đầu cổ, tỷ lệ đáp ứng rất khác biệt giữa các vị trí: Tuyến mang tai (0%), Đáy lưỡi (30%), Xoang hàm (50%), trong khi vòm mũi họng, thanh quản, tam giác sau lợi đạt 100%, a-mi-đan chỉ 25%.
Các kết quả này cho thấy mức độ đáp ứng với SFRT thay đổi đáng kể tùy thuộc vào mô bệnh học và vị trí giải phẫu, tuy nhiên nhiều loại u có đáp ứng cao vượt kỳ vọng, kể cả các khối u thường kháng xạ.
Đáng chú ý, một số báo cáo gần đây nhấn mạnh tiềm năng của SFRT trong điều trị u kháng xạ, đặc biệt là sarcoma. Một trường hợp điển hình là bệnh nhân có khối sarcoma tế bào hình thoi kích thước lớn (631 cm³) được điều trị bằng SFRT 18 Gy, sau đó là cEBRT 32 Gy. Kết quả mô bệnh học sau phẫu thuật cho thấy chỉ còn 5–10% tế bào u sống, với mô u còn lại chỉ 65 cm³, chủ yếu là xơ hóa và hoại tử — tương đương mức đáp ứng 90%, vượt xa mức thoái triển hình ảnh học chỉ 0–0.5% nếu xạ trị ngoài 50 Gy đơn thuần.
Một nghiên cứu sử dụng kỹ thuật mô phỏng Monte Carlo đã được thực hiện để mô phỏng phân bố liều của liệu pháp GRID kinh điển. Với mô hình Linear Quadratic (LQ) và Hug–Kellerer (H-K), các chỉ số Therapeutic Ratio (TR) và Equivalent Uniform Dose (EUD) được xác định. Kết quả cho thấy TR của các khối u kháng xạ tăng lên rõ rệt theo mức liều xạ, trong khi TR của các u nhạy xạ không thay đổi nhiều, gợi ý rằng liệu pháp GRID có thể đặc biệt hữu ích về mặt sinh học đối với các khối u kháng xạ.
Một số xu hướng phát triển tiềm năng của SFRT
Minibeam Radiation Therapy (MBRT): Xạ trị chùm tia nhỏ
Minibeam (MBRT) là một biến thể của microbeam, với bề rộng chùm tia lớn hơn (500–700 μm, so với 25–100 μm ở MRT), và khoảng cách giữa các chùm thường gấp đôi chiều rộng (1–3 mm). Cũng như MRT, MBRT thường được thực hiện với các chùm tia mức năng lượng kilovoltage, song có một số ưu điểm nổi bật:
- Hiệu ứng bảo toàn mô (Tissue-sparing effect) của MBRT vẫn được duy trì ở các chùm tia có kích thước lớn hơn 0.68 mm.
- Không bị ảnh hưởng bởi nhịp đập của tim, không đòi hỏi suất liều quá cao như MRT.
- Triển khai về mặt kỹ thuật dễ hơn MRT, thích hợp hơn trong điều kiện tiền lâm sàng và lâm sàng hạn chế về hạ tầng synchrotron.
Một số thiết bị chiếu xạ động vật nhỏ đã được phát triển để tạo ra mẫu minibeam với tỷ số liều đỉnh-thung lũng (PVDR) tương đương các máy synchrotron. MBRT đã cho thấy gây tổn thương da ít trầm trọng hơn và hầu như không gây tổn thương não ở động vật gặm nhấm (1 phân liều 20 Gy) so với nhóm được xạ trị truyền thống. Ngoài ra:
- Carbon ion minibeam với độ dày 525 μm đã được sử dụng để điều trị tổn thương não thỏ, kiểm soát tốt mà không gây tổn thương não lan rộng.
- Proton MBRT với chùm tia rộng 400 μm và khoảng cách 3200 μm giữa các chùm tia đã được thử nghiệm trên chuột mang glioma, với liều đỉnh 70 Gy/phân liều – cho thấy hiệu quả kiểm soát khối u cao, tiêu diệt hoàn toàn u ở 22% trường hợp, đồng thời hạn chế tổn thương não.
Điểm vượt trội của carbon và proton minibeam là khả năng giảm liều tại mô lành gần vùng chiếu, từ đó cho phép nâng liều trong điều trị các khối u kháng xạ.
SFRT trong xạ trị chính xác (precision radiotherapy)
SFRT và xạ trị quy ước có thể hội tụ trong xu hướng xạ trị chính xác, nơi khối u được bao phủ liều toàn bộ nhưng liều phân bố không đồng nhất — được điều chỉnh dựa trên sự khác biệt sinh học nội tại của từng vùng trong khối u. Điều này bao gồm:
- Mức độ nhạy xạ, mức độ ác tính của khối u, hoặc hình thái đột biến gen hay các con đường dẫn truyền tín hiệu tại các ổ tổn thương cụ thể bên trong khối u.
- Sự hỗ trợ của radiomics cho phép nhận diện các vùng dị biệt nội u — ví dụ như vùng chuyển hóa cao bất thường trên FDG-PET/CT trong u phổi không tế bào nhỏ (NSCLC), có liên quan chặt chẽ đến tiên lượng di căn xa và sống còn toàn bộ.
Khái niệm này đã được ứng dụng thử nghiệm trong phương pháp “dose painting by number (DPbN)”, khi đó, từng voxel của u được gán xác suất kiểm soát tại chỗ và chỉ định liều xạ tối ưu. Kết quả cho thấy:
- Những vùng có nguy cơ cao đòi hỏi liều điều trị >100 Gy để đạt kiểm soát tối ưu – điều này khó thực hiện với phác đồ chuẩn (35×2 Gy), nhưng khả thi với các kỹ thuật như DPbN hoặc SFRT.
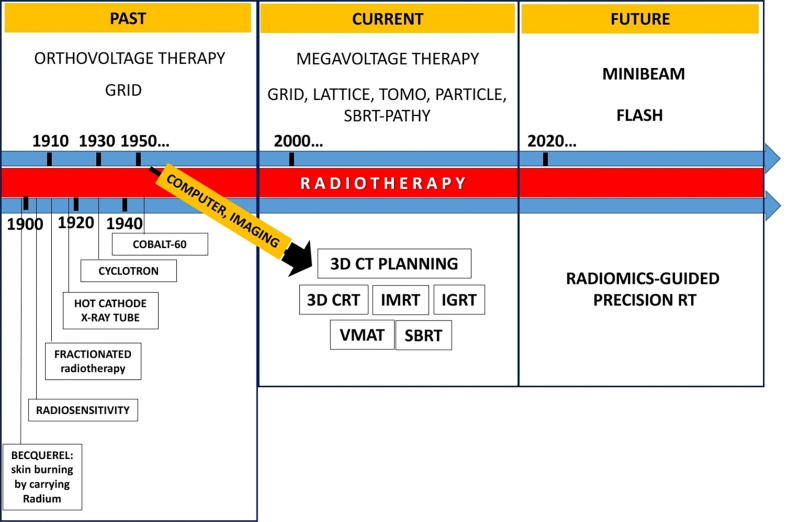
Do đó, SFRT không chỉ có triển vọng trong điều trị khối u lớn hoặc u kháng xạ, mà còn có thể là một phần của chiến lược xạ trị thích ứng cá thể hóa, có thể được tích hợp vào lập kế hoạch điều trị hằng ngày. Một điểm thú vị là SFRT và xạ trị truyền thống cùng phát triển song hành, được ví như hình tượng âm–dương: Mỗi một cách thức thực hiện xạ trị truyền thống đều có thể ứng dụng một cách sáng tạo trong thực hiện SFRT.
Kết luận
SFRT có ý nghĩa quan trọng với cách tiếp cận độc đáo nhắm đến bao phủ một phần hay toàn bộ khối u trong một phân bố liều xạ không đồng nhất, mang lại cho lĩnh vực xạ trị những giải pháp ứng dụng sáng tạo, bổ trợ cho các kỹ thuật xạ trị tiêu chuẩn. Trong khi ứng dụng SFRT trên lâm sàng còn giới hạn tại một số trung tâm, phổ biến cho các chỉ định điều trị giảm nhẹ hay trường hợp tái phát, SFRT có tiềm năng ứng dụng trong điều trị các ung thư nguyên phát theo hướng triệt căn như ung thư vùng đầu cổ, phổi, vú, phụ khoa và sarcoma. Các thử nghiệm lâm sàng tích hợp SFRT như một giải pháp tăng cường liều hoặc kỹ thuật xạ trị chủ đạo cần được khuyến khích thực hiện. Ứng dụng tương lại của khái niệm SFRT sẽ phụ thuộc sự tiến bộ của kỹ thuật và những hiểu biết sâu sắc hơn về cơ chế sinh học xảy ra tại khối u hay mô lành bị chiếu xạ với SFRT.
Bài viết gốc: