Bài viết gốc trên Seminars in Radiation Oncology.
Tác giả: Mario Levis (Khoa Ung bướu, Đại học Torino, Ý) và Michael Oertel (Khoa Xạ trị, Viện trường Muenster, Đức)
Đường dẫn: https://doi.org/10.1016/j.semradonc.2024.07.013
Vai trò của xạ trị trong điều trị u lympho đang thay đổi nhanh chóng. Sự phát triển của các liệu pháp toàn thân mới và ứng dụng FDG-PET trong vai trò của một yếu tố tiên lượng bệnh dựa trên đặc điểm chuyển hóa, đang thúc đẩy một tiến trình định hình lại các phác đồ điều trị. Trong bối cảnh này, chỉ định xạ trị đang dần được rút gọn cho một số trường hợp, bao gồm các bệnh nhân nguy cơ thấp, nhằm tránh đối diện với nguy cơ của các biến chứng muộn sau xạ trị. Trong hơn một thập kỷ vừa qua, những thay đổi đáng chú ý nhất trong bức tranh toàn cảnh về chiến lược điều trị được ghi nhận cho u lympho Hodgkin giai đoạn tiến xa và u lympho tế bào B lớn lan tỏa. Mục đích chính của bài viết này là xem xét lại toàn diện y văn cập nhật về các chỉ định của xạ trị trong các bệnh lý này, nhấn mạnh ưu và nhược điểm của chiến lược quản lý với PET dẫn đường và giới thiệu một số xu hướng mới cho tương lai, kết hợp xạ trị và các liệu pháp toàn thân mới trong cả điều trị bước đầu và khi bệnh tái phát.
Nội dung chính
Kỳ 1: U lympho Hodgkin giai đoạn tiến xa
Chỉ định xạ trị củng cố – Y văn trước kỷ nguyên PET
Trước khi các thăm dò chức năng xuất hiện, xạ trị cũng cố đã từng là một thành phần quan trọng của phác đồ điều trị bước đầu cho một phân nhóm chọn lọc bệnh nhân u lympho Hodgkin thể kinh điển giai đoạn tiến xa, sở hữu các đặc điểm bất lợi. Đặc biệt, hiệu quả của xạ trị đã được chứng minh cho các bệnh nhân có tổn thương ban đầu bulky hay chỉ đáp ứng một phần về hình thái sau liệu trình điều trị toàn thân. Nhìn lại lịch sử, nhiều nghiên cứu về u lympho Hodgkin thể kinh điển (cHL) giai đoạn tiến xa bao gồm cả những bệnh nhân giai đoạn IIB có các yếu tố không thuận lợi. Một số nghiên cứu cũng đã chỉ ra rằng vai trò của xạ trị củng cố phụ thuộc “sức mạnh” của phác đồ nội khoa và mức độ đáp ứng về hình thái. Thử nghiệm UK LY09 không ngẫu nhiên, không cho thấy sự khác biệt giữa các phác đồ xen kẽ nhiều thuốc với ABVD (Doxorubicin, bleomycin, vinblastine và dacarbazine), bên cạnh đó, xác định lợi ích rõ ràng của xạ trị củng cố (30 đến 35 Gy) tại tổn thương bulky hoặc tồn dư sau hóa trị. Hơn nữa, tác động của xạ trị lên PFS được khẳng định sau hiệu chỉnh các biến số gây nhiễu trong phân tích đa biến với các bệnh nhân đáp ứng không hoàn toàn với hóa trị (HR = 0,25). Ở một phương diện khác, các kết quả khác nhau được ghi nhận khi phác đồ tăng cường BEACOPP_leo thang (Bleomycin, etoposide, doxorubicin, cyclophosphamide, vincristine, procarbazine, và prednisone) được ứng dụng thay cho ABVD. Thử nghiệm GHSG HD12 cho thấy xạ trị củng cố cải thiện kiểm soát bệnh ở các bệnh nhân có bệnh tồn dư đo được trên 1,5cm, nhưng không phải với tất cả trường hợp có tổn thương bulky đạt được đáp ứng hình thái hoàn toàn sau hóa trị BEACOPP. Hai thử nghiệm này gợi mở rằng đóng góp của xạ trị có thể liên quan đến cường độ của hóa trị và lợi ích từ xạ trị củng cố tại các vị trí bulky ban đầu sau ABVD không ghi nhận được sau BEACOPP_leo thang ở những trường hợp đạt đáp ứng hoàn toàn.
Chỉ định của xạ trị củng cố – Dữ liệu gần đây với chiến lược tùy biến dựa trên PET
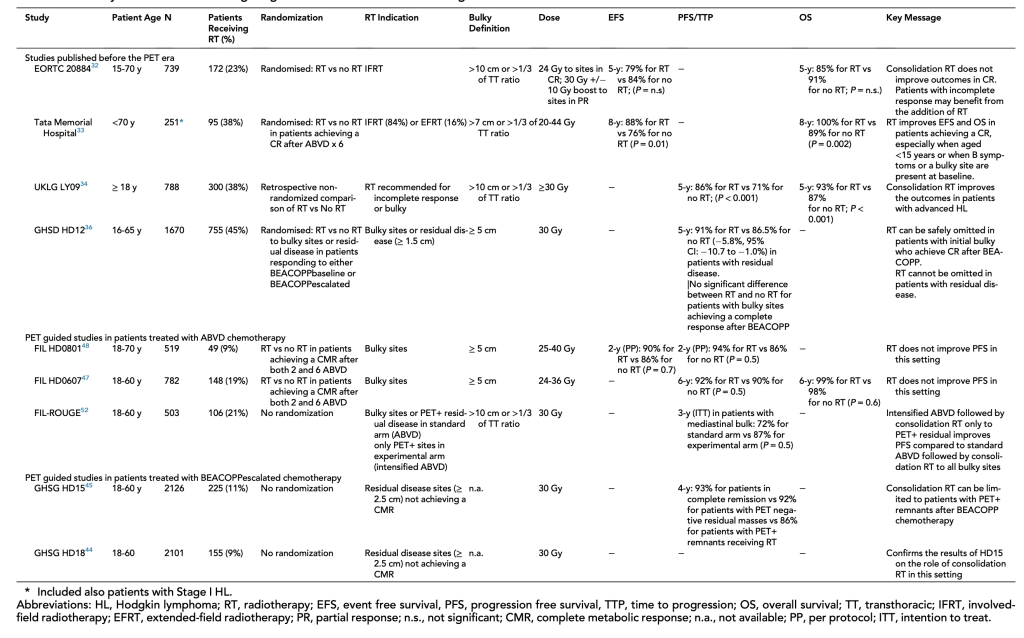
Phác đồ điều trị cho cHL giai đoạn tiến xa đang thay đổi đáng kể trong kỷ nguyên mới với sự ra đời của các thăm dò hình ảnh chuyển hóa. Thật vây, chụp cắt lớp phát xạ positron (PET) cải thiện hiệu quả đánh giá giai đoạn bệnh ban đầu và, đặc biệt, trong đánh giá đáp ứng với hóa trị. Một số nghiên cứu đã chứng minh giá trị dự báo của hình ảnh PET lặp lại sau 2 chu kỳ hóa trị (PET2) với cHL giai đoạn tiến xa, là động lực chính cho một loạt nghiên cứu đánh giá chiến lược điều trị thích ứng với đáp ứng trên PET bằng cách tăng cường liệu pháp toàn thân cho các bệnh nhân PET2 dương tính hoặc xuống thang điều trị khi PET2 âm tính. Xấp xỉ 25% bệnh nhân (19 – 42%) được tuyển chọn vào các nghiên cứu này có chẩn đoán cHL giai đoạn IIB, tương tự các nghiên cứu cổ điển. Kết cục lâm sàng khả quan của các bệnh nhân PET2 âm tính trong các dữ liệu gần đây, tỷ lệ PFS 2 năm > 80%, dẫn đến giả thiết rằng việc đạt được kết quả đáp ứng hoàn toàn về mặt chuyển hóa (cMR) có thể đối kháng tác động tiêu cực đến tiên lượng của các yếu tố lâm sàng như tổn thương ban đầu bulky. Bảng 1 tổng hợp kết quả của các nghiên cứu khảo sát vai trò của xạ trị củng cố trong cHL giai đoạn tiến xa. Trong thử nghiệm GHSG HD15, xạ trị củng cố chỉ được thực hiện cho các bệnh nhân có tổn thương tồn dư trên 2,5 cm, không đạt CMR (Điểm Dauville >= 3) sau 6 – 8 chu kỳ BEACOPP_leo thang. Trong nghiên cứu này, các bệnh nhân với tổn thương tồn dư trên 2,5 cm đạt CMR sau hóa trị có tỷ lệ PFS rất tương đồng với các bệnh nhân có đáp ứng hoàn toàn về hình thái (PFS 4 năm 92% so với 93%). Các kết quả này cho thấy tính an toàn của việc bỏ qua xạ trị nếu bệnh nhân đạt CMR, bất kể sự hiện diện của tổn thương bulky ban đầu và kích thước u tồn dư sau BEACOPP_leo thang. Ở một nhóm thiểu số người bệnh đạt đáp ứng một phần về chuyển hóa tại PET sau hóa trị (26%), xạ trị nên được chỉ định, mang lại tỷ lệ PFS khả quan, 86% tại thời điểm 4 năm, có thể so sánh với các bệnh nhân PET âm tính (86% so với 93%, p = 0,02) và tránh việc phải sử dụng liệu pháp hóa trị liều cao cứu vãn. Tuy nhiên, cần đặc biệt chú ý không ngoại suy các kết quả này cho các bệnh nhân được điều trị với phác đồ hóa trị cường độ nhẹ hơn (Ví dụ: ABVD).
Một số thử nghiệm đã áp dụng cách tiếp cận tương tự, tùy biến điều trị theo đáp ứng trên PET, cho các bệnh nhân được điều trị với phác đồ ABVD. Trong thử nghiệm RATHL, các bệnh nhân có PET2 âm tính được phân nhóm ngẫu nhiên nhận ABVD hoặc một phác đồ hiệu chỉnh, bỏ bleomycin (AVD) cho 4 chu kỳ còn lại, nếu PET2 dương tính, bệnh nhân được tăng cường hóa trị với BEACOPP_leo thang. Quyết định xạ trị củng cố tại vị trí bulky hoặc tồn dư đạt CMR được dành cho bác sĩ lâm sàng, tuy nhiên, không được khuyến khích. Chỉ có 3% những bệnh nhân này được xạ trị củng cố, vì vậy, không thể đi đến kết luận cuối cùng. Trong phân tích đa biến, tổn thương ban đầu bulky không đi kèm với thất bại điều trị ở nhóm bệnh nhân có PET2 âm tính, nhưng chỉ 28% bệnh nhân nhóm này ghi nhận tổn thương ban đầu bulky, trong khi tỷ lệ này là 46% ở nhóm PET2 dương tính (Sau đó nhận phác đồ hóa trị tăng cường). Điều này gợi mở rằng tổn thương bulky ít khả năng đạt CMR tại PET2, vì vậy thường cần hóa trị tăng cường, đánh đổi nguy cơ độc tính cao hơn. Vẫn chưa rõ ràng nếu các bệnh nhân có tổn thương ban đầu bulky, không đạt được CMR tại PET2, có thể có kết cục tương đương nếu tiếp tục ABVD sau đó xạ trị củng cố, thay vì chuyển sang phác đồ hóa trị tăng cường. Hơn nữa, chúng ta cũng chưa biết liệu trình điều trị nào (Hóa trị tăng cường hay xạ trị củng cố) sẽ gây ra gánh nặng độc tính nhiều hơn.
Hai thử nghiệm ngẫu nhiên tương tự từ Ý, nghiên cứu hiệu quả của tăng cường sớm điều trị toàn thân cho các bệnh nhân PET2 dương tính, đồng thời khảo sát vai trò của xạ trị củng cố tại vị trí bulky ban đầu (>= 5cm) cho các bệnh nhân đạt PET âm tính sau 2 (PET2) và 6 chu kỳ ABVD (PET6). Cả hai nghiên cứu đều báo cáo các kết quả tương đồng, cho thấy không có lợi ích của xạ trị củng cố cho toàn bộ quần thể đối tượng bệnh nhân nghiên cứu. Trong thử nghiệm GITIL HD0607, 296 bệnh nhân có tổn thương bulky ban đầu được phân ngẫu nhiên để nhận xạ trị (148 bệnh nhân) hoặc theo dõi (148 bệnh nhân). PFS 6 năm không có khác biệt có ý nghĩa giữa 2 nhóm (92% so với 90%, p = 0,48). Trong thử nghiệm FIL HD0801, chỉ có 116 bệnh nhân được phân ngẫu nhiên nhận xạ trị củng cố hoặc theo dõi (Mỗi nhóm 58 bệnh nhân). Thêm một lần nữa, không có sự khác biệt có ý nghĩa được ghi nhận dù ưu thế có vẻ nghiên về nhánh xạ trị củng cố (PFS 2 năm theo protocol là 94% so với 86%, p = 0,5). Các NC trên đều cho thấy nhóm bệnh nhân đạt CMR ở PET2 và cả PET lần cuối cùng sau 6 chu kỳ ABVD có kết cục lâm sàng thuận lợi mà không cần bổ sung xạ trị củng cố các vị trí bulky. Đáng tiếc là các NC này cũng mắc phải một số khiếm khuyết về thống kê đã hạn chế giá trị ngoại suy của các kết quả và đòi hỏi phải diễn giải một cách thận trọng. Thử nghiệm GITIL HD0607 không có tính toán lực (Power calculation) và tỷ lệ PFS toàn bộ cao, một cách đáng ngạc nhiên, so với các nghiên cứu tương tự, đặt ra hoài nghi nếu so sánh với dữ liệu thực tế. Trong khi đó, HD0801 được thiết kế với một giả thiết đánh giá quá cao EFS 2 năm vượt trội 20% ở nhánh xạ trị, hệ quả là cỡ mẫu nhỏ đã không đủ sức mạnh để phát hiện bất kỳ khác biệt nào về EFS lẫn PFS < 10%.
Một vấn đề khác, định nghĩa tổn thương bulk cho cHL đã thay đổi theo thời gian và đến nay, vẫn chưa thống nhất. Các thử nghiệm RATHL, SWOG 0816 và GHSG HD18 sử dụng các định nghĩa bulky cổ điển, bao gồm chiều rộng lớn nhất của khối u lớn hơn hoặc bằng 1/3 đường kính lồng ngực ngang mức T5/T6 trên phim Xquang hoặc kích thước lớn nhất đo được >= 10 cm trên bất kỳ thăm dò chẩn đoán hình ảnh nào. Các thử nghiệm HD0607 và HD0801 tại Ý chọn ngưỡng cut-off để xác định tổn thương bulky là 5 cm. Cũng cần nói thêm, đường kính lớn nhất của tổn thương > 7 cm là một yếu tố dự báo cho kết cục PFS tồi trong thử nghiệm HD060. Giá trị cutoff tương tự cũng được đánh giá là ngưỡng tối ưu để xác định tổn thương bulky với cHL giai đoạn sớm, với tiềm năng giảm bớt ý nghĩa tiên lượng của nó nếu bổ sung xạ trị. Mối liên hệ phức tại giữa tính chất bulky và kết cục lâm sàng cũng đã được tìm hiều trong một nghiên cứu quốc tế đa trung tâm gần đây. Các tác giả ghi nhận được OS tốt hơn ở các bệnh nhân có tổn thương trung thất bulky so với các trường hợp có tổn thương bulky nằm ngoài trung thất, cho thấy tác động tiềm năng từ các yếu tố lâm sàng khác không liên quan đơn thuần, trực tiếp đến gánh nặng khối u. Những khác biệt này cản trở một định nghĩa thống nhất cho tổn thương bulky trên thực hành lâm sàng hàng ngày, đòi hỏi hiểu rõ các định nghĩa cụ thể được sử dụng trong mỗi bối cảnh nhất định. Thêm vào đó, tác động qua lại giữa tính chất bulky với cường độ của điều trị toàn thân và kết quả đáp ứng cần được xem xét đồng bộ.
Vậy, có thể rút ra được bài học gì từ tất cả các nghiên cứu sử dụng PET dẫn đường kể trên? Dù cho khác biệt về định nghĩa bulky, phác đồ hoá trị và vai trò của xạ trị củng cố, các bệnh nhân đạt được CMR tại PET2, được xác nhận trên PET sau khi kết thúc hoá trị (Sau 6 chu kỳ với ABVD hay 4 chu kỳ BEACOPP_leo thang), có kết cục lâm sàng rất tốt mà không cần bổ sung thêm xạ trị củng cố. Nhìn vào chi tiết các dữ liệu y văn, chúng ta chưa thể loại trừ một số trong các bệnh nhân trên vẫn có thể hưởng lợi từ xạ trị củng cố, nhưng các tiêu chuẩn để lựa chọn ra ứng viên tiềm năng cần được thảo luận thêm.
Ở một khía cạnh khác, tăng cường điều trị toàn thân cho các bệnh nhân không đạt CMR tại đánh giá giữa liệu trình có thể làm che mờ giá trị tiên lượng của các tổn thương bulky và để lại câu hỏi chưa được giải đáp về vai trò tiềm năng của xạ trị củng cố trong cải thiện kết cục lâm sàng cho dưới nhóm bệnh nhân này. Một vấn đề cũng chưa rõ ràng nếu bệnh nhân tiếp tục phác đồ ABVD dù đạt đáp ứng không hoàn toàn về chuyển hoá tại PET2, có thể hay không đạt được kết quả thuận lợi với sự bổ sung xạ trị củng cố. Ở thử nghiệm HD0801, trong số 15 bệnh nhân PET2 dương tính hoàn thành 6 chu kỳ ABVD, 11 bệnh nhân (73%) đã đạt CMR sau khi kết thúc liệu trình với 4 trường hợp trong đó (36%) đạt CMR sau xạ trị củng cố. Hơn nữa, một bộ phận nhỏ bệnh nhân (<10%) với PET2 âm tính lại trở thành dương tính tại PET cuối liệu trình (ePET). Không thể chắc chắn rằng những trường hợp này nên được xem là đáp ứng không hoàn toàn, bệnh tiến triển hay phản ứng tăng hấp thụ FDG lành tính. Trong GHSG HD18, một số lượng hạn chế bệnh nhân (31, 3%) có PET2 âm tính nhưng ePET dương tính, đã được xạ trị củng cố đến tổn thương tồn dư >= 2,5 cm sau khi hoàn thành hoá trị BEACOPP_leo thang. Còn trong HD0801, hầu hết bệnh nhân rơi vào tình huống ngày (PET2 âm tính, ePET dương tính), được hoá trị liều cao cứu vãn theo sau bởi ghép tế bào gốc tự thân (ASCT). Thú vị là, chỉ 4 bệnh nhân không nhận thêm hoá trị tăng cường nhưng được xạ trị củng cố. Tất cả đều sống sót và lui bệnh hoàn toàn sau thời gian trung vị 27 tháng. Vì vậy, xạ trị có thể giúp khôi phục lại CMR trong một nhóm nhỏ bệnh nhân có tình trạng tái hoạt động chuyển hoá giữa PET2 và ePET, ít nhất là khi tổn thương tăng hấp thụ giới hạn tại vị trí có thể bao phủ trong một thể tích bia.
Gần đây hơn, các kết quả cuối cùng của thử nghiệm FIL-ROUGE đã được báo cáo tại hội nghị Lugano năm 2023. Các bệnh nhân được phân ngẫu nhiên nhận 6 chu kỳ ABVD tuỳ biến theo đáp ứng trên PET hoặc 6 chu kỳ ABVD tăng cường mà không điều chỉnh theo kết quả PET. Xạ trị củng cố dành cho tổn thương bulky (>= 10 cm) hoặc tồn dư (Điểm Dauville trên 3 và kích thước trên 2,5 cm) ở nhánh tiêu chuẩn, nhưng chỉ thực hiện với tổn thương tồn dư ở nhánh tăng cường. Nghiên cứu thu được điểm cuối chính là cải thiện PFS 3 năm >10% ở nhánh ABVD tăng cường (86,7% so với 73,2%, p = 0,0001). Nghiên cứu này góp phần làm rõ thêm vai trò của xạ trị củng cố trong tương quan với cường độ hoá trị. Ở nhánh ABVD tăng cường, xạ trị với PET dẫn đường cho thấy hiệu quả và chứng minh được tính khả thi của việc bỏ qua xạ trị ở các bệnh nhân có tổn thương bulky nhưng đạt CMR (PFS 3 năm 87% so với 72% ở nhánh ABVD tiêu chuẩn). Một lần nữa, kết quả này tiếp tục khai thác phác đồ hoá trị mạnh mẽ hơn để thay thế xạ trị củng cố. Hơn nữa, chúng ta chưa biết liệu PFS còn có thể thậm chí tốt hơn ở nhánh tăng cường nếu các tổn thương bulky đạt CMR được xạ trị.
Chỉ định của xạ trị – Xu hướng tương lai với sự kết hợp cùng các phác đồ nội khoa mới
Trong tương lai, dự đoán thậm chí sẽ càng phức tạp hơn để có thể xác định vai trò của xạ trị trong u lympho Hodgkin giai đoạn tiến xạ, khi các liệu pháp nội khoa mới được phát triển nhanh chóng. Chiến lược hiện nay để cải thiện tỷ số điều trị là thay thế các tác nhân hoá trị với các thuốc mới có hiệu quả và hồ sơ độc tính ưu việt. Thử nghiệm ECHELON đã cho thấy PFS và cả sống thêm toàn bộ vượt trội ở các bệnh nhân được điều trị bởi phác đồ kết hợp kháng thể liên hợp kháng CD30 Brentuxumab Vedotin (BV) + AVD, so với 6 chu kỳ ABVD. Kết quả SWOG S1826, thử nghiệm ngẫu nhiên pha III, được giới thiệu tại hội nghị Lugano mới đây, ghi nhận thêm một bước tiến nữa về PFS với sự kết hợp thuốc ức chế anti-PD-1 Nivolumab + AVD so với BV-AVD 6 chu kỳ cùng trong 6 chu kỳ (PFS 1 năm 94% so với 86%, p = 0,0005). Tuy nhiên, sử dụng xạ trị củng cố không được dự kiến trong thử nghiệm ECHELON, và <1% bệnh nhân nhận được xạ trị củng cố trong thử nghiệm S1826. Vì vậy, chưa có kết luận cuối cùng về vai trò của xạ trị với các cách tiếp cận trên. Bổ sung thêm các dữ liệu bằng chứng là cần thiết để có thể định nghĩa lại vai trò của xạ trị trong bối cảnh các phác đồ nội khoa mới được.