Cơ sở lý thuyết về hệ số α/β trong xạ trị
Hệ số α/β (alpha/beta) là một tham số quan trọng trong mô hình bình phương – tuyến tính (Linear-Quadratic, LQ) của xạ trị, dùng để biểu thị đặc điểm nhạy cảm nội tại của mỗi loại tổ chức mô hoặc khối u cụ thể đối với xạ trị phân liều. Về định nghĩa, α/β chính là liều (Gy) tại đó hai thành phần gây chết tế bào do bức xạ – thành phần tuyến tính (α) và thành phần bậc hai (β) – đóng góp ngang nhau vào hiệu quả gây chết tế bào. Nói cách khác, α/β phản ánh mức độ quan trọng tương đối giữa tổn thương không thể sửa chữa hay tổn thương gây chết tế bào (do một buổi chiếu xạ riêng lẻ hay 1 phân liều, liên quan đến α) và các tổn thương có thể sửa chữa hay “tổn thương cận tử” được tích lũy (Sau >= 2 phân liều, liên quan đến β) trong quá trình gây chết tế bào do tia xạ.
Về ý nghĩa sinh học, hệ số α/β quyết định mức nhạy cảm với kích thước phân liều (fraction size) của loại tổ chức mô: mô hoặc khối u có α/β thấp nghĩa là thành phần β (Bình phương) chiếm ưu thế hơn, cho phép tế bào có cơ hội sửa chữa nhiều hơn giữa các phân liều; do đó hiệu quả gây chết tế bào phụ thuộc nhiều vào kích thước mỗi phân liều. Ngược lại, α/β cao hàm ý thành phần α (tuyến tính) trội hơn, mô ít nhạy cảm với thay đổi kích thước phân liều.
- α/β thấp (≈1–5 Gy): Thường gặp ở mô lành đáp ứng muộn (ví dụ: tủy sống, não, thận, gan). Những mô này chịu tổn thương nhiều hơn nếu dùng phân liều lớn, nhưng được bảo vệ tốt hơn khi liệu trình xạ được chia thành các phân liều nhỏ nhờ khả năng sửa chữa giữa các lần chiếu xạ. Do vậy, các khối u có α/β thấp được kỳ vọng nhạy cảm hơn với phác đồ xạ trị giảm số phân liều (hypofractionation) dựa trên tăng kích thước mỗi phân liều.
- α/β cao (≈8–10 Gy hoặc hơn): Gặp ở mô đáp ứng sớm và đa số các khối u phát triển nhanh. Những mô/u này ít phụ thuộc vào kích thước phân liều – tức hiệu quả gần như tương đương giữa phân liều nhỏ hay lớn. Thí dụ: da, niêm mạc, tủy xương và nhiều u phân bào nhanh đều có α/β cao. Với chúng, việc chia liều (phân liều chuẩn 1,8–2 Gy/ngày) chủ yếu để bảo vệ mô lành chứ bản thân khối u không được lợi nhiều từ phân liều.
Trong thực hành, giá trị α/β thường được ước tính khoảng 3 Gy cho các mô bình thường đáp ứng muộn và 10 Gy cho các khối u/hệ mô tăng sinh nhanh. Việc lựa chọn phác đồ phân liều dựa trên sự khác biệt α/β giữa mô lành và mô u. Ví dụ, phác đồ phân liều quy ước (1,8 – 2 Gy mỗi ngày) được thiết kế để giảm độc tính muộn cho mô lành (Vì mô lành đáp ứng muộn có α/β thấp ~3 Gy, được lợi khi phân liều nhỏ), trong khi vẫn hiệu quả trên khối u (đa số u α/β ~10 Gy). Ngược lại, với các khối u có α/β thấp bất thường (như ung thư tuyến tiền liệt α/β ≈ 1,5–3 Gy, hoặc một số ung thư vú α/β ~4 Gy), người ta có xu hướng áp dụng phác đồ giảm số phân liều (phân liều lớn hơn 2 Gy) để tận dụng việc khối u nhạy cảm với phân liều kích thước lớn. Công thức liều hiệu quả sinh học (BED) thể hiện một cách định lượng ý nghĩa của α/β trong tính toán:
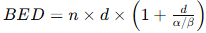
trong đó n là số phân liều và d là kích thước phân liều (Gy). Công thức này cho thấy với cùng tổng liều, nếu d thay đổi thì hiệu quả sinh học sẽ thay đổi tùy theo α/β. Ví dụ, tổng liều 30 Gy chia 15 phân liều (2 Gy/phân liều) sẽ cho BED khác so với 30 Gy chia 5 phân liều (6 Gy/phân liều) – sự chênh lệch đó được điều chỉnh qua giá trị α/β của mô/u cần quan tâm.
Tóm lại, α/β là tham số then chốt để so sánh và thiết kế các phác đồ xạ trị. Trước đây, người ta mặc định đa số khối u ác tính ở người có α/β cao (~10 Gy) như các mô đáp ứng sớm. Tuy nhiên, nhiều dữ liệu đến nay chỉ ra điều này không luôn đúng – điển hình như ung thư tiền liệt tuyến có α/β rất thấp, hoặc ung thư vú cũng thấp hơn dự kiến. Việc xác định α/β cụ thể cho từng loại ung thư giúp tối ưu hóa phân liều, cân bằng giữa kiểm soát u và bảo vệ mô lành.
Phương pháp ước tính hệ số α/β trong nghiên cứu của Suwinski và cộng sự
Nghiên cứu được đề cập (Suwinski et al., 2007) là một phân tích hồi cứu nhằm ước tính α/β của ung thư trực tràng, dựa trên dữ liệu điều trị tiền phẫu với 3 phác đồ phân liều khác nhau. Cụ thể, 168 bệnh nhân ung thư trực tràng giai đoạn tiến triển tại chỗ (T3–4 hoặc N+), không có di căn xa, đã được điều trị xạ trị tiền phẫu trong giai đoạn 1996–2002 theo một trong ba phác đồ:
- Nhóm A (xạ trị liệu trình ngắn): Tổng liều 25 Gy, chia 5 phân liều, mỗi phân liều 5 Gy (trong khoảng 1 tuần).
- Nhóm B (phân liều trung bình): Tổng liều 30 Gy, chia 10 phân liều, mỗi phân 3 Gy (trong 2 tuần).
- Nhóm C (tăng số phân liều, tăng tốc – accelerated hyperfractionation): Tổng liều 42 Gy, chia 28 phân liều, mỗi phân liều 1,5 Gy, 2 phân liều mỗi ngày (cách nhau ≥6 giờ), trong khoảng 2 tuần.
Không có bệnh nhân nào được hóa trị đồng thời; tất cả đều được phẫu thuật sau khi kết thúc xạ trị khoảng ≤1 tuần, nhằm đảm bảo thời gian từ xạ trị đến mổ ngắn và tương đương giữa các nhóm. Ba nhóm bệnh nhân được đánh giá là tương đồng về các đặc điểm lâm sàng cơ bản (tuổi, giới, giai đoạn khối u, v.v.) ngoại trừ khác biệt về phác đồ phân liều, nhờ vậy giảm thiểu sai số do chọn mẫu không ngẫu nhiên.
Phương pháp thống kê:
Các tác giả tiến hành ước tính α/β bằng hai cách tiếp cận:
1. Phân tích dữ liệu “thô” (crude data): Sử dụng trực tiếp số liệu kết quả kiểm soát u tại chỗ – tại vùng (locoregional control) thu được ở các nhóm để hiệu chỉnh tham số mô hình LQ.
- Tại thời điểm phẫu thuật, tỷ lệ khối u được kiểm soát bệnh tại chỗ – tại vùng (không có bằng chứng của ung thư tại vùng chậu) ở nhóm A, B, C lần lượt là 85%, 75,6% và 95,7%. Đáng chú ý, nhóm B có kết quả kém hơn dự kiến so với nhóm A dù nhận tổng liều cao hơn – gợi ý rằng yếu tố phân liều (Kích thước phân liều nhỏ hơn và thời gian điều trị kéo dài hơn) đã có ảnh hưởng bất lợi đến hiệu quả kiểm soát u.
- Để định lượng hiện tượng này, mô hình xác suất kiểm soát u (TCP) dựa trên công thức LQ được áp dụng:
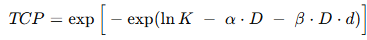
- Mô hình này xuất phát từ giả thuyết Poisson về tiêu diệt các tế bào tạo dòng và đã được hiệu chỉnh để phù hợp tình huống xạ trị tiền phẫu (có xem xét khả năng một tỷ lệ kiểm soát nhất định nhờ phẫu thuật đơn thuần khi D = 0). Các tham số α, β, K được tìm bằng phương pháp Ước lượng hợp lý cực đại (maximum-likelihood) sao cho mô hình khớp tốt nhất với dữ liệu tỷ lệ kiểm soát u của ba phác đồ. Do thời gian điều trị của cả ba nhóm đều khá ngắn (trung vị 6, 14 và 20 ngày lần lượt cho A, B, C) – dưới ngưỡng 3–4 tuần thường được cho là sẽ bắt đầu có hiện tượng tái lập quần thể tế bào mạnh mẽ ở một số loại u – nên ban đầu, mô hình này không đưa tham số thời gian vào. Nói cách khác, giả thiết là hiện tượng tăng sinh của các tế bào ung thư trực tràng trong quá trình xạ trị (repopulation) không đáng kể khi liệu trình xạ <3 tuần. Tuy nhiên, các tác giả vẫn kiểm tra thêm mô hình có yếu tố thời gian: bổ sung một hạng tử γ.T (với T là tổng thời gian xạ trị, γ là hệ số giảm liều hiệu quả do tăng sinh mỗi ngày) vào công thức TCP để đánh giá ảnh hưởng của thời gian điều trị.
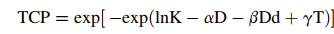
2. Phân tích định lượng thời gian sống (actuarial data): Do không phải tất cả bệnh nhân đều có thời gian theo dõi như nhau, phân tích trên dữ liệu thô có thể chưa phản ánh đầy đủ nguy cơ tái phát theo thời gian. Do đó, nhóm nghiên cứu tiến hành phân tích hồi quy Cox trên thời gian sống thêm không tái phát tại chỗ – tại vùng (locoregional recurrence-free survival) của các bệnh nhân. Trong mô hình Cox đa biến, họ đưa vào hai biến độc lập: tổng liều D và tích số D·d (tương đương với D2 chia cho số phân liều, phản ánh thành phần β). Hệ số hồi quy ước tính ứng với D được coi là tương ứng với –α, và hệ số ứng với D·d tương ứng với –β (dấu âm do liều tăng thì nguy cơ giảm). Từ đó, tỷ số α/β có thể tính bằng tỷ lệ của hai hệ số này. Lưu ý rằng trước khi xây dựng mô hình Cox, các yếu tố lâm sàng khác (tuổi, giới, giai đoạn T, N trước và sau mổ…) đã được kiểm định và không cho thấy ảnh hưởng có ý nghĩa đến kiểm soát u tại chỗ trong quần thể này (p > 0,05). Do vậy, tác giả tập trung mô hình vào ảnh hưởng của liều và phân liều, giả định các yếu tố khác đồng nhất giữa các nhóm.
Tóm lại, nghiên cứu sử dụng mô hình toán LQ kết hợp hồi cứu lâm sàng: dựa vào kết cục kiểm soát khối u của 3 phác đồ phân liều khác nhau, nhà nghiêm cứu tìm hệ số α, β sao cho mô hình LQ khớp với dữ liệu thực tế, và kiểm chứng lại bằng phân tích sống còn để tận dụng toàn bộ dữ liệu theo thời gian.
Kết quả ước tính hệ số α/β cho ung thư trực tràng và ý nghĩa lâm sàng
Kết quả chính của nghiên cứu cho thấy hệ số α/β ước tính cho ung thư trực tràng vào khoảng 5 Gy – tức thuộc mức “thấp trung bình” so với giả thuyết cổ điển về α/β của khối u. Cụ thể, phân tích theo mô hình LQ (dữ liệu thô) tìm được α ≈ 0,339 Gy-1 (SE 0,115) và β ≈ 0,067 Gy-2 (SE 0,027), dẫn đến α/β ≈ 5,06 Gy. Khoảng tin cậy 95% của α/β khá rộng, từ khoảng 0 Gy đến ~10 Gy (do cỡ mẫu và tính không đồng nhất nhất định của dữ liệu). Điều này nghĩa là mặc dù ước tính trung bình ~5 Gy, người ta chưa thể loại trừ hoàn toàn khả năng α/β thực sự cao ~10 Gy. Dù vậy, kết quả định hướng rằng giá trị khả dĩ nằm ở mức trung gian, thấp hơn giả định 10 Gy trước đây.Khi đưa thêm yếu tố thời gian vào mô hình (giả thiết tăng sinh bắt đầu ngay, không có thời gian trễ), bộ tham số ước tính thay đổi nhẹ: α hầu như giữ nguyên (0,335), β giảm còn ~0,03, và xuất hiện tham số γ ≈ 0,15 Gy/ngày. Trong trường hợp này, α/β tính ra xấp xỉ 11,1 Gy. Nói cách khác, nếu ung thư trực tràng có α/β ~11 Gy và tốc độ tăng sinh làm giảm hiệu quả tương đương 0,15 Gy mỗi ngày, thì việc kéo dài phác đồ từ 1 lên 2 tuần (nhóm B so với A) cần tăng tổng liều thêm khoảng 0,15 × 8 ≈ 1,2 Gy để bù đắp. Tuy nhiên, trong phép hiệu chỉnh này tham số γ chỉ đạt ý nghĩa thống kê biên (p = 0,04) và có tương quan cao với kích thước phân liều. Do khoảng thời gian điều trị giữa các nhóm khác nhau không lớn, mô hình bao gồm thời gian dễ bị nhiễu đồng tuyến (collinearity)1 so với mô hình phân liều. Vì vậy, α/β ≈ 5 Gy (bỏ qua thời gian) được cho là kết luận hợp lý hơn từ dữ liệu này. Kết quả phân tích Cox trên số liệu thời gian sống cũng ủng hộ kết luận đó: mô hình Cox cho ước tính α/β ≈ 4,9 Gy (95% CI: ~–0,9 đến 10,7 Gy) – rất gần với con số 5 Gy nói trên. Như vậy, cả hai cách phân tích đều nhất quán về một hệ số α/β “thấp trung bình” cho ung thư trực tràng trong bối cảnh xạ trị tiền phẫu.
Diễn giải kết quả: Giá trị α/β ~5 Gy đối với ung thư trực tràng là điều đáng chú ý, vì lâu nay nhiều nhà lâm sàng vẫn giả định các khối u trực tràng (gồm cả biểu mô tuyến) có đáp ứng kiểu “sớm” với α/β ~10 Gy như các ung thư khác. Kết quả này gợi ý rằng khối u trực tràng có thể nhạy cảm với kích thước phân liều – tức có một phần tính chất của mô đáp ứng muộn. Hệ quả lâm sàng trực tiếp là: kích thước phân liều ảnh hưởng nhiều đến hiệu quả kiểm soát u. Thật vậy, dữ liệu nghiên cứu cho thấy phác đồ B (nhiều phân liều hơn, kích thước phân liều nhỏ hơn) cho kiểm soát u kém hơn phác đồ A (ít phân liều hơn, kích thước phân liều lớn hơn) mặc dù tổng liều cao hơn 5 Gy. Nếu α/β thực sự ~10 Gy và tốc độ tăng sinh nhanh, đáng lẽ thêm 5 Gy ở nhóm B phải bù đắp đủ tác động bất lợi của kéo dài 8 ngày điều trị (theo ước tính trước đây, ~0,54 Gy/ngày cho α/β = 10 Gy). Nhưng trái lại, nhóm B vẫn kém hiệu quả, ám chỉ rằng khối u nhạy cảm với việc giảm kích thước phân liều hơn dự tính – phù hợp với α/β thấp hơn (≈5 Gy). Ngược lại, nhóm C (42 Gy phân liều nhỏ 1,5 Gy, 2 phân liều/ngày) đạt kiểm soát u cao nhất có thể một phần do tổng liều vượt trội, nhưng cũng đặt ra câu hỏi về vai trò của tăng tốc liệu trình xạ trị. Tác giả lưu ý rằng hiệu quả cao của nhóm C một phần có thể do tăng tốc (thời gian điều trị ngắn ~2 tuần với liều cao) và cũng có thể do các tế bào u chưa kịp phục hồi hoàn toàn giữa hai lần chiếu mỗi ngày (khoảng cách 6 giờ có thể chưa đủ cho mô u sửa chữa hết tổn thương) – yếu tố này chưa được đưa vào mô hình và nếu tính đến có thể làm tăng ước tính hiệu quả sinh học thực sự của phác đồ C. Dù vậy, nhìn tổng thể thì xu hướng kết quả phù hợp giả thuyết α/β thấp: phác đồ phân liều lớn hơn/ngắn hơn (A, C) cho hiệu quả tốt hơn mong đợi so với phác đồ phân liều nhỏ hơn/kéo dài (B). Kết quả này còn được ủng hộ gián tiếp bởi một nghiên cứu trên mô hình chuột: khi so sánh các phác đồ tiền phẫu tương tự, người ta cũng thấy 30 Gy/10 phân liều ≤3 Gy kém hiệu quả hơn 25 Gy/5 Gy và phác đồ tăng tốc liều cao cho kết quả tốt nhất – gợi ý bản chất sinh học của ung thư trực tràng có độ nhạy phân liều tương đối cao.
Độ tin cậy và hạn chế: Mặc dù gợi mở, các phát hiện trên cần được diễn giải thận trọng. Nhóm tác giả nhấn mạnh rằng vì đây là nghiên cứu hồi cứu, không có chọn nhóm ngẫu nhiên cho các phác đồ, và chất lượng phẫu thuật không được kiểm soát đồng nhất, nên kết quả chỉ mang tính giả thuyết để định hướng nghiên cứu tiếp theo. Một số điểm cần lưu ý:
- Các nhóm phân liều không ngẫu nhiên có thể dẫn đến thiên lệch chọn bệnh nhân: ví dụ, một số bệnh nhân trẻ, gần bệnh viện hơn có thể được chọn phác đồ C (tăng tốc) so với bệnh nhân xa được chọn phác đồ A/B. Dù đặc điểm cơ bản giữa nhóm nhìn chung cân bằng, không loại trừ khả năng những khác biệt ẩn số (ví dụ kích thước u, nguy cơ vi thể) ảnh hưởng kết quả.
- Chất lượng phẫu thuật và chăm sóc sau mổ khác nhau: Đây là yếu tố quan trọng ảnh hưởng kiểm soát tại chỗ ung thư trực tràng. Trong nghiên cứu, do thực hiện qua nhiều năm và không thuộc một thử nghiệm duy nhất, khó đảm bảo mọi bệnh nhân đều được phẫu thuật bởi cùng một kỹ thuật viên hay tuân thủ chặt chẽ kỹ thuật phẫu thuật chuẩn hóa. Sự khác biệt này có thể tác động đến tỷ lệ tái phát, độc lập với phân liều xạ trị.
- Một tỷ lệ bệnh nhân có thể đã nhận hóa trị bổ trợ sau mổ, phân bố không hoàn toàn ngẫu nhiên giữa các nhóm, cũng có thể ảnh hưởng đến kiểm soát bệnh về lâu dài.
- Cỡ mẫu giới hạn và khoảng tin cậy rộng: 168 bệnh nhân chia 3 nhóm là tương đối nhỏ để xác định chính xác α/β. Như thấy, khoảng tin cậy 95% của α/β rất rộng (từ ~0 đến >10 Gy), do đó kết quả trung bình ~5 Gy cần được xác nhận trên quần thể lớn hơn.
- Thiếu nhóm chứng phẫu thuật đơn thuần: Nghiên cứu không có nhóm bệnh nhân chỉ phẫu thuật (0 Gy) để trực tiếp xác định tỷ lệ kiểm soát tự nhiên. Tác giả phải ước lượng gián tiếp tham số K (liên quan đến tỷ lệ kiểm soát với phẫu thuật) dựa trên dữ liệu ngoại suy. Điều này không ảnh hưởng đến tính toán α/β (vì α, β chủ yếu dựa trên so sánh các nhóm xạ trị khác nhau), nhưng làm tăng bất định của tham số K.
Nhìn chung, các hạn chế trên khiến kết luận về α/β cho ung thư trực tràng từ nghiên cứu này chưa thể xem là chắc chắn, nhưng phù hợp về mặt sinh học và có giá trị định hướng.
Ứng dụng lâm sàng: Nếu giả thuyết α/β ~5 Gy cho ung thư trực tràng được khẳng định, điều này tác động đến cách thiết kế phác đồ xạ trị tiền phẫu. Một α/β ở mức trung gian ngụ ý khối u trực tràng không “miễn nhiễm” với thay đổi phân liều như các u α/β cao, do đó việc rút ngắn thời gian điều trị hoặc tăng kích thước phân liều có thể cải thiện đáp ứng tại khối u. Thực tế lâm sàng đã phần nào phản ánh điều này: phác đồ ngắn 5×5 Gy trong 1 tuần hiện được sử dụng rộng rãi cho xạ trị tiền phẫu ung thư trực tràng và cho kết quả tương đương phác đồ dài ngày 25×1,8–2 Gy trong 5 tuần (khi kết hợp hóa trị) về kiểm soát tại chỗ, mặc dù thời gian theo dõi khác biệt. Phân tích của Suwinski et al. góp phần lý giải tại sao phác đồ 5×5 Gy không thua kém phác đồ dài hơn về hiệu quả kiểm soát u. Ngoài ra, kết quả gợi ý rằng trong trường hợp cần kéo dài thời gian điều trị, ta nên tăng tổng liều nhiều hơn so với ước tính dựa trên α/β cao trước đây. Ví dụ, nếu điều trị kéo dài thêm 1 tuần, có lẽ cần tăng liều nhiều hơn mức 0,5 Gy/ngày (theo giả thuyết α/β=10 Gy) – có thể khoảng 0,3 Gy/ngày nếu α/β ~5 Gy – để bù đắp cho sự phân bào của u. Mặt khác, do α/β của mô lành vùng chậu (ruột, tủy sống) ~3 Gy, phác đồ 5×5 Gy tuy thuận lợi cho khối u nhưng nguy cơ biến chứng muộn cao hơn so với phác đồ chuẩn 25×2 Gy. Do đó, các quyết định lâm sàng vẫn phải cân nhắc đánh đổi giữa kiểm soát u và an toàn mô lành, nhất là khi khác biệt α/β giữa u và mô lành không quá lớn.
Tóm lại, nghiên cứu của Suwinski và cộng sự đã đề xuất ung thư trực tràng có hệ số α/β thấp hơn dự kiến (~5 Gy), giúp giải thích kết quả của các phác đồ phân liều tiền phẫu khác nhau. Dù có những giới hạn và chưa thay đổi trực tiếp thực hành, kết quả này mang ý nghĩa gợi mở quan trọng. Nó khuyến khích các thử nghiệm lâm sàng và nghiên cứu tiếp theo để xác định chính xác hơn thông số α/β cho ung thư trực tràng, từ đó tối ưu hóa phác đồ xạ trị (ví dụ: lựa chọn giữa xạ trị ngắn ngày hay dài ngày, xác định liều bổ sung khi kéo dài điều trị, v.v.). Nếu được khẳng định, việc hiệu chỉnh chiến lược phân liều dựa trên α/β đặc thù của từng loại u sẽ góp phần nâng cao hiệu quả điều trị đồng thời giảm thiểu độc tính cho bệnh nhân ung thư trực tràng.
Nguồn tài liệu tham khảo: Nghiên cứu của Suwinski et al. (Int J Radiat Oncol Biol Phys, 2007) và các tài liệu về mô hình tuyến tính – bậc hai trong xạ trị.
- Nhiễu đồng tuyến (Collinearity): là một hiện tượng khi hai hoặc nhiều biến độc lập trong mô hình có mối tương quan chặt chẽ với nhau. Điều này khiến mô hình khó xác định chính xác ảnh hưởng riêng rẽ của từng biến lên kết quả, vì mô hình “không biết chọn biến nào” để gán tác động. ↩︎

