1. Giới thiệu
Việc mắc ung thư trong thời kỳ mang thai là một tình huống hiếm gặp, ước tính cứ 1.000 trường hợp mang thai thì có 1 ca mắc bệnh.
Tuy nhiên, số lượng các trường hợp ung thư gây biến chứng cho thai kỳ có thể gia tăng trong những năm tiếp theo, đặc biệt là do độ tuổi từ lần mang thai đầu tăng lên. Các loại ung thư phổ biến nhất được chẩn đoán trong suốt thời gian mang thai là ung thư vú (UTV), ung thư cổ tử cung, lymphoma, ung thư buồng trứng, bệnh bạch cầu, ung thư đại trực tràng và melanoma.
Chẩn đoán UTV trong thời kỳ mang thai là một thách thức đối với bệnh nhân (BN), người chăm sóc và bác sĩ, vì lợi ích của việc điều trị cho bà mẹ phải cân bằng tác hại tiềm ẩn đối với thai nhi. Đáng chú ý, tình huống phức tạp này cần được quản lý bởi một nhóm chuyên gia đa ngành và tiếp cận điều trị được đề xuất cần được thảo luận với bệnh nhân và gia đình cô ấy, có tính đến tiên lượng ung thư, tuổi thai và các rủi ro có thể xảy ra cho thai nhi.
Xem xét độ tuổi trẻ của BN UTV trong thời kỳ mang thai, nên cung cấp tư vấn di truyền phù hợp.
2. Ung thư vú trong thai kỳ: Tiên lượng và sinh học
UTV trong thai kỳ đã được chứng minh là có liên quan đến tỉ lệ biểu hiện thụ thể nội tiết thấp hơn, do đó sự chiếm ưu thế của các phân nhóm “hung hãn” hơn đặc trưng cho lứa tuổi trẻ, chẳng hạn như tam âm hoặc HER-2 dương tính. Chẩn đoán xảy ra thường xuyên ở giai đoạn tiến xa hơn so với BN không mang thai, có khả năng góp phần xác định tiên lượng xấu hơn. Điều này có thể liên quan đến sự chậm trễ trong chẩn đoán, đến việc xếp giai đoạn không tối ưu do tính gây quái thai của hầu hết các quy trình điện quang hình ảnh học và đến nguy cơ quản lý không tối ưu. Một số nghiên cứu về vấn đề này, với kết quả trái ngược nhau, có thể là do quy mô mẫu nhỏ. Một nghiên cứu hồi cứu được tiến hành trên một đoàn hệ 75 phụ nữ mang thai bị UTV được điều trị trong tam cá nguyệt thứ hai và thứ ba bằng 5-fluorouracil, doxorubicin, và cyclophosphamide, so sánh với một đoàn hệ bệnh nhân không mang thai phù hợp về độ tuổi, giai đoạn bệnh và năm được chẩn đoán, cho thấy sự cải thiện đáng kể về mặt sống còn không bệnh (DFS – Disease-free survival) và sống còn toàn bộ (OS – Overall survival) đối với BN mang thai [1]. Một nghiên cứu đoàn hệ khác bao gồm 311 BN được chẩn đoán mắc UTV trong thai kỳ (trong đó phần lớn được điều trị chống ung thư toàn thân) và 865 phụ nữ được chẩn đoán UTV ngoài thai kỳ không tìm thấy tác động bất lợi của thai kỳ đối với cả DFS và OS, sau khi điều chỉnh cho các đặc điểm BN, khối u, và điều trị [2]. Kết quả của những nghiên cứu này ủng hộ quan điểm cho rằng chẩn đoán UTV trong thời kỳ mang thai không liên quan đến kết quả tồi tệ hơn, nếu BN được điều trị tại chỗ và toàn thân tiêu chuẩn.
Để hiểu rõ hơn về mặt sinh học của UTV trong thai kỳ, Nguyen và các đồng nghiệp đã đặt mục tiêu xác định những thay đổi phân tử cụ thể ở các BN này, so với những phụ nữ không mang thai. Một hồ sơ thay đổi số lượng bản sao trên toàn bộ hệ gen ở các mẫu bệnh phẩm khối u nguyên phát cho thấy không có sự khác biệt giữa bệnh nhân và nhóm đối chứng [3]. Tuy nhiên, một phân tích giải trình tự toàn bộ bộ gen cho thấy UTV liên quan đến thai kỳ có số lượng đột biến không im lặng, đột biến trong họ gen mucin và sự gia tăng dấu hiệu đột biến thiếu hụt sửa chữa bắt cặp sai và nồng độ tế bào lymphô xâm nhập khối u (tumor-infiltrating lymphocyte – TILs), cho thấy tác động tiềm năng của thai kỳ đối với sinh học khối u [3], [4].
Một đánh giá có hệ thống gần đây đã tóm tắt các bằng chứng có sẵn về hồ sơ bộ gen của UTV liên quan đến thai kỳ, chứng minh sự biểu hiện bất thường của một vài oncogen (ví dụ MYC, SRC, FOS), gen ức chế khối u (ví dụ TP53, PTEN, CAV1), điều hòa chết tế bào theo lập trình (ví dụ PDCD4, BLC2, BIRC5), điều hòa phiên mã (ví dụ JUN, KLF1, SP110), gen liên quan đến cơ chế sửa chữa DNA (ví dụ Sig20, BRCA1/2, FEN1), trong quá trình tăng sinh tế bào (ví dụ AURKA, MKI67) và trong đáp ứng miễn dịch (ví dụ PD1, PDL1) [5].
Cần có thêm nghiên cứu trong lĩnh vực này để làm sáng tỏ các đặc điểm sinh học đặc biệt của UTV trong suốt thời kỳ mang thai.
3. Điều trị kháng ung thư trong thai kỳ
Các hướng dẫn khuyến cáo rằng UTV trong thai kỳ nên được điều trị theo các khuyến cáo tương tự như bệnh ác tính vú ở phụ nữ trẻ không mang thai. Đặc điểm lâm sàng và bệnh lý, tuổi thai khi chẩn đoán UTV, ngày dự sinh và sở thích của BN là những yếu tố chủ yếu cần được xem xét để có phương pháp quản lý tối ưu. Cách tiếp cận đa ngành là bắt buộc để có được kết quả tốt nhất có thể cho bà mẹ và đứa trẻ trong tương lai.
3.1. Liệu pháp tại chỗ
Phẫu thuật UTV được coi là an toàn trong suốt thai kỳ và nên tuân theo các khuyến cáo tương tự như đối với phụ nữ không mang thai nếu có thể. Mặc dù chẩn đoán chậm trễ thường có liên quan đến kích thước khối u vú lớn hơn, phẫu thuật triệt để không nên là lựa chọn được ưu tiên. Vì xạ trị phải được trì hoãn sau khi sinh nên loại phẫu thuật vú chủ yếu bị ảnh hưởng bởi thời gian dự kiến bắt đầu xạ trị và nên được thảo luận trong một nhóm đa ngành. Bệnh nhân được chẩn đoán trong tam cá nguyệt đầu tiên, không phải là ứng viên để được hóa trị và mong muốn thực hiện phẫu thuật bảo tồn vú và tiếp tục mang thai, phải được thông báo rằng trì hoãn quá lâu trong việc bắt đầu xạ trị hỗ trợ có thể dẫn đến gia tăng nguy cơ tái phát tại chỗ. Mặc dù các nghiên cứu lớn chưa được tiến hành nhưng tỉ lệ sống còn tương tự đã được quan sát thấy ở những phụ nữ đã trải qua phẫu thuật bảo tồn vú hoặc phẫu thuật triệt căn. Lưu ý, phần lớn thuốc gây mê có thể được sử dụng an toàn trong thời kỳ mang thai. Có thể thực hiện tái tạo vú ngay lập tức bằng cách sử dụng túi giãn mô sau khi đoạn nhũ mà không làm tăng nguy cơ cho bệnh nhân hoặc thai nhi. Tuy nhiên, cần phải tính đến những thay đổi sinh lý của vú ở phụ nữ mang thai và có thể cân nhắc đến việc trì hoãn quá trình tái tạo sau khi sinh [6].
Sinh thiết hạch lính gác ở bệnh nhân mang thai là một chủ đề gây tranh cãi. Các khuyến cáo từ ASCO không ủng hộ quy trình này, trong khi các hướng dẫn của NCCN xác nhận cách tiếp cận này dựa trên một vài nghiên cứu đã cho thấy quy trình này có thể được thực hiện an toàn [7], [8]. Nếu bệnh nhân mang thai được đề nghị sinh thiết hạch cửa, tiêm dung dịch keo Technetium-99m (99mTc) nên là lựa chọn ưu tiên. Để giảm thiểu tiếp xúc với bức xạ, nên áp dụng phác đồ một ngày, tiêm dung dịch keo vào buổi sáng của ngày phẫu thuật [9]. Thuốc nhuộm xanh và xanh isosulfan nên tránh vì nguy cơ gây ra phản ứng dị ứng hoặc phản vệ và xanh methylene chống chỉ định trong tam cá nguyệt đầu tiên vì tác dụng gây quái thai đã biết [10].
Một nghiên cứu theo dõi quốc tế bao gồm 145 phụ nữ bị UTV trong thai kỳ đã báo cáo tỉ lệ phát hiện cao và tỉ lệ tái phát ở nách thấp với sinh thiết hạch lính gác [11]. Do đó, cách tiếp cận này có thể được coi là an toàn ở những bệnh nhân mang thai không có di căn hạch trên lâm sàng khi sử dụng keo phóng xạ và phác đồ một ngày [9].
3.2. Hóa trị
Việc hóa trị cho phụ nữ trong thời kỳ mang thai nên được thực hiện theo các hướng dẫn dành cho BN không mang thai một cách chặt chẽ nhất có thể [9], . Rủi ro đối với thai nhi thay đổi tùy theo tuổi thai; do đó, chỉ định hóa trị trong bối cảnh này phụ thuộc rất nhiều vào thời điểm chẩn đoán UTV [12].
Trước khi bắt đầu bất kỳ phương pháp điều trị ung thư nào, cần phải tiến hành siêu âm để kiểm tra thai nhi nhằm loại trừ các bất thường đã có từ trước.
Trong tam cá nguyệt đầu tiên, việc tiếp xúc với các tác nhân gây độc tế bào có thể ảnh hưởng đến quá trình hình thành cơ quan của thai nhi, dẫn đến tăng nguy cơ sẩy thai và dị tật bẩm sinh ở khoảng 14% trường hợp. Do đó, hóa trị chống chỉ định trong tam cá nguyệt đầu tiên [9], [13], [14], [15]. Nếu có nhu cầu cấp thiết phải bắt đầu hóa trị trong khoảng thời gian này thì phương án chấm dứt thai kỳ để tránh sự chậm trễ để khởi trị nên được thảo luận một cách cẩn thận với bệnh nhân.
Sau tam cá nguyệt đầu tiên, tỉ lệ dị tật thai nhi do phác đồ hóa trị giảm xuống còn 3%, tương tự như những gì quan sát thấy ở dân số chung. Do đó, hóa trị có thể được thực hiện an toàn trong tam cá nguyệt thứ hai và thứ ba, luôn luôn có sự giám sát chặt chẽ đối với mẹ và thai nhi [9], [12]. Hàng rào nhau thai hạn chế sự tiếp xúc của thai nhi với thuốc gây độc tế bào, với khả năng xuyên quan nhau thai khác nhau đối với các loại thuốc khác nhau [16], [17].
Hiện nay, các phác đồ dựa trên anthracycline, cyclophosphamide và taxane đại diện cho tiêu chuẩn chăm sóc của điều trị (tân) hỗ trợ cho BN UTV. Hợp chất platinum có thể có vai trò trong điều trị tân hỗ trợ cho BN UTV tam âm [18], [19], [20], [21].
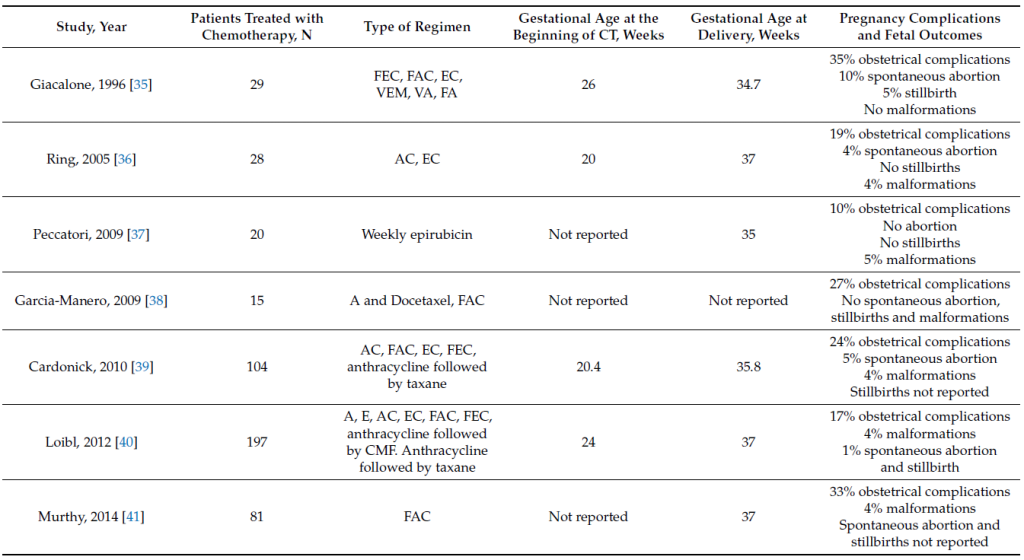
Bảng 1 tóm tắt các kết quả chính về việc sử dung anthracycline và taxane trong thai kỳ về các biến chứng khi mang thai và kết quả của thai nhi [22]. Anthracycline và các tác nhân alkyl hóa như cyclophosphamide đã được biết là an toàn cho phụ nữ mang thai trong nhiều năm; gần đây, bằng chứng đáng tin cậy hơn về tính an toàn khi sử dụng taxane trong thai kỳ đã xuất hiện (xem Bảng 1). Tác dụng độc hại tiềm ẩn đối với thai nhi của các dẫn xuất platinum là rất hiếm do chúng ít có liên quan đến phác đồ điều trị tiêu chuẩn cho UTV. Một nghiên cứu đã báo cáo rằng hóa trị dựa trên platinum có liên quan đến kích thước thai nhỏ hơn so với tuổi thai [23]. Nhìn chung, các phác đồ có chứa anthracycline và taxane có vẻ an toàn trong tam cá nguyệt thứ hai và thứ ba của thai kỳ [24].
Việc sử dụng hóa trị liều dày (bằng cách giảm khoảng cách giữa các chu kỳ điều trị và tăng liều dùng) đã được coi là tiêu chuẩn chăm sóc để điều trị cho BN UTV có nguy cơ cao [25], [26]. Một phân tích gộp được tiến hành cụ thể ở những BN tiền mãn kinh cho thấy sự cải thiện đáng kể về DFS và OS khi sử dụng hóa trị liều dày trong bối cảnh này [27]. Mặc dù liều dày là lựa chọn ưu tiên cho BN tiền mãn kinh có nguy cơ tái phát cao, nhưng có rất ít dữ liệu về việc sử dụng phác đồ này ở BN UTV trong thời kỳ mang thai. Một nghiên cứu đoàn hệ hồi cứu được tiến hành trên 109 phụ nữ mang thai bị UTV, trong số đó có 10 người được điều trị hóa trị liều dày, đã cho thấy tính an toàn của cách tiếp cận này [28]. Tuy nhiên, kích thước mẫu nhỏ hạn chế khả năng tư vấn cho BN về tính an toàn của hóa trị liều dày trong thai kỳ.
Giống như ở phụ nữ không mang thai, liều lượng hóa trị nên dựa trên diện tích bề mặt cơ thể hiện tại [9], [10], [12]. Những thay đổi sinh lý xảy ra trong thai kỳ (ví dụ, tăng thể tích huyết thanh, tăng tốc độ lộc cầu thận, thay đổi nồng độ albumin) có thể dẫn đến nồng độ tối đa thấp hơn và giảm tiếp xúc với hóa trị [29], [30]. Do đó, nên tránh dùng liều thấp hơn cho phụ nữ mang thai. Mặt khác, liệu có cần tăng liều hóa trị vẫn chưa chắc chắn, vì dùng quá liều có thể gây độc cho thai nhi.
Sau tuần thứ 35 của thai kỳ, nên ngừng hóa trị để có khoảng thời gian 2/3 tuần trước khi sinh nhằm ngăn ngừa các biến chứng về huyết học trong quá trình sinh [29], [31].

3.3. Liệu pháp nội tiết
Liệu pháp nội tiết chống chỉ định trong điều trị UTV thai kỳ. Trong các mô hình động vật, tamoxifen gây ra các tác dụng quái thai, liên quan nhiều hơn đến đường tiết niệt sinh dục và làm tăng nguy cơ phát triển UTV ở con cái [32], [33]. Một đánh giá có hệ thống tóm tắt dữ liệu của 248 trường hợp mang thai ở BN UTV tiếp xúc với tamoxifen trong suốt thai kỳ [34]. Trong số 68 thai kỳ đủ tháng, 12 trẻ (18%) sinh ra với dị tật lớn (bao gồm cơ quan sinh dục không rõ ràng, hội chứng Pierre Robin và loạn sản mắt – tai – cột sống), 2 trẻ (3%) bị dị tật nhẹ (mụn thịt trước tai và viễn thị nặng) và 54 trẻ (79%) không có bất kỳ dị tật nào. Tỉ lệ dị tật lớn sau khi tiếp xúc với tamoxifen là 17,6% trong khi ở nhóm dân số không tiếp xúc nói chung, tỉ lệ này là khoảng 3%; tuy nhiên, một số trẻ sơ sinh bị dị tật lớn cũng tiếp xúc với nhiều tác nhân gây quái thai (ví dụ, các thuốc chống ung thư khác, X-quang và các loại thuốc có khả năng gây quái thai khác). Cuối cùng, tamoxifen gây ra sự thay đổi tế bào tương tự như diethylstilbestrol, có liên quan đến các biến cố bất lợi dài hạn trở nên rõ ràng hơn sau này trong cuộc sống; do đó tác động của việc tiếp xúc với tamoxifen có thể không chỉ giới hạn ở các di tật lớn được quan sát thấy khi sinh [35]. Do không có dữ liệu về kết quả nhi khoa dài hạn, tỉ lệ dị tật lớn ở động vật và thai kỳ của người tăng lên và một số yếu tố gây nhiễu trong dữ liệu hiện có, nên không thể đưa ra kết luận chắc chắn về tác động gây quái thai của việc tiếp xúc với tamoxifen. Các hướng dẫn quốc tế chống chỉ định sử dụng tamoxifen trong thời kỳ mang thai và trong trường hợp vô tình tiếp xúc, nên ngừng dùng thuốc ngay lập tức nếu BN muốn tiếp tục mang thai [12]. Ở những BN muốn thụ thai, nên để đào thài thuốc trong thời gian 3 tháng sau khi ngừng tamoxifen [36]. Không có dữ liệu nào về việc tiếp xúc với chất ức chế aromatase trong thai kỳ, mặc dù khả năng gây quái thai của chúng đã được nghiên cứu trên mô hình động vật [37].
TÀI LIỆU THAM KHẢO
[1]. Litton, J.K.; Warneke, C.L.; Hahn, K.M.; Palla, S.L.; Kuerer, H.M.; Perkins, G.H.; Mittendorf, E.A.; Barnett, C.;
Gonzalez-Angulo, A.M.; Hortobágyi, G.N.; et al. Case control study of women treated with chemotherapy
for breast cancer during pregnancy as compared with nonpregnant patients with breast cancer. Oncologist
2013, 18, 369–376.
[2]. Amant, F.; von Minckwitz, G.; Han, S.N.; Bontenbal, M.; Ring, A.E.; Giermek, J.; Wildiers, H.; Fehm, T.;
Linn, S.C.; Schlehe, B.; et al. Prognosis of Women With Primary Breast Cancer Diagnosed During Pregnancy:
Results From an International Collaborative Study. JCO J. Clin. Oncol. 2013, 31, 2532–2539.
[3]. Nguyen, B.; Venet, D.; Azim, H.A.; Brown, D.; Desmedt, C.; Lambertini, M.; Majjaj, S.; Pruneri, G.; Peccatori, F.; Piccart, M.; et al. Breast cancer diagnosed during pregnancy is associated with enrichment of non-silent mutations, mismatch repair deficiency signature and mucin mutations. NPJ Breast Cancer 2018, 4, 23.
[4]. Nguyen, B.; Venet, D.; Lambertini, M.; Desmedt, C.; Salgado, R.; Horlings, H.M.; Rothé, F.; Sotiriou, C. Imprint of parity and age at first pregnancy on the genomic landscape of subsequent breast cancer. Breast Cancer Res. 2019, 21, 25.
[5]. Korakiti, A.-M.; Moutafi, M.; Zografos, E.; Dimopoulos, M.-A.; Zagouri, F. The Genomic Profile of Pregnancy-Associated Breast Cancer: A Systematic Review. Front. Oncol. 2020, 10, 1773.
[6]. Toesca, A.; Gentilini, O.; Peccatori, F.; Azim, H.A.; Amant, F. Locoregional treatment of breast cancer during pregnancy. Gynecol. Surg. 2014, 11, 279–284.
[7]. Lyman, G.H.; Somerfield, M.R.; Bosserman, L.D.; Perkins, C.L.; Weaver, D.L.; Giuliano, A.E. Sentinel Lymph Node Biopsy for Patients with Early-Stage Breast Cancer: American Society of Clinical Oncology Clinical Practice Guideline Update. J. Clin. Oncol. 2017, 35, 561–564.
[8]. NCCN Clinical Practice Guidelines in Oncology, Breast Cancer—Version 6.2020.
[9]. Loibl, S.; Schmidt, A.; Gentilini, O.; Kaufman, B.; Kuhl, C.; Denkert, C.; von Minckwitz, G.; Parokonnaya, A.; Stensheim, H.; Thomssen, C.; et al. Breast Cancer Diagnosed During Pregnancy: Adapting Recent Advances in Breast Cancer Care for Pregnant Patients. JAMA Oncol. 2015, 1, 1145.
[10]. Amant, F.; Loibl, S.; Neven, P.; Van Calsteren, K. Breast cancer in pregnancy. Lancet 2012, 379, 570–579.
[11]. On Behalf of the International Network on Cancer, Infertility and Pregnancy; Han, S.N.; Amant, F.;
Cardonick, E.H.; Loibl, S.; Peccatori, F.A.; Gheysens, O.; Sangalli, C.A.; Nekljudova, V.; Steensen, K.D.; et al.
Axillary staging for breast cancer during pregnancy: Feasibility and safety of sentinel lymph node biopsy.
Breast Cancer Res. Treat. 2018, 168, 551–557.
[12]. Peccatori, F.A.; Azim, H.A.; Orecchia, R.; Hoekstra, H.J.; Pavlidis, N.; Kesic, V.; Pentheroudakis, G. Cancer, pregnancy and fertility: ESMOClinical Practice Guidelines for diagnosis, treatment and follow-up. Ann. Oncol. 2013, 24, vi160–vi170.
[13]. Leslie, K.K.; Koil, C.; Rayburn,W.F. Chemotherapeutic Drugs in Pregnancy. Obstet. Gynecol. Clin. N. Am.
2005, 32, 627–640.
[14]. Cardonick, E.; Iacobucci, A. Use of chemotherapy during human pregnancy. Lancet Oncol. 2004, 5, 283–291.
[15]. National Toxicology Program NTP Monograph. Developmental Eects and Pregnancy Outcomes Associated
With Cancer Chemotherapy Use During Pregnancy. NTP Monogr. 2013, 2, i-214.
[16]. Van Calsteren, K.; Verbesselt, R.; Beijnen, J.; Devlieger, R.; De Catte, L.; Chai, D.C.; Van Bree, R.; Heyns, L.; de Hoon, J.; Amant, F. Transplacental transfer of anthracyclines, vinblastine, and 4-hydroxycyclophosphamide in a baboon model. Gynecol. Oncol. 2010, 119, 594–600.
[17]. Bar-Joseph, H.; Peccatori, F.A.; Goshen-Lago, T.; Cribiù, F.M.; Scarfone, G.; Miller, I.; Nemerovsky, L.; Levi, M.; Shalgi, R.; Ben-Aharon, I. Cancer During Pregnancy: The Role of Vascular Toxicity in Chemotherapy-Induced Placental Toxicity. Cancers 2020, 12, 1277.
[18]. Paluch-Shimon, S.; Cardoso, F.; Partridge, A.H.; Abulkhair, O.; Azim, H.A.; Bianchi-Micheli, G.; Cardoso, M.-J.; Curigliano, G.; Gelmon, K.A.; Harbeck, N.; et al. ESO–ESMO 4th International Consensus Guidelines for Breast Cancer in YoungWomen (BCY4). Ann. Oncol. 2020, 31, 674–696.
[19]. Cardoso, F.; Kyriakides, S.; Ohno, S.; Penault-Llorca, F.; Poortmans, P.; Rubio, I.T.; Zackrisson, S.; Senkus, E.; ESMO Guidelines Committee. Early breast cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann. Oncol. 2019, 30, 1194–1220.
[20]. Denduluri, N.; Chavez-MacGregor, M.; Telli, M.L.; Eisen, A.; Gra, S.L.; Hassett, M.J.; Holloway, J.N.;
Hurria, A.; King, T.A.; Lyman, G.H.; et al. Selection of Optimal Adjuvant Chemotherapy and Targeted
Therapy for Early Breast Cancer: ASCO Clinical Practice Guideline Focused Update. JCO J. Clin. Oncol.
2018, 36, 2433–2443.
[21]. Poggio, F.; Bruzzone, M.; Ceppi, M.; Pondé, N.F.; La Valle, G.; Del Mastro, L.; de Azambuja, E.; Lambertini, M. Platinum-based neoadjuvant chemotherapy in triple-negative breast cancer: A systematic review and meta-analysis. Ann. Oncol. 2018, 29, 1497–1508.
[22]. Poggio, F.; Tagliamento, M.; Pirrone, C.; et al. Update on the management of breast cancer during pregnancy. Cancers. 2020, 12, 3616.
[23]. De Haan, J.; Verheecke,M.; Van Calsteren, K.; Van Calster, B.; Shmakov, R.G.; Mhallem Gziri, M.; Halaska, M.J.; Fruscio, R.; Lok, C.A.R.; Boere, I.A.; et al. Oncological management and obstetric and neonatal outcomes for women diagnosed with cancer during pregnancy: A 20-year international cohort study of 1170 patients. Lancet Oncol. 2018, 19, 337–346.
[24]. Tehrani, O.S. Systemic Treatments in Pregnancy-Associated Breast Cancer. In Diseases of the Breast
during Pregnancy and Lactation; Alipour, S., Omranipour, R., Eds.; Advances in Experimental Medicine
and Biology; Springer International Publishing: Cham, Switzerland, 2020; Volume 1252, pp. 115–124,
ISBN 978-3-030-41595-2.
[25]. Del Mastro, L.; De Placido, S.; Bruzzi, P.; De Laurentiis, M.; Boni, C.; Cavazzini, G.; Durando, A.; Turletti, A.; Nisticò, C.; Valle, E.; et al. Fluorouracil and dose-dense chemotherapy in adjuvant treatment of patients with early-stage breast cancer: An open-label, 2 2 factorial, randomised phase 3 trial. Lancet 2015, 385, 1863–1872.
[26]. Gray, R.; Bradley, R.; Braybrooke, J.; Liu, Z.; Peto, R.; Davies, L.; Dodwell, D.; McGale, P.; Pan, H.; Taylor, C.; et al. Increasing the dose intensity of chemotherapy by more frequent administration or sequential scheduling: A patient-level meta-analysis of 37 298 women with early breast cancer in 26 randomised trials. Lancet 2019, 393, 1440–1452.
[27]. Lambertini, M.; Ceppi, M.; Cognetti, F.; Cavazzini, G.; De Laurentiis, M.; De Placido, S.; Michelotti, A.;
Bisagni, G.; Durando, A.; Valle, E.; et al. Dose-dense adjuvant chemotherapy in premenopausal breast cancer
patients: A pooled analysis of the MIG1 and GIM2 phase III studies. Eur. J. Cancer 2017, 71, 34–42.
[28]. Cardonick, E.; Gilmandyar, D.; Somer, R.A. Maternal and Neonatal Outcomes of Dose-Dense Chemotherapy for Breast Cancer in Pregnancy. Obstet. Gynecol. 2012, 120, 1267–1272.
[29]. Alfasi, A.; Ben-Aharon, I. Breast Cancer during Pregnancy—Current Paradigms, Paths to Explore. Cancers 2019, 11, 1669.
[30]. Van Calsteren, K.; Verbesselt, R.; Ottevanger, N.; Halaska, M.; Heyns, L.; Van Bree, R.; de Bruijn, E.; Chai, D.; Delforge, M.; Noens, L.; et al. Pharmacokinetics of chemotherapeutic agents in pregnancy: A preclinical and clinical study. Acta Obstet. Gynecol. Scand. 2010, 89, 1338–1345.
[31]. Berveiller, P.; Mir, O.; Degrelle, S.A.; Tsatsaris, V.; Selleret, L.; Guibourdenche, J.; Evain-Brion, D.; Fournier, T.; Gil, S. Chemotherapy in pregnancy: Exploratory study of the eects of paclitaxel on the expression of placental drug transporters. Investig. New Drugs 2019, 37, 1075–1085.
[32]. Barthelmes, L.; Gateley, C.A. Tamoxifen and pregnancy. Breast 2004, 13, 446–451.
[33]. Halakivi-Clarke, L.; Cho, E.; Onojafe, I.; Liao, D.J.; Clarke, R. Maternal exposure to tamoxifen during pregnancy increases carcinogen-induced mammary tumorigenesis among female rat ospring. Clin. Cancer Res. 2000, 6, 305–308.
[34]. Buonomo, B.; Brunello, A.; Noli, S.; Miglietta, L.; Del Mastro, L.; Lambertini, M.; Peccatori, F.A. Tamoxifen Exposure during Pregnancy: A Systematic Review and Three More Cases. Breast Care 2020, 15, 148–156.
[35]. Al Jishi, T.; Sergi, C. Current perspective of diethylstilbestrol (DES) exposure in mothers and ospring.
Reprod. Toxicol. 2017, 71, 71–77.
[36]. Lambertini, M.; Peccatori, F.A.; Demeestere, I.; Amant, F.; Wyns, C.; Stukenborg, J.-B.; Paluch-Shimon, S.; Halaska, M.J.; Uzan, C.; Meissner, J.; et al. Fertility preservation and post-treatment pregnancies in post-pubertal cancer patients: ESMO Clinical Practice Guidelines. Ann. Oncol. 2020, 31, 1664–1678.
[37]. Tiboni, G.M. Aromatase inhibitors and teratogenesis. Fertil. Steril. 2004, 81, 1158–1159.

