Tóm tắt: Thiếu máu là một tình trạng phổ biến ở bệnh nhân ung thư, có thể là hệ quả trực tiếp của bệnh hay độc tính của các phương pháp điều trị. Tình trạng thiếu máu đóng vai trò là một yếu tố tiên lượng độc lập liên quan đến rút ngắn thời gian sống còn và tăng tỷ lệ biến chứng. Điều này nhấn mạnh tầm quan trọng của việc sàng lọc và quản lý thiếu máu một cách hiệu quả để có thể giảm thiểu tác động của nó.
Nội dung chính
Định nghĩa và mức độ phổ biến của thiếu máu ở người bệnh ung thư
Thiếu máu được chẩn đoán dựa trên ngưỡng hemoglobin (Hb) tiêu chuẩn của Tổ chức Y tế Thế giới (WHO): dưới 12.0 g/dL ở phụ nữ và dưới 13.0 g/dL ở nam giới. Mức độ nghiêm trọng được phân loại theo Tiêu chí thuật ngữ chung về các biến cố bất lợi liên quan đến điều trị (CTCAE), với chỉ số Hb dưới 8 g/dL được định nghĩa là thiếu máu nặng (độ 3).
Tỷ lệ thiếu máu ở người bệnh ung thư dao động tùy thuộc vào loại ung thư, giai đoạn và phác đồ điều trị. Một nghiên cứu tổng quan hệ thống năm 2004 cho thấy có tới 80% người bệnh ung thư giai đoạn tiến triển bị thiếu máu tại một thời điểm nào đó trong liệu trình điều trị. Mặc dù thiếu máu thường liên quan đến các tác nhân hoá trị gây độc tế bào cổ điển, các loại thuốc mới hơn vẫn có thể gây giảm hemoglobin.
Nguyên nhân của thiếu máu
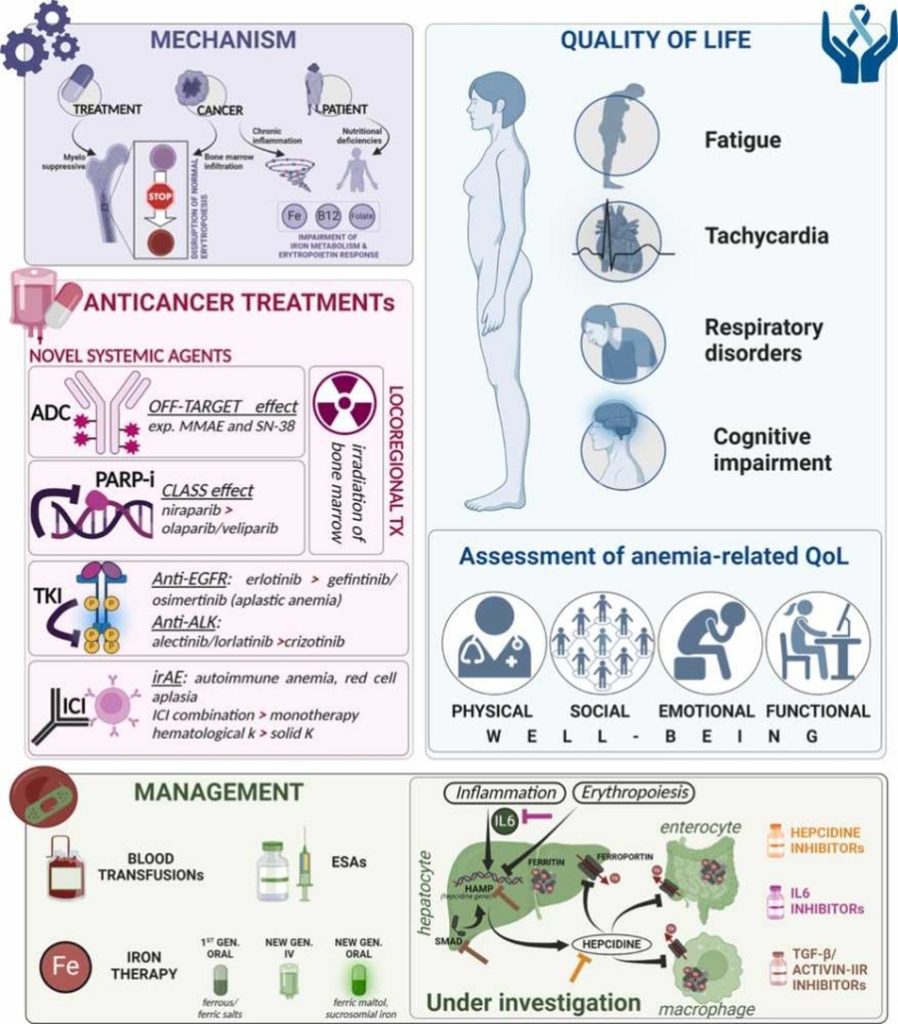
Thiếu máu ở người bệnh ung thư có thể là hệ quả của bệnh lý ung thư, độc tính của các phương pháp điều trị và các tình trạng bệnh lý kết hợp.
– Do bệnh ung thư:
- Xâm lấn tủy xương bởi các tế bào ác tính, làm gián đoạn quá trình tạo hồng cầu bình thường.
- Tình trạng viêm mạn tính do ung thư dẫn đến giải phóng cytokine, làm suy giảm cân bằng nội môi sắt và quá trình sinh tổng hợp và hoạt động của erythropoietin.
- Mất máu do chảy máu từ các tổn thương ung thư. Ví dụ: Ho máu, chảy máu tiêu hoá (Nôn, đại tiện ra máu…)
- Phá hủy hồng cầu do tan máu.
– Độc tính của các phương pháp điều trị
- Hóa trị: Các tác nhân hóa trị cổ điển tác động mạnh đến các tế bào có hoạt động phân bào mạnh, bao gồm cả các tế bào gốc, tiền thân của các dòng tế bào máu tại tủy xương.
- Xạ trị: Có thể gây ra các tác dụng tương tự, đặc biệt khi được vùng chiếu xạ ảnh hưởng đến một thể tích đáng kể tủy xương tạo máu như vùng chậu, cột sống và xương dài.
- Các liệu pháp sinh học mới: Có thể can thiệp vào quá trình tạo hồng cầu hoặc làm trầm trọng thêm tình trạng thiếu máu hiện có.
– Các yếu tố liên quan đến người bệnh:
- Thiếu hụt dinh dưỡng: Suy mòn do ung thư và chế độ dinh dưỡng kém có thể dẫn đến thiếu hụt các nguyên liệu cần thiết cho quá trình tạo hồng cầu như sắt, vitamin B12 và folate.
Tác động của các liệu pháp mới đến tình trạng thiếu máu của người bệnh ung thư
Mặc dù thiếu máu ở người bệnh ung thư, kinh điển, gắn liền với các tác nhân hóa trị gây độc tế bào, một số liệu pháp sinh học mới vẫn có thể gây ra các độc tính trên hệ tạo máu.
– Liệu pháp kháng thể liên hợp thuốc (ADCs – Antibody-Drug Conjugates):
- Cấu trúc và cơ chế: Cấu trúc ADCs gồm kháng thể đơn dòng quyết định tính đặc hiệu kháng nguyên của thuốc, phân tử gây độc tế bào (Được gọi la “payload”) và một chất liên kết giúp ổn định cấu trúc thuốc. Độc tính huyết học là một tác dụng phụ của payload.
- Tỷ lệ thiếu máu: Hầu hết các ADCs có thể gây độc tính huyết học, với tỷ lệ thiếu máu mọi cấp độ khoảng 30% và độ 3-4 khoảng 15%. Một số payload như monomethyl auristatin E (MMAE) liên quan đến thiếu máu nặng hơn. Nguy cơ thiếu máu khác nhau đáng kể giữa các ADCs, ngay cả khi chúng có cùng payload hoặc kháng thể.
- Các ví dụ cụ thể:
- Trastuzumab deruxtecan (T-DXd): Gây thiếu máu mọi cấp độ khoảng 35% và thiếu máu nặng khoảng 12% ở bệnh nhân ung thư vú, và thậm chí cao hơn ở ung thư dạ dày (58% mọi cấp độ, 38% mức độ nặng).
- Trastuzumab emtansine (T-DM1): Thiếu máu là một trong những biến cố bất lợi độ 3 hoặc nặng hơn phổ biến nhất, với tỷ lệ tương tự T-DXd, và cũng là biến cố gây tử vong phổ biến nhất được báo cáo với T-DM1 (khoảng 1.7%).
- Sacituzumab govitecan: Một ADC bao gồm kháng thể kháng TROP2 (Sacituzumab) và payload ứng chế topoisomerase I – SN38. Tỷ lệ thiếu máu mọi cấp độ khoảng 35% và thiếu máu nặng 6-10% trong các thử nghiệm lâm sàng. Trong thực tế, tỷ lệ này có thể lên tới 80% đối với thiếu máu mọi cấp độ ở bệnh nhân điều trị bổ trợ sau mổ. Kiểu gen UGT1A1 *28/*28 có thể làm tăng gấp đôi tỷ lệ thiếu máu nặng.
- Enfortumab vedotin: ADC nhắm trực tiếp đến Nectin-4 với monomethyl auristatin E (MMAE) làm payload, được chỉ định hiện nay cho ung thư biểu mô đường niệu giai đoạn tiến xa. Nhìn chung, liệu pháp này gây nguy cơ thiếu máu thấp hơn so với hóa trị (11% mọi cấp độ, 3% nặng).
– Thuốc ức chế Poly ADP ribose polymerase (PARPi):
- Cơ chế: Ức chế PARP, một enzym sửa chữa DNA, dẫn đến tổn thương sợi kép DNA và gây chết tế bào ung thư, đặc biệt ở những tế bào có khiếm khuyết tái tổ hợp tương đồng (ví dụ, do thiếu BRCA).
- Tác dụng phụ: Độc tính huyết học, bao gồm thiếu máu, là một tác dụng của cả nhóm thuốc này, có thể do “bẫy” PARP, thuốc PARPi liên kết phân tử PARP với các vị trí DNA bị hư hỏng, không chỉ làm suy giảm khả năng tiếp cận các protein sửa chữa, mà còn, đặc biệt với PARP-2 có vẻ liên quan đến quá trình tạo hồng câu, gây ra tình trạng thiếu máu,
- Các ví dụ cụ thể: Niraparib liên quan đến tỷ lệ thiếu máu cao nhất trong tất cả các PARPi, mặc dù Olaparib, Rucaparib và Talazoparib cũng có khuynh hướng độc tính rõ rệt hơn đối với dòng hồng cầu.
- Kết hợp thuốc: Dữ liệu an toàn với Olaparib + Bevacizumab nằm trong giới hạn chấp nhận được. Tuy nhiên, nguy cơ khi kết hợp PARPi với hóa trị dựa trên platinum chưa được hiểu rõ hoàn toàn.
– Thuốc ức chế Tyrosine-kinase (TKIs):
- TKI kháng EGFR (trong ung thư phổi không tế bào nhỏ): Erlotinib có tỷ lệ thiếu máu cao hơn (khoảng 25%) so với Gefitinib (khoảng 10%). Osimertinib (thế hệ thứ ba) có nguy cơ thấp hơn (khoảng 10%). Cần lưu ý về nguy cơ thiếu máu bất sản (aplastic anaemia) dù hiếm gặp với Osimertinib.
- TKI kháng ALK (trong ung thư phổi không tế bào nhỏ ALK-dương tính): Thiếu máu mức độ thấp là một độc tính đã biết, với tỷ lệ cao hơn ở các tác nhân thế hệ thứ ba như Alectinib và Lorlatinib (lên đến 25% mọi cấp độ) so với Crizotinib. Cơ chế chính xác chưa được hiểu rõ hoàn toàn, nhưng sự can thiệp vào quá trình chuyển hóa hồng cầu và tính toàn vẹn của màng, gây ra biến dạng hồng cầu và tan máu, đã được đề xuất.
– Thuốc ức chế điểm kiểm soát miễn dịch (ICIs):
- Tỷ lệ thiếu máu nặng: Dao động từ 0.1% đến 17%.
- Cơ chế: Độc tính huyết học của ICIs có thể do cơ chế không miễn dịch hoặc miễn dịch, khó phân biệt trên thực tế lâm sàng. Thiếu máu tan máu do miễn dịch do sản xuất tự kháng thể do mất ức chế miễn dịch qua tế bào T điều hoà Treg) và/hoặc hoạt hoá tế bào B, cũng có thể do các cơ chế gây độc tế bào qua trung gian lympho T. Tình trạng này được chẩn đoán dựa trên sự giảm đột ngột Hemoglobin huyết thanh ≥ 2 g/dL cùng với các xét nghiệm gợi ý tan máu (Công thức máu ngoại vi, số lượng hồng cầu lưới, thử nghiệm Coombs, ngưng kết lạnh, LDH, bilirubin gián tiếp và haptoglobin). ICIs rất hiếm gặp (Khoảng 0,3% trường hợp) gây ra suy tuỷ xương với biểu hiện bất sản hồng cầu thuần tuý, giảm hai hay ba dòng tế bào máu. Sinh thiết tuỷ xương hay huyết tuỷ đồ ở hầu hết những bệnh nhân giảm nặng toàn bộ các dòng tế bào máu cho thấy tình trạng thiếu máu bất sản nghiêm trọng. Khác với thiếu máu tan máu, dạng độc tính huyết học này thường đi kèm với đáp ứng kém với các trị liệu và tỷ lệ tử vong cao.
- Xử trí: Điều trị thiếu máu tan máu miễn dịch bao gồm ngừng ICI, corticosteroid có hoặc không có rituximab, và các thuốc ức chế miễn dịch khác nếu cần. Hầu hết bệnh nhân phục hồi trong vòng 1 tháng, nhưng có nguy cơ tái phát biến cố bất lợi liên quan miễn dịch 50% nếu tiếp tục ICI.
Thiếu máu và chất lượng cuộc sống
Bên cạnh các ý nghĩa lâm sàng, thiếu máu ảnh hưởng sâu sắc đến chất lượng cuộc sống của bệnh nhân ung thư, dẫn đến tăng mệt mỏi, giảm khả năng hoạt động thể chất. Bệnh nhân thiếu máu thường bị hạn chế trong các hoạt động hàng ngày, giảm khả năng tham gia vào các vai trò xã hội và nghề nghiệp, dẫn đến suy sụp về tinh thần.
– Các triệu chứng ảnh hưởng đến chất lượng cuộc sống: Mệt mỏi, tim đập nhanh, rối loạn hô hấp, suy giảm nhận thức.
– Công cụ đánh giá chất lượng cuộc sống người bệnh ung thư thiếu máu: Các công cụ như EORTC QLQ-C30 và FACT-An (đặc biệt cho thiếu máu) đã được phát triển để đánh giá QoL.
– Nghiên cứu về chất lượng cuộc sống: Các nghiên cứu đã xác nhận tác động tiêu cực của thiếu máu lên QoL, với bệnh nhân thiếu máu báo cáo các triệu chứng rõ rệt hơn về mệt mỏi, khó thở, đau, chán ăn, buồn nôn, nôn và tiêu chảy, cùng với chức năng thể chất, vai trò và cảm xúc kém hơn.
– Có sự khác biệt theo tuổi: Có những kết quả mâu thuẫn về tác động của thiếu máu lên chất lượng cuộc sống theo tuổi, một số nghiên cứu cho thấy người lớn tuổi bị ảnh hưởng nặng hơn, trong khi một số khác lại cho thấy bệnh nhân trẻ tuổi dễ bị tổn thương hơn.
– Cải thiện chất lượng cuộc sống khi điều trị thiếu máu: Các thử nghiệm đã chứng minh rằng việc điều trị thiếu máu, ví dụ bằng epoetin alfa, có thể tăng mức hemoglobin và cải thiện tất cả các lĩnh vực chất lượng cuộc sống đặc hiệu cho thiếu máu, bao gồm mệt mỏi và khả năng thực hiện các hoạt động hàng ngày.
Quản lý người bệnh ung thư thiếu máu
Quản lý thiếu máu ở bệnh nhân ung thư cần một phương pháp tiếp cận toàn diện, đa mô thức với hai mục tiêu chính: Điều trị thiếu máu và cho phép tiếp tục liệu pháp toàn thân, duy trì mức hemoglobin chấp nhận được.
– Truyền hồng cầu:
- Ưu điểm: Can thiệp tức thì và hiệu quả nhất cho thiếu máu nặng, có triệu chứng và/hoặc đe dọa tính mạng, nhanh chóng tăng hemoglobin và hematocrit, giảm các triệu chứng mệt mỏi và khó thở.
- Hạn chế: Có các nguy cơ biến cố cấp tính và dài hạn đáng kể như sốt, phản ứng dị ứng, lây truyền bệnh nhiễm trùng, quá tải sắt, và ức chế miễn dịch. Truyền máu cũng liên quan đến tỷ lệ biến cố huyết khối tắc mạch và tử vong cao hơn ở những bệnh nhân ung thư nhập viện. Ngoài ra, truyền máu chỉ mang lại lợi ích tạm thời.
- Các yếu tố quyết định truyền hồng cầu bao gồm chỉ số hemoglobin, gánh nặng triệu chứng và phân tầng nguy cơ của người bệnh (Phác đồ hoá trị liều cao/xạ trị và các bệnh đồng mắc).
– Các tác nhân kích thích tạo hồng cầu (ESAs – Erythropoiesis-stimulating agents):
- Cơ chế: Là các chất tương tự erythropoietin, kích thích sản xuất hồng cầu.
- Chỉ định: Được chỉ định cho bệnh nhân đang hóa trị và thiếu máu có triệu chứng với Hb < 10 g/dL hoặc thiếu máu không triệu chứng với Hb < 8 g/dL, sau khi điều chỉnh thiếu sắt và các nguyên nhân khác.
- Lợi ích: Giảm nhu cầu truyền máu và duy trì mức hemoglobin ổn định.
- Rủi ro và tranh cãi:
- Tăng nguy cơ huyết khối tắc mạch (50-75% ở bệnh nhân được điều trị bằng ESAs).
- Tăng tỷ lệ tử vong khi ESAs được sử dụng với ngưỡng Hb cao hơn (Hb > 12 g/dL).
- Khả năng ESAs kích thích tăng trưởng khối u vẫn còn gây tranh cãi, do các nghiên cứu tiền lâm sàng cho thấy erythropoietin tái tổ hợp có thể kích thích tăng sinh tế bào khối u trong điều kiện thiếu oxy và thay đổi biểu hiện của VEGF, HIF1alfa, PD-L1, đồng thời có thể tạo ra môi trường vi mô khối u ức chế miễn dịch, giảm hiệu quả của liệu pháp miễn dịch.
- Hiện tại: Vai trò của ESAs đã giảm đi đáng kể trong những năm gần đây do bằng chứng về tăng nguy cơ huyết khối tắc mạch và tử vong, đặc biệt ở những bệnh nhân không được bổ sung sắt đầy đủ. Chỉ định của ESAs đã được hạn chế đối với bệnh nhân được điều trị với mục đích giảm nhẹ.
– Bổ sung sắt:
- Tầm quan trọng: Thiếu sắt là yếu tố then chốt trong thiếu máu liên quan đến ung thư và góp phần làm trầm trọng thêm tình trạng này.
- Thiếu sắt tuyệt đối và chức năng: Đặc trưng bởi tình trạng thiếu sắt mặc dù có đủ dự trữ sắt, liên quan đến sự cô lập sắt do tín hiệu tiền viêm, dẫn đến tăng mức hepcidin lưu hành. Hepcidin có thể giảm hoạt động của nồng độ erythropoietin thấp trên các tế bào tiền thân hồng cầu
- Các dạng bổ sung sắt:
- Sắt uống truyền thống: Có nhiều nhược điểm như thời gian điều trị dài hơn, tác dụng phụ đường tiêu hóa (30-70% bệnh nhân), và sinh khả dụng thấp (10-15%). Không hiệu quả cho thiếu máu liên quan viêm.
- Sắt tiêm tĩnh mạch: Được coi là hiệu quả hơn, đặc biệt trong trường hợp kém hấp thu. Tuy nhiên, vẫn có nguy cơ phản ứng truyền dịch nhỏ (1/200) và phản ứng phản vệ (<1/200.000). Việc này cũng gây gánh nặng công việc và chi phí đáng kể cho hệ thống chăm sóc sức khỏe do cần giám sát tại bệnh viện.
- Các chế phẩm sắt uống thế hệ mới:
- Sắt maltol: Chưa có nhiều dữ liệu bằng chứng về hiệu quả ở người bệnh ung thư thiếu máu.
- Sắt Sucrosomial (SI): Đã được chứng minh khả năng dung nạp tốt và hiệu quả trong việc tăng nồng độ hemoglobin ở bệnh nhân ung thư thiếu máu, có hoặc không hóa trị. SI cũng cải thiện đáp ứng huyết học với ESA, cho thấy tác dụng hiệp đồng. SI ít bị ảnh hưởng bởi tương tác thuốc-thuốc và thức ăn, hấp thu phần lớn không phụ thuộc hepcidin, và có thể giảm hepcidin trong môi trường viêm mạn tính, tăng cường hấp thu sắt từ chế độ ăn uống.
- Thận trọng: Có giả thuyết cho rằng bổ sung sắt có thể ảnh hưởng đến đa dạng vi khuẩn đường ruột, tăng nguy cơ mầm bệnh đường ruột, mặc dù thấp hơn đối với SI.
– Các lựa chọn điều trị mới:
- Thuốc ức chế hepcidin: Hepcidin đóng vai trò chính trong thiếu máu do viêm mạn tính. Các thuốc ức chế hepcidin như kháng thể đơn dòng LY2787106 và oligonucleotide RNA NOX-H94 đã cho thấy kết quả sơ bộ đầy hứa hẹn trong các thử nghiệm lâm sàng ban đầu, nhưng cần nghiên cứu thêm.
- Bẫy phân tử thụ thể TGF-β/activin II (Sotatercept và Luspatercept):
- Họ TGF-β gồm nhiều phân tử (TGF-β1, β2, β3, activin A, B, GDFs…) có vai trò điều hoà sự tăng sinh, biệt hoá và chết tế bào. Activin A/B và GDF11 khi gắn vào thụ thể Activin II (ActRIIA hoặc ActRIIB) trên tế bào dòng hồng cầu sẽ ức chế quá trình biệt hoá tế bào tiền thân dòng hồng cầu, từ đó giảm sản xuất hồng cầu. Ở người bệnh ung thư, tăng hoạt hoá trục activin/TGF-β góp phần gây ra thiếu máu mạn tính, đặc biệt ở những người có viêm mạn tính hoặc trải qua hoá trị.
- Các tác nhân nhóm này là protein tái tổ hợp dạng hoà tan của thụ thể ActRIIA hoặc ActRIIB, có khả năng “bẫy” các ligand như activin A, B, GDF8 và GDF11, từ đó ngăn chặn chúng gắn vào thụ thể trên bề mặt tế bào, khôi phục quá trình sinh hồng cầu. Luspatercept đã được phê duyệt cho hội chứng loạn sản tủy có nguy cơ thấp, chứng minh hiệu quả trong việc cải thiện tỷ lệ không phụ thuộc truyền máu. Sotatercept cũng đã chứng minh khả năng dung nạp và hiệu quả trong thiếu máu do ung thư gây ra ở các thử nghiệm giai đoạn 2.
Kết luận
Thiếu máu vẫn là một thách thức đáng kể và đang trở nên phổ biến, cần được quan tâm trong kỷ nguyên Ung thư học chính xác, ảnh hưởng đến kết quả và chiến lược quản lý toàn diện cho người bệnh. Việc quản lý thiếu máu hiệu quả có ý nghĩa quan trọng, để giảm thiểu tác động của nó đến chất lượng cuộc sống. Mặc dù truyền hồng cầu mang lại lợi ích tức thì, chúng đi kèm với những rủi ro đáng kể. Các giải pháp sắt tiêm tĩnh mạch ngày càng an toàn hơn nhưng vẫn gây gánh nặng đáng kể về chi phí và khối lượng công việc.
Phân tích dữ liệu hiện có cho thấy sắt Sucrosomial (SI) đường uống là một lựa chọn điều trị hiệu quả và tiết kiệm chi phí để bổ sung sắt ở bệnh nhân ung thư thiếu máu, mang lại sự tiện lợi cho cả bệnh nhân và hệ thống chăm sóc sức khỏe. Việc giám sát và điều trị thiếu máu kịp thời có thể ngăn ngừa nhu cầu truyền máu, từ đó nâng cao chất lượng cuộc sống bằng cách giảm bớt các triệu chứng và giảm biến chứng liên quan đến điều trị.
Khi xu hướng Ung thư học chính xác tiếp tục phát triển, các chiến lược quản lý thiếu máu cũng cần được tối ưu hóa để cải thiện kết quả và nâng cao chất sóc bệnh nhân. Nghiên cứu trong tương lai nên tập trung vào việc tối ưu hóa các chiến lược quản lý thiếu máu trong bối cảnh điều trị bổ trợ, nhấn mạnh việc phát hiện sớm và các kế hoạch điều trị phù hợp. Việc chủ động giải quyết thiếu máu cho phép cải thiện đáng kể chất lượng cuộc sống của bệnh nhân ung thư, nâng cao khả năng dung nạp và hưởng lợi từ các liệu pháp ung thư, đồng thời giảm thiểu gánh nặng bệnh lý liên quan đến điều trị.