Nội dung chính
Tóm tắt
Ung thư biểu mô tế bào Merkel (Merkel Cell Carcinoma – MCC) là thể ung thư biểu mô thần kinh nội tiết tại da hiếm gặp, chỉ chiếm tỷ lệ dưới 1% ung thư da, sở hữu đặc tính diễn biến lâm sàng đặc biệt ác tính, chủ yếu do polyomavirus Merkel (MCPyV) và bức xạ cực tím gây ra. MCC được báo cáo lần đầu tiên vào năm 1972 và được phân loại là ung thư biểu mô thần kinh nội tiết do sự giống nhau về hình thái tế bào thần kinh nội tiết với nhân tròn hoặc bầu dục đồng nhất và bào tương ít. Tuy nhiên, các tế bào Merkel là dạng biệt hóa cuối cùng, và do đó, tế bào gốc được giả định hiện nay là từ một tế bào tiền thân, có thể liên quan đến các tế bào tiền B, tế bào pro-B, nguyên bào sợi, tế bào gốc trung mô ở da, hoặc các tế bào tiền thân biểu bì. Các khối u thường phát sinh nhất ở lớp hạ bì nhưng đã được xác định ở tất cả các lớp mô học của da, bao gồm cả tổ chức mô dưới da và thượng bì, với tới 10% các trường hợp MCC cho thấy các tế bào MCC dạng Paget trong thượng bì.
Do sự hiếm gặp và biểu hiện lâm sàng ban đầu không đặc hiệu, việc chẩn đoán MCC thường bị trì hoãn. Bệnh có tiên lượng tồi, thậm chí còn tồi hơn u hắc tố ác tính, với tỷ lệ sống thêm sau 5 năm ước tính từ 35% đến 60% đối với bệnh giai đoạn I hoặc II, và dưới 15% đối với giai đoạn bệnh di căn.
Đối với bệnh giai đoạn khu trú, phẫu thuật cắt rộng u cùng với xạ trị bổ trợ là chiến lược điều trị tiêu chuẩn. Liệu pháp miễn dịch với các tác nhân ức chế PD-1/PD-L1 hiện là lựa chọn chuẩn cho giai đoạn tiến triển, không có khả năng phẫu thuật. Ngoài ra, nhiều thử nghiệm lâm sàng đang diễn ra nhằm khảo sát các liệu pháp ức chế điểm kiểm soát miễn dịch mới, các chất điều hòa miễn dịch, liệu pháp nhắm đích, liệu pháp tế bào, vắc-xin và liệu pháp virus tiêu diệt khối u với mục tiêu cải thiện kết quả cho bệnh nhân mắc bệnh tiến triển hoặc những người tái phát sau liệu pháp miễn dịch bước đầu.
I. Chẩn đoán Ung thư biểu mô tế bào Merkel (MCC)
1. Đặc điểm dịch tễ và yếu tố nguy cơ:
- Tuổi: Tuổi trung bình tại thời điểm chẩn đoán là 77 tuổi, tỷ lệ mắc tăng mạnh theo tuổi.
- Phơi nhiễm tia cực tím (UV): Tỷ lệ mắc MCC liên quan chặt chẽ với vùng địa lý vĩ độ thấp và chỉ số bức xạ UV cao, khối u thường xuất hiện ở các vùng da tiếp xúc nắng. Một phân nhóm MCC (thường âm tính với virus) ở bệnh nhân da trắng sống ở vùng tiếp xúc UV cao, có đặc điểm là gánh nặng đột biến khối u cao với dấu hiệu UV điển hình (Các đột biến gen đặc trưng liên quan đến tình trạng phơi nhiễm tia UV).
- Giới tính: Tỷ lệ mắc bệnh ở nam giới cao hơn 2.5 lần so với nữ giới.
- Suy giảm miễn dịch: Khoảng 6-12% bệnh nhân MCC bị suy giảm miễn dịch. Nguy cơ mắc MCC tăng đáng kể ở bệnh nhân mắc bệnh lý ác tính về huyết học (đặc biệt là bệnh bạch cầu lympho mạn tính), nhiễm HIV/AIDS, và những người nhận ghép tạng đặc.
- Nhiễm Merkel Cell Polyomavirus (MCPyV): MCPyV là tác nhân gây bệnh chính, chịu trách nhiệm cho tới 80% các trường hợp MCC ở châu Âu. MCC dương tính với virus có thể có tiên lượng tốt hơn so với MCC do UV gây ra.
2. Tiếp cận chẩn đoán MCC
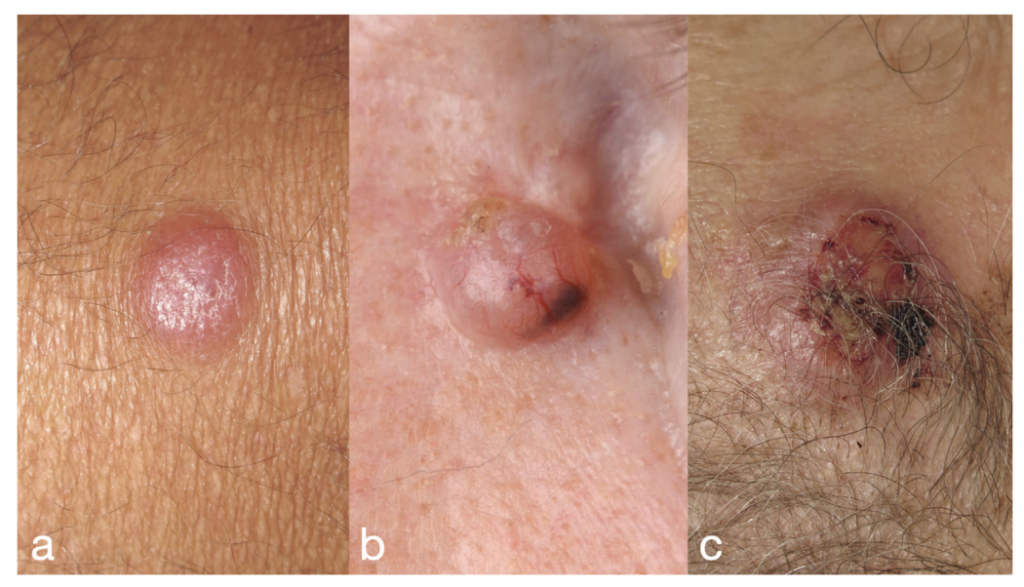
- Biểu hiện lâm sàng: MCC thường biểu hiện dưới dạng một nốt hoặc mảng màu hồng hoặc đỏ, cứng, không đau, phát triển nhanh trong vài tuần hoặc vài tháng (Hình 1). Các vị trí phổ biến nhất là vùng đầu và cổ (29-43.9%) và các chi (36.9-45%).
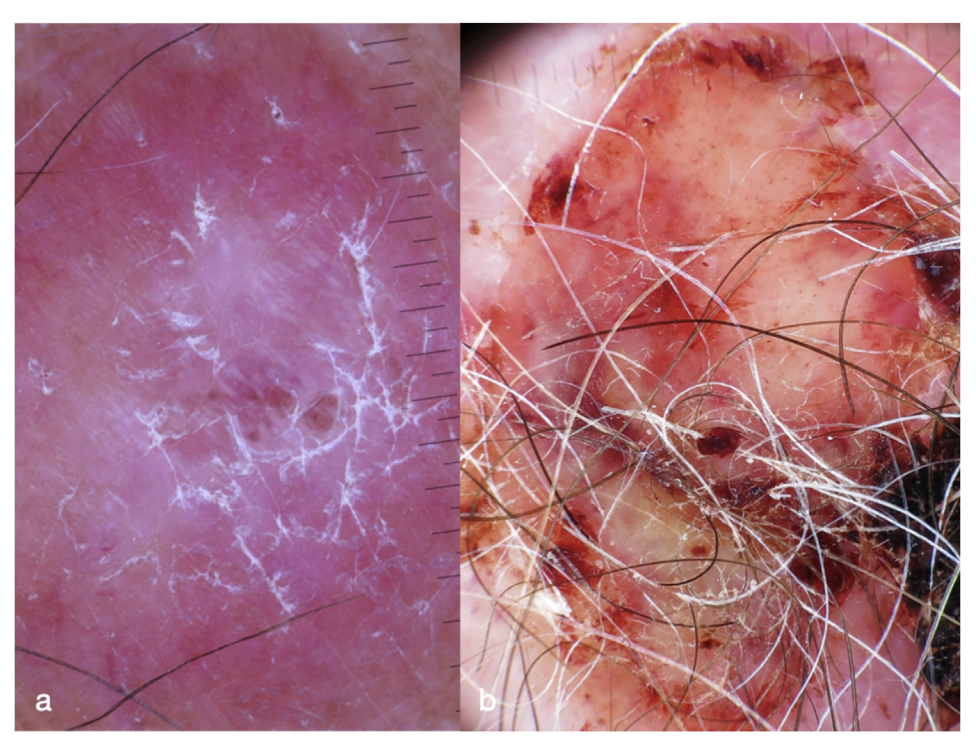
- Đặc điểm soi da (Dermatoscopy): Soi da tổn thương MCC cho thấy màu đỏ chủ đạo tương ứng với nhiều mạch máu hoặc hồng ban. Màu đỏ sữa hoặc hồng không cấu trúc là một đặc điểm soi da khác của MCC, có thể được quan sát thấy dưới dạng màu nền hoặc các vùng tròn nhỏ hơn (Màu đỏ sữa hoặc các khối cầu hoặc cục). Một số hình thái của mạch máu có thể quan sát được, bao gồm dạng chấm, hình cầu, hình cây phân nhánh không đều… (Hình 2).
Chẩn đoán ban đầu: MCC thường bị chẩn đoán ban đầu nhầm với các tổn thương viêm (Mụn trứng cá, viêm nang lông…) hoặc khối u lành tính (u nang biểu bì, u mỡ) hoặc các khối u ác tính khác (ung thư biểu mô tế bào đáy hoặc tế bào vảy, u hắc tố không sắc tố, u lympho). Một khuyến nghị hữu ích cho các bác sĩ lâm sàng là bất kỳ nốt sần nào có hình thái không đặc hiệu, không đau và phát triển nhanh đều nên được sinh thiết.
- Khám lâm sàng: Khám da toàn thân cẩn thận và tất cả các vùng hạch ngoại vi, đặc biệt là hạch vùng tương ứng với vị trí tổn thương da.
- Chẩn đoán hình ảnh: Siêu âm hạch vùng. Cắt lớp vi tính toàn thân được khuyến nghị để loại trừ di căn hạch vùng và di căn xa. PET/CT toàn thân bằng 18-FDG được ưu tiên hơn CT có tiêm thuốc cản quang cổ/ngực/bụng/chậu. MRI não thường không được chỉ định ở bệnh nhân giai đoạn I-II không có triệu chứng.
- Sinh thiết tổn thương da bằng kỹ thuật sinh thiết kim, lấy trọn hoặc một phần tổn thương có thể được thực hiện để lấy được mẫu mô.
- Chẩn đoán mô bệnh học và hóa mô miễn dịch:
- Mô học: Trên tiêu bản nhuộn HE, khối u thường biểu hiện các tấm và ổ tế bào nhỏ, tròn, màu xanh, không biệt hóa, ít bào tương, nhân có hình ảnh “muối tiêu”, hạt nhân lớn, tỷ lệ phân bào cao và đôi khi có tế bào hoại tử. Một biến thể tế bào nhỏ cho thấy các đặc điểm trùng lặp với u lympho biểu hiện tại da. Chẩn đoán phân biệt quan trọng bao gồm u hắc tố, sarcoma Ewing, u nguyên bào thần kinh, bệnh bạch cầu tại da hoặc ung thư biểu mô biệt hóa kém di căn đến da (ví dụ: Ung thư phổi tế bào nhỏ).
- Nhuộm hóa mô miễn dịch là bắt buộc để xác nhận chẩn đoán và phân biệt MCC với các khối u tương tự về mô học. MCC được đặc trưng bởi biểu hiện của cả các dấu ấn biểu mô như cytokeratin 20 (CK20) với kiểu bắt màu dạng chấm cạnh nhân đặc trưng, AE1/AE3 và CAM5.2, và các dấu ấn thần kinh nội tiết như neuron-specific enolase (NSE) (rất nhạy nhưng biểu hiện bởi các khối u thần kinh nội tiết khác), synaptophysin, CD56 và chromogranin A (CgA) (đặc hiệu hơn cho MCC). CgA là dấu ấn được sử dụng phổ biến nhất với kiểu bắt màu bào tương lan tỏa. Ngược lại, các dấu ấn sau đây thường âm tính: thyroid transcription factor 1 (TTF-1) (quan trọng cho chẩn đoán phân biệt với ung thư phổi tế bào nhỏ, đặc biệt khi không rõ vị trí nguyên phát), S-100 và HMB-45 (biểu hiện bởi u hắc tố), leukocyte common antigen và các dấu ấn tế bào lympho khác (biểu hiện bởi u lympho), CK7 và carcinoembryonic antigen (biểu hiện bởi ung thư biểu mô tuyến mồ hôi).

3. Phân giai đoạn và yếu tố tiên lượng
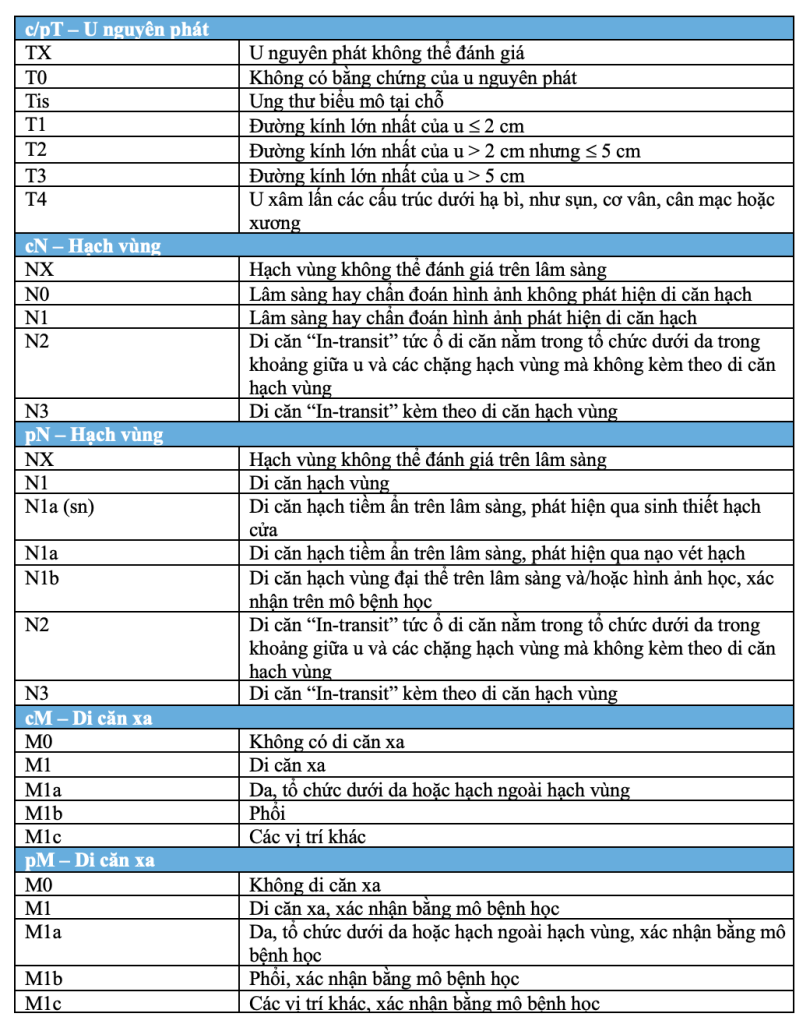
Tiên lượng kết quả sống thêm phụ thuộc vào giai đoạn bệnh tại thời điểm chẩn đoán. Hệ thống phân loại giai đoạn AJCC/UICC 8 được khuyến nghị cho phân loại giai đoạn MCC.
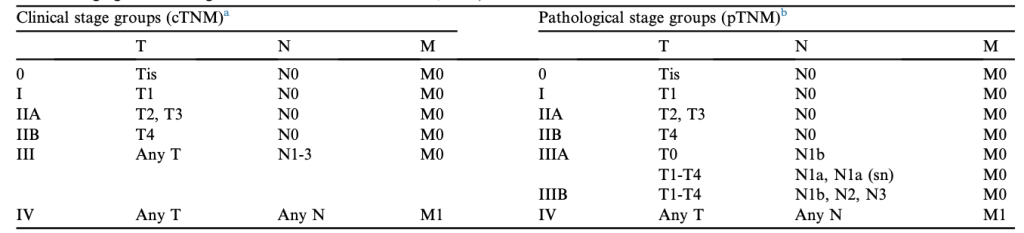
MCC có tỷ lệ tái phát tại chỗ, tái phát vùng và di căn xa cao. Các yếu tố lâm sàng liên quan đến kết quả bất lợi là tuổi cao, giới tính nam, vị trí ở đầu và cổ hoặc thân mình so với chi trên, kích thước khối u nguyên phát (pT) và tình trạng suy giảm miễn dịch đồng mắc. Đường kính dài nhất của khối u, được đưa vào phân loại giai đoạn AJCC 8, cũng là một yếu tố lâm sàng có giá trị dự báo quan trọng. Kích thước khối u có tương quan chặt chẽ với nguy cơ di căn hạch, đây cũng là một yếu tố dự báo tiên lượng rất mạnh. Nguy cơ di căn hạch vùng (vi di căn hoặc di căn đại thể) tăng từ 14% đối với khối u đường kính 0,5 cm lên 25% đối với khối u đường kính 1,7 cm (kích thước trung bình) và lên hơn 36% đối với khối u từ 6 cm trở lên.
Tỷ lệ sống thêm toàn bộ sau 5 năm được báo cáo vào khoảng 60% đối với bệnh giai đoạn I sớm, giảm dần xuống khoảng 35-55% ở giai đoạn II, 26-40% ở giai đoạn III, và dưới 15% ở giai đoạn IV. Ngoài ra, kết quả sống thêm toàn bộ còn liên quan đến độ dày khối u, kích thước khối u, vị trí giải phẫu sâu nhất bị khối u xâm lấn, kiểu tăng trưởng khối u, xâm lấn mạch bạch huyết (LVI), mật độ tế bào lympho xâm nhập khối u, và sự hiện diện hoặc vắng mặt của hiện tượng tích tụ trong biểu bì các sợi elastin bị biến đổi do phơi nhiễm tia UV; độ sâu/độ dày khối u thấp và không có LVI là những yếu tố thuận lợi cho kết quả thời gian sống thêm dài hơn.
Tiên lượng còn phức tạp hơn do tỷ lệ tái phát cao. Nguy cơ tái phát là hơn 50% ở những bệnh nhân chỉ được điều trị bằng phẫu thuật và chỉ giảm nhẹ xuống khoảng 39% khi kết hợp phẫu thuật và xạ trị bổ trợ.
Với sự ra đời của liệu pháp miễn dịch, đã có những hiểu biết mới về các cách tiềm năng để dự đoán và cải thiện tiên lượng. Các dấu ấn như p63, c-kit, PD-1, PD-L1, và sự xâm nhập của tế bào T CD8 là các đặc điểm sinh học có giá trị tiên lượng. Người bệnh có mức độ dương tính c-kit và p63 cao hơn có xu hướng sống thêm ngắn hơn, trong khi đó, bộc lộ PD-1, PD-L1 và sự xâm nhập của bạch cầu lympho T CD8 là các yếu tố tiên lượng thuận lợi. Một thử nghiệm gần đây cho thấy các khối u âm tính với virus có PD-L1 và CD8 cao có đáp ứng thuận lợi hơn với liệu pháp miễn dịch.
Tình trạng dương tính hay âm tính với MCPyV cũng có ảnh hưởng đến tiên lượng của MCC. Một số báo cáo ghi nhận phân nhóm MCC virus dương tính có tiên lượng khả quan hơn với thời gian sống thêm không bệnh tiến triển dài hơn. Điều này được cho là do MCC âm tính với virus có gánh nặng đột biến cao hơn trong khi các khối u dương tính với virus có gánh nặng đột biến thấp hơn.
II. Quản lý Ung thư biểu mô tế bào Merkel (MCC)
1. Phẫu thuật
- Phẫu thuật cắt rộng u là tiêu chuẩn cho điều trị bước đầu MCC giai đoạn khu trú. Mục tiêu là cắt bỏ tổn thương nguyên phát với diện cắt không còn tế bào ung thư trên vi thể (R0). Diện cắt an toàn 1 cm được khuyến nghị, theo sau bởi xạ trị bổ trợ. Nếu dự kiến không thể xạ trị bổ trợ, một diện cắt rộng rãi hơn (lên đến 2 cm) nên được thực hiện.
- Phẫu thuật Mohs: Có thể là một lựa chọn an toàn và hiệu quả thay thế cho cắt rộng u, đặc biệt ở các khu vực giải phẫu nhạy cảm về thẩm mỹ và chức năng như đầu và cổ.
- Quản lý hạch vùng:
- Di căn hạch dưới lâm sàng (Hạch cửa dương tính): Xạ trị bổ trợ đơn thuần (50-55 Gy) hoặc kết hợp với nạo vét hạch hoàn toàn (Complete Lymph Nodes Dissection – CLND) được ưu tiên hơn chỉ CLND.
- Di căn hạch trên lâm sàng: Tiêu chuẩn điều trị là CLND, có thể kèm theo xạ trị bổ trợ sau mổ.
2. Xạ trị
- MCC là thể u nhạy cảm với xạ trị: Tế bào MCC rất nhạy cảm với bức xạ, xạ trị trở thành một công cụ điều trị quan trọng ở nhiều giai đoạn bệnh.
- Xạ trị bổ trợ:
- Sau phẫu thuật cắt bỏ khối u nguyên phát, xạ trị bổ trợ vào giường u giúp cải thiện đáng kể kết quả kiểm soát tái phát tại chỗ và tại vùng, cũng như tỷ lệ sống không bệnh và toàn bộ.
- Nên được thực hiện trong vòng 8 tuần sau phẫu thuật.
- Mức liều thông thường là 50-55 Gy. Nếu diện cắt dương tính, cần liều xạ cao hơn: 60 Gy cho diện cắt R1 và 66 Gy cho diện cắt R2. Bolus nên được xem xét để đảm bảo liều xạ đến da đầy đủ.
- Có thể cân nhắc bỏ qua xạ trị bổ trợ cho các khối u nhỏ (< 2 cm, giai đoạn I), phẫu thuật đạt R0, hạch âm tính và không có yếu tố nguy cơ khác, nhưng cần thảo luận trong hội chẩn tiểu ban đa chuyên khoa.
- Xạ trị đơn thuần/triệt căn: Có thể được xem xét như một lựa chọn thay thế phẫu thuật ở bệnh nhân không đủ điều kiện phẫu thuật hoặc khi khối u ở các khu vực nhạy cảm cần bảo tồn mô. Tổng liều nên là 60-66 Gy với phân liều quy ước 2 Gy.
- Xạ trị giảm nhẹ: Được thực hiện thường quy cho các tổn thương có triệu chứng ở bệnh nhân giai đoạn tiến triển hoặc di căn để giảm gánh nặng khối u và cải thiện chất lượng cuộc sống. Có thể dùng phác đồ 8 Gy trong một lần xạ hoặc 20 Gy trong năm phân liều.
- Phác đồ giảm số phân liều (Hypofractionated schedules): Có thể cân nhắc cho các bệnh nhân cao tuổi, thể trạng “dễ tổn thương” để giảm số lần cần đến bệnh viện.
3. Liệu pháp toàn thân
Liệu pháp miễn dịch (Immunotherapy):
- Là lựa chọn điều trị toàn thân đầu tay cho MCC giai đoạn tiến triển.
- MCC là khối u rất nhạy cảm với miễn dịch, do sự hiện diện của các kháng nguyên “mới” tạo ra bởi tia UV hoặc protein virus.
- Các kháng thể đơn dòng kháng PD-(L)1 như Avelumab (cho MCC di căn) và Pembrolizumab, Retifanlimab (cho MCC tái phát hoặc di căn) đã được FDA chấp thuận.
- Các thử nghiệm pha I/II cho thấy tỷ lệ đáp ứng khách quan cao (33.0%-68%) và thời gian đáp ứng bền vững, với tỷ lệ sống thêm 5 năm được cải thiện đáng kể cho bệnh nhân giai đoạn III và IV (từ 34.1% trước khi có liệu pháp miễn dịch lên 42.9%).
- Hồ sơ độc tính nhìn chung tương đương với các chỉ định khác, với các biến cố bất lợi độ 3-4 xảy ra ở 11.4-28% bệnh nhân được điều trị.
- Tỷ lệ tái phát cao khi ngừng điều trị miễn dịch, đặc biệt nếu bệnh nhân không đạt được đáp ứng hoàn toàn. Tuy nhiên, các bệnh nhân này thường tái nhạy cảm khi điều trị lại.
- Hiện nay, liệu pháp miễn dịch đang được nghiên cứu trong chỉ định điều trị bổ trợ và tân bổ trợ với mục tiêu giảm nguy cơ tái phát sau phẫu thuật.
Hóa trị (Chemotherapy):
- Trước năm 2016, hóa trị là phương pháp điều trị chính cho MCC giai đoạn muộn.
- Hiện nay, hóa trị không còn là lựa chọn hàng đầu cho MCC tiến triển. Nó được dành riêng cho các trường hợp bệnh nhân không đáp ứng, không dung nạp hoặc có chống chỉ định với liệu pháp miễn dịch, hoặc khi liệu pháp miễn dịch hoặc thử nghiệm lâm sàng không có sẵn.
- Các phác đồ phổ biến bao gồm các phác đồ nền tảng platinum, etoposide, taxane hoặc anthracycline.
- Hóa trị có tỷ lệ đáp ứng thay đổi (23-61%), nhưng thời gian sống không bệnh tiến triển (PFS) (3.1 tháng) và sống thêm toàn bộ ngắn (9-9.5 tháng). Hóa trị cũng đi kèm với nguy cơ độc tính cao, đặc biệt ở bệnh nhân lớn tuổi.
Các liệu pháp mới nổi và đang nghiên cứu:
- Liệu pháp nhắm trúng đích (Targeted Therapies): Bao gồm Tuvusertib (chất ức chế ATR kinase), Navtemadlin (chất ức chế MDM2), Bevacizumab kết hợp Atezolizumab, Lenvatinib kết hợp Pembrolizumab. Các nghiên cứu cũng đang tìm hiểu về JAK2, MEK-ERK, và MUC1 như các mục tiêu tiềm năng.
- Liệu pháp tế bào (Cellular Therapies): Đang có các thử nghiệm về tế bào T biến đổi gen biểu hiện thụ thể TCR đặc hiệu với MCPyV, tế bào CAR-T kháng Glypican-3 (GPC3), và liệu pháp tế bào lympho xâm nhập khối u (TIL).
- Vắc-xin điều trị (Therapeutic Vaccines): Các vắc-xin đang được thử nghiệm bao gồm ITI-3000 (vắc-xin DNA cho MCPyV) và các vắc-xin tân kháng nguyên cá nhân hóa.
- Liệu pháp virus gây ly giải khối u (Oncolytic Virus Therapies): Bao gồm Talimogene laherparepvec (T-VEC), MQ710, RP1, MEM-288, VET3-TGI, được thiết kế để ly giải trực tiếp tế bào u hoặc kích hoạt phản ứng miễn dịch kháng u.
- Các phương pháp điều hoà miễn dịch khác: Các chất chủ vận thụ thể TNF, IL-2, IL-15, và các chất điều hòa vi môi trường khối u đang được nghiên cứu để cải thiện hiệu quả của miễn dịch liệu pháp.
III. Các cân nhắc đặc biệt trong quản lý MCC
- Bệnh nhân suy giảm miễn dịch:
- MCC ở bệnh nhân suy giảm miễn dịch có xu hướng diễn biến nặng hơn.
- Tỷ lệ tái phát tại chỗ sau phẫu thuật cao hơn. Hiệu quả của xạ trị ở liều tiêu chuẩn cũng có thể bị suy giảm, với tỷ lệ tái phát tại chỗ cao hơn sau xạ trị giảm nhẹ và PFS giảm khi xạ trị với mục đích triệt căn.
- Dữ liệu về hiệu quả và tác dụng phụ của các chất ức chế điểm kiểm soát miễn dịch (ICI) ở bệnh nhân suy giảm miễn dịch còn hạn chế do tiêu chí loại trừ trong các thử nghiệm lâm sàng then chốt. Các thử nghiệm lâm sàng đang nghiên cứu ICI kết hợp với thuốc ức chế miễn dịch cho bệnh nhân ghép thận.
- Chăm sóc giảm nhẹ và hỗ trợ:
- Tuổi trung bình của bệnh nhân MCC cao (77 tuổi), thường đi kèm với nhiều bệnh nền.
- Đánh giá lão khoa toàn diện và chất lượng cuộc sống liên quan đến sức khỏe (HRQoL) cần được tích hợp vào quá trình ra quyết định điều trị để tối ưu hóa việc quản lý người bệnh là đối tượng dễ bị tổn thương.
- Việc kiểm soát triệu chứng như đau, loét, rỉ dịch, mùi và chảy máu là rất quan trọng để cải thiện chất lượng cuộc sống.
- Nên chuyển bệnh nhân đến đội ngũ chăm sóc hỗ trợ và giảm nhẹ sớm, đặc biệt đối với những bệnh nhân có bệnh tiến triển tại chỗ hoặc di căn có triệu chứng.
IV. Theo dõi và tái phát
- Nguy cơ tái phát: MCC có nguy cơ tái phát cao, đặc biệt trong 2-3 năm đầu sau chẩn đoán ban đầu, với khoảng 40-50% bệnh nhân phát triển di căn hạch và khoảng 33% di căn xa. Các vị trí di căn xa phổ biến nhất là da/mô mềm (25%), gan (23%), xương (21%), tụy (8%), phổi (7%) và não (5%).
- Lịch trình theo dõi:
- Khám lâm sàng: Khám da toàn thân định kỳ, sờ nắn sẹo, da xung quanh và các vùng hạch.
- Chẩn đoán hình ảnh: Siêu âm hạch vùng, Cắt lớp vi tính, MRI và PET-CT (nhạy hơn CT đơn thuần).
- Dấu ấn sinh học: Định lượng Neuron-Specific Enolase trong huyết thanh và hiệu giá kháng thể oncoprotein MCPyV đang được nghiên cứu như các dấu ấn sinh học tiềm năng để theo dõi sự tiến triển và đáp ứng điều trị.
- Nguy cơ ung thư thứ phát: Bệnh nhân MCC có nguy cơ cao phát triển các loại ung thư thứ phát, đặc biệt là ung thư da (u hắc tố và các loại ung thư da không hắc tố khác) và các bệnh lý ác tính về huyết học như CLL.
Tài liệu tham khảo
- Pan K, Vromans AM, Cheng L, Grant-Kels JM, Katz SC, Hadfield MJ. Merkel Cell Carcinoma: Current Treatment Landscape and Emerging Therapeutic Targets. Curr Oncol Rep. 2025 Jun 3. doi: 10.1007/s11912-025-01693-z. Epub ahead of print. PMID: 40459726.
- Cutaneous Merkel cell carcinoma (MCC): A report from the 16th Annual Meeting for Multicenter Merkel Interest Group – A supplementation to the new European guidelines 2022 on MCC. Minutilli, Ettore et al. European Journal of Cancer, Volume 175, 107 – 109