Mặc dù không có dữ liệu ngẫu nhiên xác định khoảng thời gian tối ưu để bắt đầu điều trị hỗ trợ, nhưng hoá trị thường được bắt đầu sau khi hồi phục hoàn toàn, điển hình là từ 4 đến 8 tuần sau phẫu thuật và theo như hầu hết các thử nghiệm hỗ trợ đã hoàn thành [1-6].
Bệnh nhân ung thư đại tràng giai đoạn III thường được hóa trị hỗ trợ từ 3 đến 6 tháng với fluoropyrimidine kết hợp oxaliplatin. Sự cải thiện DFS khi bổ sung oxaliplatin vào fluoropyrimidine đã được chứng minh bằng hai thử nghiệm lớn pha III.
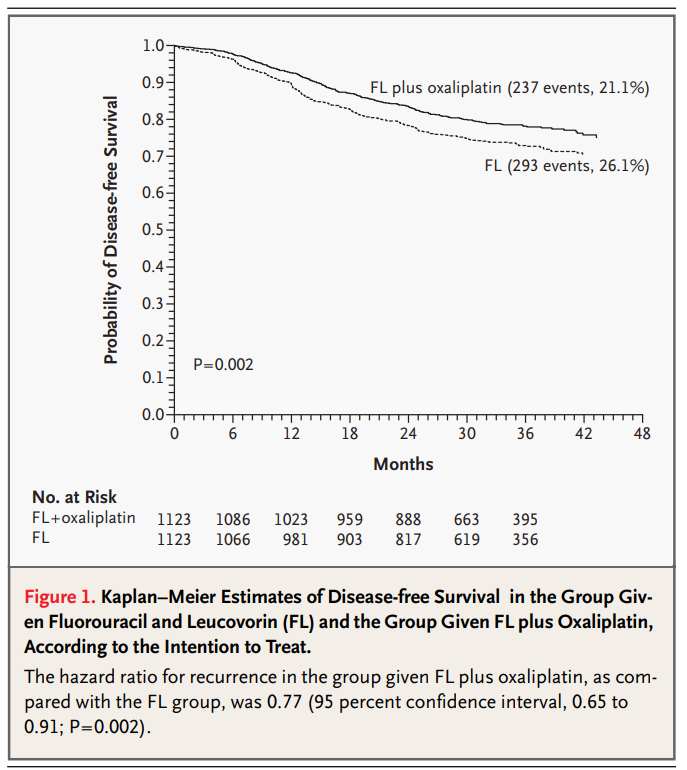
Thử nghiệm MOSAIC ở Châu Âu (Multicenter International Study of Oxaliplatin/5-Fluorouracil/Leucovorin in the Adjuvant Treatment of Colon Cancer) đã chọn ngẫu nhiên 2246 bệnh nhân (60% ở giai đoạn III) dùng FOLFOX (truyền 5-fluorouracil [5-FU] , leucovorin calcium và oxaliplatin) so với 5-FU và leucovorin. Thử nghiệm này đã chứng minh sự cải thiện về tiêu chí chính DFS-5 năm từ 67% đến 73% ở những bệnh nhân được bổ sung oxaliplatin vào 5-FU [5]. Lợi ích về OS đã được ghi nhận ở phân nhóm giai đoạn III (OS-10 năm, 67% so với 59%; HR = 0,80; P = 0,016) [5].
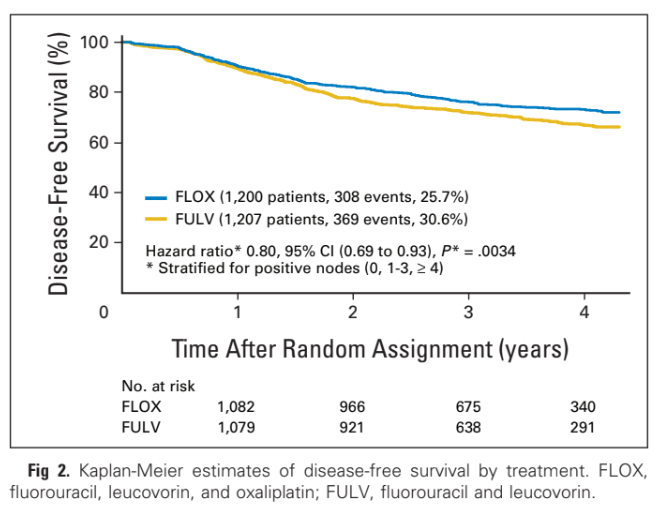
Thử nghiệm NSABP (National Surgical Adjuvant Breast and Bowel Project) C-07 ở Bắc Mỹ đã chọn ngẫu nhiên 2407 bệnh nhân (70% ở giai đoạn III) dùng bolus 5-FU/LV bolus hàng tuần 5-FU, leucovorin (bFU/LV) có (FLOX) hoặc không có oxaliplatin cũng cho thấy sự cải thiện về tiêu chí chính DFS-5 năm với việc bổ sung oxaliplatin (69% so với 64%; HR = 0,82; 95% CI: 0,69 – 0,93) [2]. Tuy nhiên, điều này phải trả giá bằng việc tăng độc tính trên đường tiêu hóa liên quan đến bFU/LV (tiêu chảy ≥ độ 3, 32% so với 38%; nôn ói, 8% so với 13% và rối loạn điện giải, 12% so với 17%, bFU/LV so với FLOX ) và do đó phương pháp sử dụng 5-FU được ưu tiên là điều trị ngoại trú [2].
Cả hai thử nghiệm MOSAIC và NSABP C-07 đều yêu cầu tổng thời gian điều trị hỗ trợ là 6 tháng, điều này có liên quan đến độc tính đáng kể, đặc biệt là bệnh lý thần kinh do oxaliplatin. Hơn 90% bệnh nhân trong thử nghiệm MOSAIC phát triển bệnh lý thần kinh trong quá trình hóa trị, trong đó có 13% có triệu chứng độ 3 trở lên. Sau thời gian theo dõi 48 tháng, bệnh lý thần kinh độ 1, 2 hoặc 3 tồn tại dai dẳng ở 12%, 3% và 0,7% bệnh nhân. Mặc dù tất cả các thử nghiệm này đều sử dụng 5-FU, các thử nghiệm ngẫu nhiên và phân tích gộp khác ủng hộ một cách thuyết phục việc thay thế 5-FU bằng capecitabine trong bối cảnh hỗ trợ [7-9].
Hợp tác IDEA (International Duration Evaluation of Adjuvant Chemotherapy) là một phân tích kết hợp tiến cứu của sáu thử nghiệm quốc tế giai đoạn III điều tra tính không thua kém của 3 so với 6 tháng hóa trị hỗ trợ (FOLFOX hoặc CAPOX [capecitabine và oxaliplatin] theo sự lựa chọn của bác sĩ) trong ung thư đại tràng giai đoạn III với tiêu chí chính là DFS-3 năm [10].
Nghiên cứu đã thất bại trong việc cho thấy sự không kém của 3 tháng điều trị hỗ trợ so với 6 tháng (DFS-3 năm, 74,6% so với 75,5%; HR = 1,07; 95% CI = 1,00 – 1,15; ranh giới HR không thua kém = 1,12). Tuy nhiên, các phân tích phân nhóm được xác định trước dựa trên loại phác đồ cho thấy rằng tính không thua kém của 3 tháng được ghi nhận với CAPOX (HR = 0,95; 95% CI = 0,85 – 1,06) nhưng không ghi nhận với FOLFOX (HR = 1,16; 95% CI = 1,06 – 1,26). Hơn nữa, một phân tích thăm dò ở những bệnh nhân có nguy cơ thấp (T1 – T3 và N1) đã chứng minh tính không thua kém của 3 so với 6 tháng (DFS-3 năm, 83,1% và 83,3%, tương ứng; HR = 1,01; 95% CI = 0,90 – 1.12) và vượt trội của 6 tháng hơn 3 tháng ở những bệnh nhân có nguy cơ cao (T4 hoặc N2) (DFS-3 năm, 64,4% so với 62,7%; HR = 1,12; 95% CI: 1,03 – 1,23) [10].
Sau một thời gian theo dõi dài hơn, kết quả cập nhật cho thấy DFS- 5 năm là 69,1% so với 70,8% (HR = 1,08; 95% CI = 1,01 – 1,15; tỷ lệ phát hiện sai được điều chỉnh P = 0,22); tỉ lệ OS-5 năm là 82,4% so với 82,8% (HR = 1,02; 95% CI = 0,95 – 1,11) và chênh lệch tuyệt đối về tỉ lệ OS-5 năm là -0,4% (95% CI = -2,1% đến 1,3%) [11]. Cùng với nhau, những dữ liệu này gợi ý nêu bật ý nghĩa của việc phân tầng nguy cơ dựa trên giải phẫu bệnh và khả năng rút ngắn thời gian điều trị bằng CAPOX, đặc biệt ở những bệnh nhân có nguy cơ thấp.
Bằng chứng về liệu pháp hỗ trợ cho bệnh nhân giai đoạn II kém thuyết phục hơn. Cho đến nay, nghiên cứu ngẫu nhiên lớn nhất trên bệnh nhân giai đoạn II, QUASAR (Quick and Simple and Reliable), cho thấy lợi ích sống còn khiêm tốn là 3,6% ở những bệnh nhân điều trị 5-FU hỗ trợ so với quan sát sau phẫu thuật [12]. Tuy nhiên, nghiên cứu này có một số hạn chế nghiêm trọng, bao gồm tuyển chọn bệnh nhân ung thư trực tràng (29%), số lượng hạch bạch huyết được đánh giá hạn chế (trung vị 6) và xạ trị ở một số bệnh nhân (14%) [12].
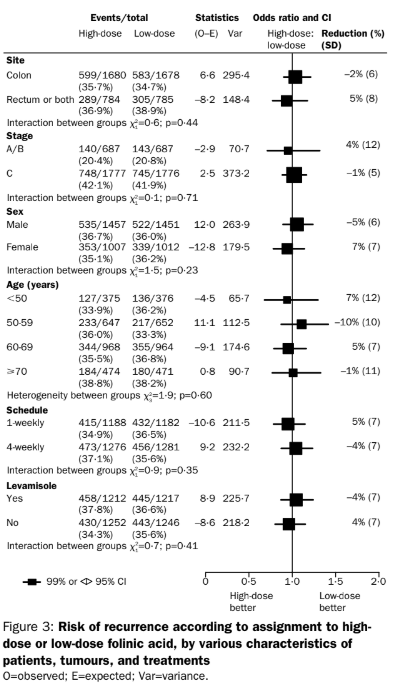
Các phân tích tổng hợp khác đã cho thấy những cải thiện nhỏ về DFS (5% – 10%) nhưng không cải thiện về OS đối với việc sử dụng 5-FU so với quan sát trong ung thư đại tràng giai đoạn II [13-16]. Phân tích dưới nhóm ở bệnh nhân giai đoạn II từ các thử nghiệm MOSAIC và NSABP C-07 cho thấy không có lợi ích có ý nghĩa thống kê về cả OS hoặc DFS khi bổ sung oxaliplatin vào 5-FU [5]. Những phát hiện này cũng được ủng hộ bởi một phân tích tổng hợp của cơ sở dữ liệu ACCENT (Adjuvant Colon Cancer End Points) [17-19].
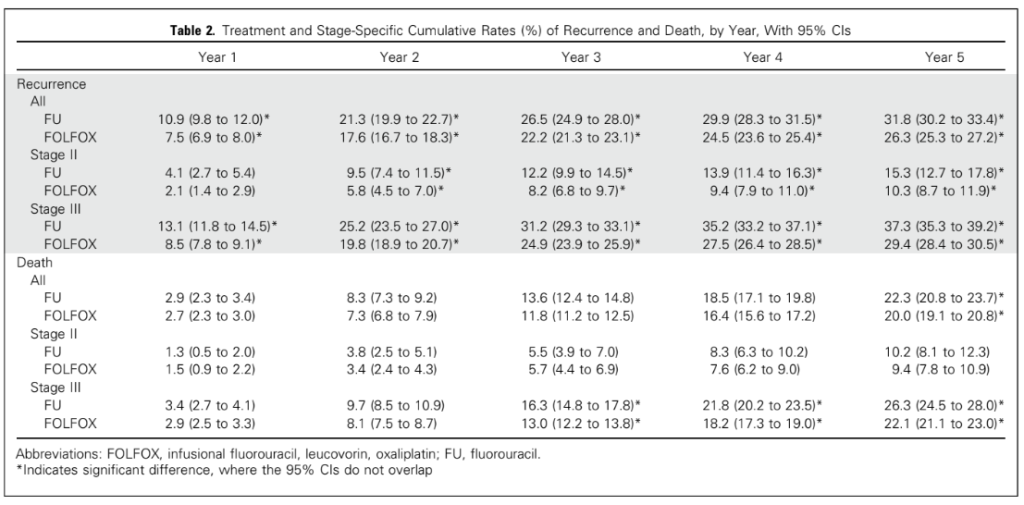
Tuy nhiên, một nhóm bệnh nhân giai đoạn II có nguy cơ tái phát cao có thể được xác định dựa trên các đặc điểm mô bệnh học. Những đặc điểm này được NCCN xác định là khối u T4 (giai đoạn IIB/IIC); mô học kém biệt hóa (không bao gồm mất ổn định vi vệ tinh mức độ cao [MSI-H]); xâm lấn lymphô mạch máu (LVI); xâm lấn thần kinh (PNI); tắc ruột; thủng tại chỗ; diện cắt gần, không xác định hoặc dương tính; và lấy mẫu hạch bạch huyết không đầy đủ (< 12 hạch) [20].
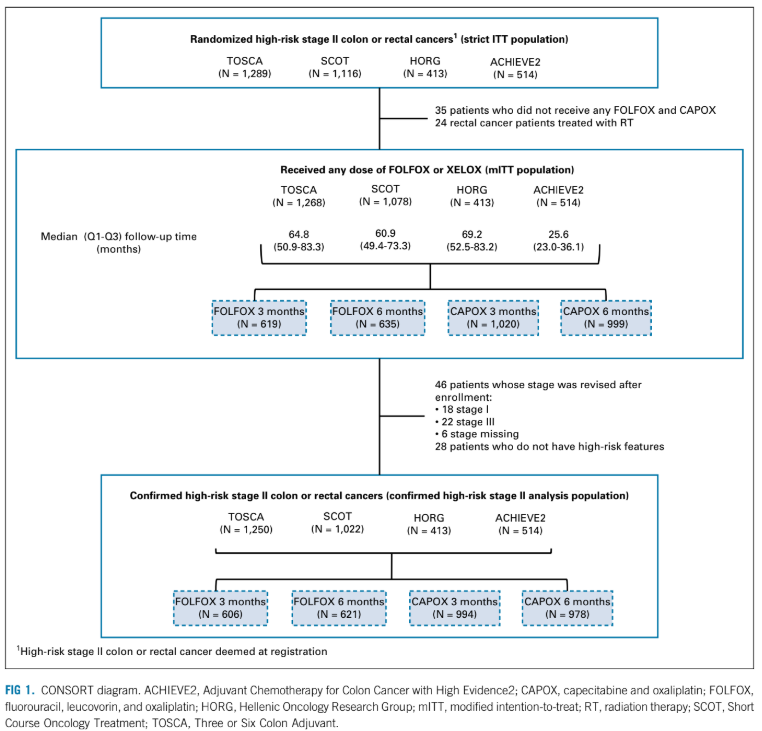
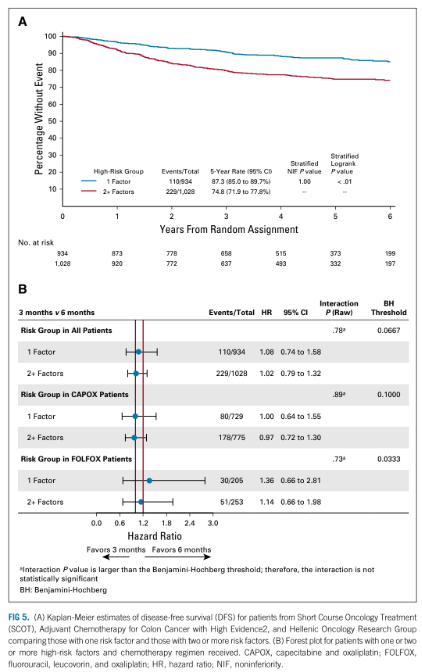
Dữ liệu từ các thử nghiệm ngẫu nhiên cho thấy rằng những bệnh nhân ung thư đại tràng giai đoạn II có nguy cơ cao có thể nhận được lợi ích khiêm tốn từ việc bổ sung oxaliplatin vào fluoropyrimidine. Trong các phân tích thăm dò của thử nghiệm MOSIAC, có xu hướng cải thiện DFS (82% so với 77%) và OS (85% so với 83,3%) mà không đạt được ý nghĩa thống kê trong phân nhóm này [5]. Một phân tích tổng hợp được lên kế hoạch trước trên 3273 bệnh nhân ung thư đại tràng giai đoạn II có nguy cơ cao từ bốn thử nghiệm trong dữ liệu hợp tác IDEA đã thất bại trong việc cho thấy sự không kém của 3 so với 6 tháng sử dụng liệu pháp hỗ trợ (80,7% so với 84%; HR DFS = 1,18; 80% CI = 1,05 – 1,31; P = 0,404; ranh giới không thua kém = 1,2). Giống như bệnh nhân giai đoạn III, độc tính thấp hơn đáng kể ở nhóm 3 tháng và dường như có xu hướng khác biệt về DFS dựa trên phác đồ điều trị (CAPOX: HR = 1,02; 80% CI = 0,88 – 1,17; P = 0,087 và FOLFOX: HR = 1,42; 80% CI = 1,19 – 1,70; P = 0,894) [21].
Khoảng 20% đến 25% bệnh nhân giai đoạn II và 10% đến 15% bệnh nhân giai đoạn III MSI-H khiếm khuyết sửa chữa bắt cặp sai (dMMR) có ý nghĩa tiên lượng và có thể có ý nghĩa dự đoán đối với liệu pháp hỗ trợ [22-24]. Dữ liệu đáng kể cho thấy bệnh nhân dMMR giảm khả năng bệnh tái phát với một số nghiên cứu cho thấy tỷ lệ tái phát có thể thấp bằng một nửa so với các khối u có bộc lộ sửa chữa bắt cặp sai (pMMR) [25]. Hiệu quả tiên lượng dương này của dMMR dường như cũng rõ rệt hơn ở ung thư đại tràng giai đoạn II hơn giai đoạn III [22-24]. Một số nghiên cứu này cũng ủng hộ rằng dMMR cũng có thể là dấu hiệu dự đoán âm cho lợi ích của việc sử dụng fluoropyrimidine đơn chất, mặc dù một số nghiên cứu khác lại đề xuất ngược lại [22, 26-28].
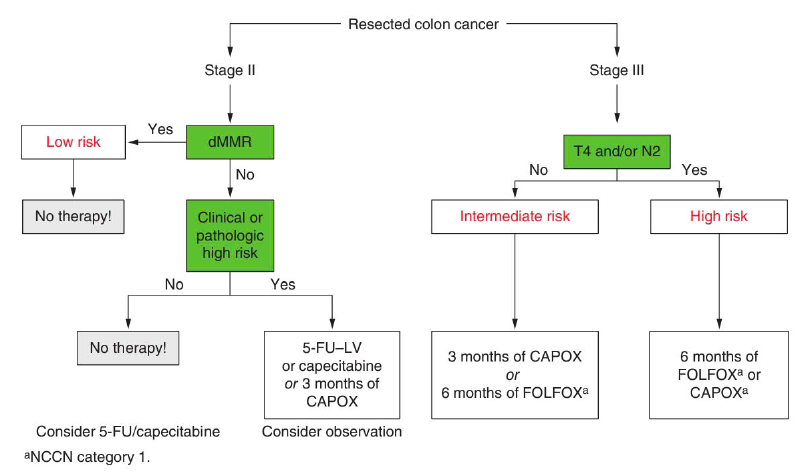
Irinotecan không có vai trò rõ ràng trong điều trị hỗ trợ. Ba thử nghiệm ngẫu nhiên pha III cho thấy sự cải thiện về DFS hoặc OS trong bối cảnh hỗ trợ. Hơn nữa, dữ liệu chưa hỗ trợ việc bổ sung bevacizumab, cetuximab hoặc panitumumab trong bối cảnh hỗ trợ [3, 6, 29-34].
TÀI LIỆU THAM KHẢO
[1]. Lieu C, Kennedy EB, Bergsland E, et al. Duration of oxaliplatin-containing adjuvant therapy for stage III colon cancer: ASCO clinical practice guideline. J Clin Oncol. 2019;37:1436-1447.
[2]. Kuebler JP, Wieand HS, O’Connell MJ, et al. Oxaliplatin combined with weekly bolus fluorouracil and leucovorin as surgical adjuvant chemotherapy for stage II and III colon cancer: results from NSABP C-07. J Clin Oncol. 2007;25:2198-2204.
[3]. de Gramont A, Van Cutsem E, Schmoll H-J, et al. Bevacizumab plus oxaliplatin-based chemotherapy as adjuvant treatment for colon cancer (AVANT): a phase 3 randomised controlled trial. The Lancet Oncol. 2012;13:1225-1233.
[4]. Cutsem EV, Labianca R, Bodoky G, et al. Randomized phase III trial comparing biweekly infusional fluorouracil/leucovorin alone or with irinotecan in the adjuvant treatment of stage III colon cancer: PETACC-3. J Clin Oncol. 2009;27: 3117-3125.
[5]. André T, Boni C, Mounedji-Boudiaf L, et al. Oxaliplatin, fluorouracil, and leucovorin as adjuvant treatment for colon cancer. N Engl J Med. 2004;350:2343-2351.
[6]. Alberts SR, Sargent DJ, Nair S, et al. Effect of oxaliplatin, fluorouracil, and leucovorin with or without cetuximab on survival among patients with resected stage III colon cancer: a randomized trial. JAMA. 2012;307:1383-1393.
[7]. Schmoll HJ, Twelves C, Sun W, et al. Effect of adjuvant capecitabine or fluorouracil, with or without oxaliplatin, on survival outcomes in stage III colon cancer and the effect of oxaliplatin on post-relapse survival: a pooled analysis of individual patient data from four randomised controlled trials. Lancet Oncol. 2014;15:1481-1492.
[8]. Schmoll HJ, Tabernero J, Maroun J, et al. Capecitabine plus oxaliplatin compared with fluorouracil/folinic acid as adjuvant therapy for stage III colon cancer: final results of the NO16968 randomized controlled phase III trial. J Clin Oncol. 2015;33:3733-3740.
[9]. Haller DG, Tabernero J, Maroun J, et al. Capecitabine plus oxaliplatin compared with fluorouracil and folinic acid as adjuvant therapy for stage III colon cancer. J Clin Oncol. 2011;29:1465-1471.
[10]. Grothey A, Sobrero AF, Shields AF, et al. Duration of adjuvant chemotherapy for stage III colon cancer. N Engl J Med. 2018;378:1177-1188.
[11]. Sobrero AF, Andre T, Meyerhardt JA, et al. Overall survival (OS) and long-term disease-free survival (DFS) of three versus six months of adjuvant (adj) oxaliplatin and fluoropyrimidine-based therapy for patients (pts) with stage III colon cancer (CC): final results from the IDEA (International Duration Evaluation of Adj chemotherapy) collaboration. J Clin Oncol. 2020;38:4004-4004.
[12]. Comparison of fluorouracil with additional levamisole, higher-dose folinic acid, or both, as adjuvant chemotherapy for colorectal cancer: a randomised trial. QUASAR Collaborative Group. Lancet. 2000;355:1588-1596.
[13]. Sargent D, Sobrero A, Grothey A, et al. Evidence for cure by adjuvant therapy in colon cancer: observations based on individual patient data from 20,898 patients on 18 randomized trials. J Clin Oncol. 2009;27:872-877.
[14]. Gill S, Loprinzi CL, Sargent DJ, et al. Pooled analysis of fluorouracil-based adjuvant therapy for stage II and III colon cancer: who benefits and by how much? J Clin Oncol. 2004;22: 1797-1806.
[15]. Figueredo A, Charette ML, Maroun J, et al. Adjuvant therapy for stage II colon cancer: a systematic review from the Cancer Care Ontario Program in evidence-based care’s gastrointestinal cancer disease site group. J Clin Oncol. 2004;22:3395-3407.
[16]. Efficacy of adjuvant fluorouracil and folinic acid in colon cancer. International Multicentre Pooled Analysis of Colon Cancer Trials (IMPACT) investigators. Lancet. 1995;345:939-944.
[17]. Tournigand C, Andre T, Bonnetain F, et al. Adjuvant therapy with fluorouracil and oxaliplatin in stage II and elderly patients (between ages 70 and 75 years) with colon cancer: subgroup analyses of the Multicenter International Study of Oxaliplatin, Fluorouracil, and Leucovorin in the Adjuvant Treatment of Colon Cancer trial. J Clin Oncol. 2012;30:3353-3360.
[18]. Shah MA, Renfro LA, Allegra CJ, et al. Impact of patient factors on recurrence risk and time dependency of oxaliplatin benefit in patients with colon cancer: analysis from modern-era adjuvant studies in the adjuvant colon cancer end points (ACCENT) database. J Clin Oncol. 2016;34:843-853.
[19]. Yothers G, O’Connell MJ, Allegra CJ, et al. Oxaliplatin as adjuvant therapy for colon cancer: updated results of NSABP C-07 trial, including survival and subset analyses. J Clin Oncol. 2011;29:3768-3774.
[20]. Benson AB, Venook AP, Al-Hawary MM, et al. NCCN guidelines insights: colon cancer, version 2.2018. J Natl Compr Canc Netw. 2018;16:359-369.
[21]. Iveson T, Sobrero AF, Yoshino T, et al. Prospective pooled analysis of four randomized trials investigating duration of adjuvant (adj) oxaliplatin-based therapy (3 vs 6 months {m}) for patients (pts) with high-risk stage II colorectal cancer (CC). J Clin Oncol. 2019;37:3501.
[22]. Sargent DJ, Marsoni S, Monges G, et al. Defective mismatch repair as a predictive marker for lack of efficacy of fluorouracil-based adjuvant therapy in colon cancer. J Clin Oncol. 2010;28:3219-3226.
[23]. Ribic CM, Sargent DJ, Moore MJ, et al. Tumor microsatellite-instability status as a predictor of benefit from fluorouracil-based adjuvant chemotherapy for colon cancer. N Engl J Med. 2003;349:247-257.
[24]. Klingbiel D, Saridaki Z, Roth AD, et al. Prognosis of stage II and III colon cancer treated with adjuvant 5-fluorouracil or FOLFIRI in relation to microsatellite status: results of the PETACC-3 trial. Ann Oncol. 2015;26:126-132.
[25]. Hutchins G, Southward K, Handley K, et al. Value of mismatch repair, KRAS, and BRAF mutations in predicting recurrence and benefits from chemotherapy in colorectal cancer. J Clin Oncol. 2011;29:1261-1270.
[26]. Sinicrope FA, Mahoney MR, Smyrk TC, et al. Prognostic impact of deficient DNA mismatch repair in patients with stage III colon cancer from a randomized trial of FOLFOX-based adjuvant chemotherapy. J Clin Oncol. 2013;31:3664-3672.
[27]. Kim JE, Hong YS, Kim HJ, et al. Defective mismatch repair status was not associated with DFS and OS in stage II colon cancer treated with adjuvant chemotherapy. Ann Surg Oncol. 2015;22(suppl 3):S630-S637.
[28]. Bertagnolli MM, Redston M, Compton CC, et al. Microsatellite instability and loss of heterozygosity at chromosomal location 18q: prospective evaluation of biomarkers for stages II and III colon cancer—a study of CALGB 9581 and 89803. J Clin Oncol. 2011;29:3153-3162.
[29]. Ychou M, Raoul JL, Douillard JY, et al. A phase III randomised trial of LV5FU2 + irinotecan versus LV5FU2 alone in adjuvant high-risk colon cancer (FNCLCC Accord02/FFCD9802). Ann Oncol. 2009;20:674-680.
[30]. Van Cutsem E, Labianca R, Bodoky G, et al. Randomized phase III trial comparing biweekly infusional fluorouracil/leucovorin alone or with irinotecan in the adjuvant treatment of stage III colon cancer: PETACC-3. J Clin Oncol. 2009;27:3117-3125.
[31]. Saltz LB, Niedzwiecki D, Hollis D, et al. Irinotecan fluorouracil plus leucovorin is not superior to fluorouracil plus leucovorin alone as adjuvant treatment for stage III colon cancer: results of CALGB 89803. J Clin Oncol. 2007;25:3456-3461.
[32]. Taieb J, Tabernero J, Mini E, et al. Oxaliplatin, fluorouracil, and leucovorin with or without cetuximab in patients with resected stage III colon cancer (PETACC-8): an open-label, randomised phase 3 trial. Lancet Oncol. 2014;15:862-873.
[33]. Dasari A, Messersmith WA. Should we perform a new adjuvant trial with bevacizumab? Curr Colorectal Cancer Rep. 2011;7:218.
[34]. Allegra CJ, Yothers G, O’Connell MJ, et al. Bevacizumab in Stage II-III colon cancer: 5-year update of the National Surgical Adjuvant Breast and Bowel Project C-08 trial. J Clin Oncol. 2013;31:359-364.
BS. TRẦN KIẾN BÌNH

