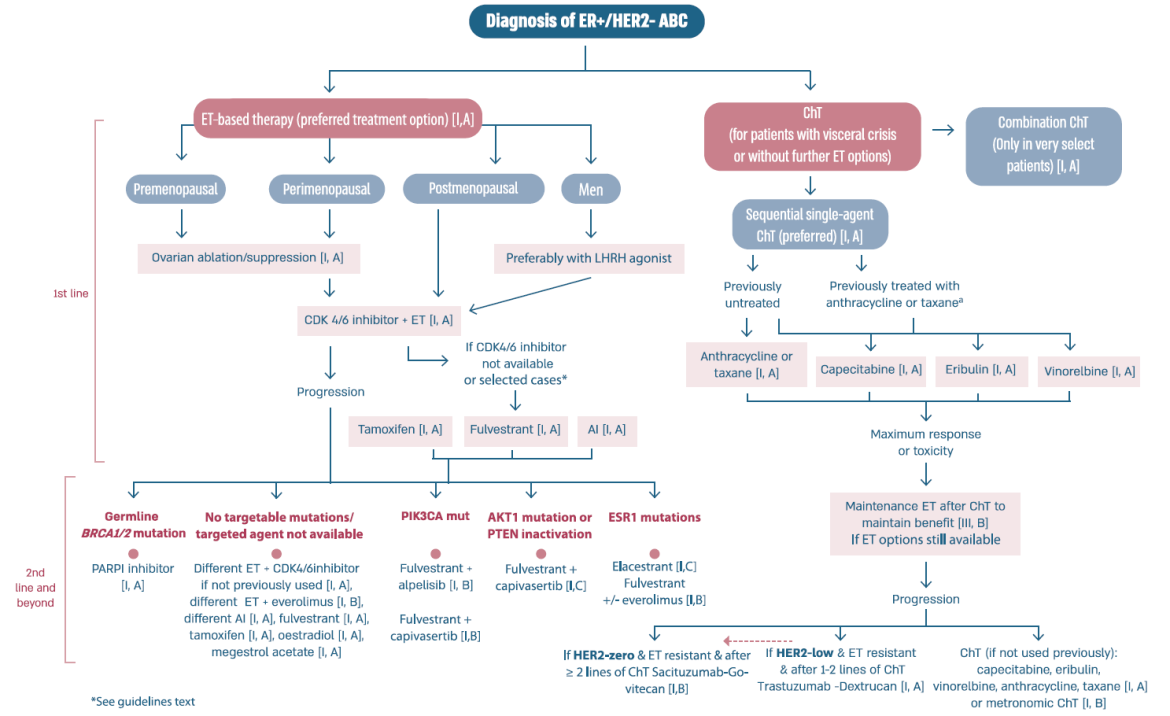
Liệu pháp dựa trên nội tiết (ET) là lựa chọn ưu tiên cho bệnh nhân (BN) có thụ thể estrogen dương tính (ER+), ngay cả khi có sự hiện diện của di căn tạng, ngoại trừ khủng hoảng tạng. (LoE/GoR: I/A) (93%)
Nhiều thử nghiệm trong ung thư vú tiến triển (ABC) ER+ không bao gồm phụ nữ tiền mãn kinh. Mặc dù vậy, hội đồng khuyến cáo rằng những phụ nữ trẻ mắc ABC nên được ức chế hoặc hủy chức năng buồng trứng (OFS/OFA) đầy đủ và sau đó được điều trị theo cách tương tự như những phụ nữ hậu mãn kinh với các tác nhân ET có hoặc không có các liệu pháp nhắm trúng đích. (LoE/GoR: Expert opinion/A) (95%)
Những thử nghiệm trong tương lai khám phá các chiến lược mới dựa trên nội tiết nên được thiết kế để cho phép cả phụ nữ tiền và hậu mãn kinh, cũng như nam giới. (LoE/GoR: Expert opinion/A) (92%)
Đối với phụ nữ tiền mãn kinh, những người đã quyết định điều trị ET, OFS/OFA kết hợp với bổ sung liệu pháp dựa trên ET là lựa chọn ưu tiên. (LoE/GoR: I/A) (93%)
OFA bằng phẫu thuật nội soi cắt bỏ buồng trứng hai bên đảm bảo ức chế estrogen và tránh thai dứt điểm, tránh khả năng bùng phát khối u ban đầu với chất chủ vận LHRH (LHRHa) và có thể tăng khả năng thỏa tiêu chí cho các thử nghiệm lâm sàng. BN cần được thông báo về các lựa chọn OFS/OFA và quyết định nên được đưa ra tùy theo từng trường hợp cụ thể. (LoE/GoR: Expert opinion/C) (91%)
Tác nhân Tamoxifen đơn lẻ là lựa chọn nội tiết duy nhất có sẵn dành cho phụ nữ tiền mãn kinh bị suy giảm OFS/OFA nhưng hội đồng tin rằng đây là lựa chọn kém hiệu quả. (LoE/GoR: I/D) (92%)
Tác nhân nội tiết bước 1 được ưu tiên tùy thuộc vào loại và thời gian sử dụng ET cũng như khoảng thời gian đã trôi qua kể từ khi kết thúc ET hỗ trợ; đó có thể là chất ức chế Aromatase (AI), Tamoxifen hoặc Fulvestrant cho phụ nữ tiền và chu mãn kinh đã OFS/OFA, nam giới (tốt nhất là dùng LHRHa) và phụ nữ hậu mãn kinh. (LoE/GoR: I/A) (84%)
Thuốc ức chế CDK4/6 kết hợp với ET là tiêu chuẩn chăm sóc cho BN ABC ER+/HER2-, vì làm tăng đáng kể OS cũng như PFS và duy trì hoặc cải thiện chất lượng cuộc sống. Thuốc ức chế CDK4/6 (CDK4/6i) có thể được kết hợp với AI hoặc với Fulvestrant (Tamoxifen không thể kết hợp với Ribociclib nhưng có thể kết hợp với Abemaciclib hoặc Palbociclib, trong ABC de novo hoặc tái phát, ở bước 1 hoặc bước 2 và trong các trường hợp đề kháng nguyên phát hay thứ phát (như được định nghĩa theo hướng dẫn ABC). Khuyến cáo này áp dụng cho phụ nữ hậu mãn kinh, ở phụ nữ tiền mãn kinh kết hợp với LHRHa và ở nam giới tốt nhất là kết hợp với LHRHa. (LoE/GoR: I/A) (97%)
Điểm ESMO – MCBS đối với việc sử dụng CDK4/6i kết hợp với ET cho BN ABC khác nhau tùy theo bối cảnh và loại thuốc. Với dữ liệu hiện có và theo dõi, các thuốc bao gồm như sau:
• Ribociclib + ET bước 1 cho tiền mãn kinh; ESMO – MCBS: 5.
• Ribociclib + AI bước 1 cho hậu mãn kinh; ESMO – MCBS: 4.
• Palbociclib + AI bước 1: ESMO – MCBS: 3.
• Abemaciclib + AI bước 1; ESMO – MCBS: 3.
• Palibociclib + Fulvestrant bước 2; ESMO – MCBS: 4.
• Ribociclib + Fulvestrant (bước 1, 2); ESMO – MCBS: 4.
• Abemaciclib + Fulvestrant bước 2; ESMO – MCBS: 4.
Đáng chú ý, ba tác nhân CDK4/6i chưa được so sánh đối đầu trực tiếp trong một thử nghiệm lâm sàng. (LoE/GoR: I/A) (89%)
Thử nghiệm SONIA đã cố gắng trả lời cho câu hỏi liệu có nên dùng CDK4/6i (90% Palibociclib) kết hợp với ET như liệu pháp bước 1 hoặc bước 2 cho ABC ER+/HER2- hay không. Không thấy có sự khác biệt có ý nghĩa thống kê nào cho PFS 2 (tiêu chí chính), OS cũng như QoL, tại thời điểm theo dõi 37 tháng. Hiện tại vẫn chưa biết liệu kết quả có giống như vậy đối với Ribociclib hoặc Abemaciclib hay không. Xét về dữ liệu tổng thể (lợi ích OS và các lựa chọn bước 2 khác nhau), hội đồng vẫn xem xét việc sử dụng CDK4/6i + ET là liệu pháp bước 1 tiêu chuẩn cho phần lớn BN ABC ER+/HER2-. Tuy nhiên, dựa trên kết quả từ thử nghiệm SONIA, vẫn chấp nhận cho việc lựa chọn ET đơn độc làm liệu pháp bước 1 cho những BN được chọn lọc (gánh nặng bệnh thấp, DFI dài, sở thích của BN, hạn chế về khả năng tiếp cận) với phân nhóm ABC này. (LoE/GoR: I/A) (93%)
Không có dữ liệu so sánh giữa sự kết hợp CDK4/6i và ET với ET đơn độc như một liệu pháp duy trì sau hóa trị. Cả hai lựa chọn đều được chấp nhận. (LoE/GoR: Expert opinion/B) (75%)
Việc sử dụng CDK4/6i + ET sau khi tiến triển với CDK4/6i đã được đánh giá trong các thử nghiệm pha 2 nhỏ, với những kết quả trái ngược nhau và không được khuyến cáo thường quy trong thực hành lâm sàng, ngoài thử nghiệm lâm sàng. (LoE/GoR: Expert opinion/D) (91%)
Các thử nghiệm so sánh sự kết hợp ET + tác nhân nhắm trúng đích với hóa trị đơn độc, trong bối cảnh bước 1 và các bước sau, đang được tiến hành và một số đã được báo cáo. Trong thử nghiệm PEARL, mặc dù có một vài hạn chế, ET + Palbociclib và Capecitabine mang lại hiệu quả tương tự, trong khi hồ sơ độc tính lại khác nhau. Trong thử nghiệm Young – PEARL, trên phụ nữ tiền mãn kinh, ET + Palbociclib vượt trội hơn Capecitabine về PFS. Do lợi ích sống còn đáng kể được thấy với ET + CDK4/6i ở bước 1, chưa từng thấy trước đây với hóa trị, sự kết hợp này nên được coi là tiêu chuẩn chăm sóc cho liệu pháp bước 1 đối với ABC ER+/HER-, dành cho phụ nữ tiền và chu mãn kinh với OFS/OFA, nam giới (tốt nhất là dùng LHRHa) và phụ nữ hậu mãn kinh. (LoE/GoR: I/A) (96%)
Trong thử nghiệm RIGHT Choice, sự kết hợp Ribociclib + AI (+ LHRHa ở phụ nữ tiền mãn kinh) được so sánh với hóa trị kết hợp (Docetaxel + Capecitabine, Paclitaxel + Gemcitabine hoặc Capecitabine + Vinorelbine) là liệu pháp bước 1 cho phụ nữ ABC tiền/chu mãn kinh ER+/HER2- với “bệnh tiến triển trên lâm sàng” được định nghĩa là: di căn tạng có triệu chứng, bệnh tiến triển nhanh hoặc tổn thương tạng sắp xảy ra, bệnh có triệu chứng rõ rệt mà không có di căn tạng, nhưng với bilirubin < 1,5xULN (do đó không phải trong khủng hoảng gan được định nghĩa theo Hướng dẫn ABC). Nhánh ET + CDK4/6i mang lại lợi ích 12 tháng về PFS, với ORR và thời gian bắt đầu đáp ứng tương tự ở cả hai nhánh, nhưng hồ sơ độc tính tốt hơn đáng kể.
Những kết quả này củng cố vị trí của ET + CDK4/6i như là tiêu chuẩn chăm sóc bước 1 cho phần lớn BN ABC ER+/HER2-, bao gồm cả những người “bệnh tiến triển trên lâm sàng”. (LoE/GoR: I/A) (95%)
Mặc dù thử nghiệm chỉ được thực hiện ở phụ nữ tiền/chu mãn kinh, nhưng hội đồng tin rằng kết quả cũng áp dụng được cho phụ nữ hậu mãn kinh và nam giới có cùng đặc điểm bệnh. (LoE/GoR: Expert opinion/B) (95%)
Việc bổ sung Everolimus vào AI là một lựa chọn hợp lý cho một số BN [OFS/OFA cho phụ nữ tiền và chu mãn kinh, nam giới (ưu tiên LHRHa) và phụ nữ hậu mãn kinh] trước đây đã từng sử dụng hoặc chưa từng sử dụng ET (trong trường hợp không có CDK4/6i), vì cho thấy kéo dài đáng kể PFS, mặc dù không có bằng chứng về lợi ích OS đáng kể. Điểm ESMO – MCBS 1.1: 2. (LoE/GoR: I/B) (88%)
Tamoxifen hoặc Fulvestrant cũng có thể được phối hợp với Everolimus. (LoE/GoR: II/B) (80%)
Cần phòng ngừa đầy đủ bằng nước súc miệng steorid, theo dõi chặt chẽ và điều trị chủ động các tác dụng phụ là điều cần thiết, đặc biệt ở BN lớn tuổi được điều trị bằng Everolimus vì tỉ lệ tử vong do độc tính tăng lên được báo cáo trong thử nghiệm Bolero – 2. (LoE/GoR: I/B) (97%)
Everolimus không nên được sử dụng sau khi bệnh tiến triển với nó, ngoài thử nghiệm lâm sàng. (LoE/GoR: NA/E) (74%)
Alpelisib với Fulvestrant là một lựa chọn điều trị cho BN [OFS/OFA cho phụ nữ tiền và chu mãn kinh, nam giới (ưu tiên LHRHa) và phụ nữ hậu mãn kinh] có khối u đột biến PIK3CA (ở exon 9 hoặc 20), đã điều trị AI trước đó và có nồng độ HbA1c phù hợp, vì mang lại lợi ích PFS trung vị khoảng 5 tháng, không có lợi ích OS có ý nghĩa thống kê. Quyết định sử dụng Alpelisib nên xem xét các tiêu chí bao gồm/loại trừ trong nghiên cứu Solar – 1 (tức là bệnh đái tháo đường đã có từ trước và HbA1c cơ bản), cũng như hồ sơ độc tính của Alpelisib. Điểm ESMO – MCBS 1.1: 2. (LoE/GoR: I/A) (96%)
Rất ít BN điều trị CDK4/6i trước đó được đưa vào Solar – 1. Tuy nhiên, một nghiên cứu đoàn hệ không ngẫu nhiên (ByLieve) dường như chỉ ra rằng Alpelisib vẫn giữ được hiệu quả nếu sử dụng sau một CDK4/6i. Xét về mức độ lợi ích của OS được thấy với ET + CDK4/6i, tiếp cận này được coi là tiêu chuẩn chăm sóc cho liệu pháp bước 1 và ET (Fulvestrant hoặc AI) + Alpelisib nên được dành cho bối cảnh bước 2, trong trường hợp khối u có đột biến PIK3CA. (LoE/GoR: I/B) (93%)
BN dùng Alpelisib kết hợp với ET đối với ABC có đột biến PIK3CA nên được hướng dẫn dùng thuốc kháng histamine không gây buồn ngủ hàng ngày để phòng ngừa phát ban khi bắt đầu điều trị. Có thể ngừng thuốc kháng histamine sau 4 tuần, vì nguy cơ phát ban chủ yếu xảy ra trong 2 tuần đầu điều trị. (LoE/GoR: I/B) (93%)
Elacestrant, một chất làm suy giảm thụ thể estrogen chọn lọc (SERD) đường uống, đã được phê duyệt là liệu pháp bước 2/3 cho BN ABC ER+/HER2- có đột biến ESR1, dựa trên thử nghiệm ngẫu nhiên pha III chứng minh lợi ích PFS trung vị 1,9 tháng (HR: 0,546). Ưu điểm này đáng chú ý nhất ở BN đã điều trị CDK4/6i trước đó trong hơn 6 tháng. Nếu có sẵn, Elscestrant đơn chất là một lựa chọn cho BN trong bối cảnh bước 2/3 có đột biến ESR1. Điểm ESMO – MCBS 1.1: 3. (LoE/GoR: I/C) (81%)
Cabivasertib, một chất ức chế AKT, kết hợp với Fulvestrant được so sánh với giả dược cộng Fulvestrant, ở BN [OFS/OFA cho phụ nữ tiền và chu mãn kinh, nam giới (ưu tiên LHRHa) và phụ nữ hậu mãn kinh] ABC ER+/HER2-, với 1 hoặc 2 bước ET trước đó và có 1 bước hoặc không có hóa trị trước đó cho bệnh di căn; tái phát hoặc tiến triển trong khi đang hoặc < 12 tháng kể từ khi kết thúc AI hỗ trợ hay tiến triển khi đang dùng AI trước đó đối với ABC là bắt buộc; khoảng 70% số BN nhận CDK4/6i trước đó. Kết quả cho thấy lợi ích PFS trung vị 3,6 tháng (HR: 0,60) trên toàn bộ dân số và lợi ích PFS trung vị 4,2 tháng (HR: 0,50) ở nhóm dân số có thay đổi con đường AKT (tức là biến đổi PIK3CA và/hoặc PTEN và/hoặc AKT1). Kết quả OS vẫn còn đang theo dõi. Các tác dụng phụ trên đường tiêu hóa, chủ yếu là tiêu chảy (72%), đã được ghi nhận.
Dựa trên những kết quả này, khi được phê duyệt, Capevasertib được thêm vào Fulvestrant có thể sử dụng như một lựa chọn điều trị trên BN ABC ER+/HER2- đề kháng nội tiết có thay đổi con đường AKT (tức là biến đổi PIK3CA và/hoặc PTEN và/hoặc AKT1). Điểm ESMO – MCBS 1.1: 3
Vẫn chưa biết hiệu quả của Capivasertib sau một liên hợp kháng thể – thuốc (ADC) chẳng hạn như T-DXd hay Sacituzumab govitecan hoặc so sánh với Everolimus hoặc Alpelisib như thế nào. (LoE/GoR: I/B) (95%)
Sacituzumab govitecan được so sánh với HT theo lựa chọn của bác sĩ, trên BN ER+/HER2-, đã được điều trị trước với ít nhất một bước ET, Taxane và CDK4/6i trong bất kỳ bối cảnh nào và tối thiểu 2, nhưng không nhiều hơn 4 bước HT cho bệnh di căn (60% BN đã nhận 3 bước HT hoặc nhiều hơn). Kết quả cho thấy sự cải thiện 1,5 tháng về PFS trung vị và 3,2 tháng về OS trung vị, cả ở nhóm HER2 thấp và HER2-. Không có hồ sơ an toàn nào mới được quan sát thấy. Giáo dục, điều trị dự phòng và quản lý sớm các tác dụng phụ, đặc biệt là tiêu chảy và buồn nôn/nôn ói vẫn rất quan trọng. Lợi ích về mặt OS được thấy ở nhóm BN đã được điều trị nhiều bước trước đó đã khiến Sacituzumab govitecan trở thành một lựa chọn điều trị cho nhóm BN này, Điểm ESMO – MCBS 1.1: 4. (LoE/GoR: I/B) (95%)
Datopotamab deruxtecan (Dato-DXd) được so sánh với HT theo lựa chọn của bác sĩ (chủ yếu là Eribulin), trên BN ABC ER+/HER2-, đã được điều trị trước với 1-2 bước HT trong bối cảnh không thể phẫu thuật hoặc di căn và đã tiến triển với ET và không phù hợp với ET và đã dẫn đến cải thiện 2 tháng về PFS trung vị (HR 0,63). Kết quả từ kết cục chính kép OS vẫn đang chờ đợi. Viêm miệng, các biến cố ở mắt (chủ yếu là khô mắt), buồn nôn, nôn ói và mệt mỏi là những tác dụng phụ thường gặp nhất. Bệnh phổi kẽ (ILD)/viêm phổi không phổ biến. Giáo dục và các biện pháp phòng ngừa (như súc miệng, thuốc chống nôn) được khuyến cáo. Do sự khác biệt khiêm tốn về PFS, không có dữ liệu về OS ở thời điểm hiện tại, hồ sơ độc tính và tính sẵn có của các lựa chọn điều trị khác, Dato-DXd chưa thể được khuyến cáo sử dụng trong thực hành lâm sàng thường quy (LoE/GoR: I/D) (66%)
Trastuzumab deruxtecan (T-DXd) được so sánh với HT do bác sĩ lựa chọn, trên BN ABC có HER2 thấp, đã được điều trị 1-2 bước HT trong bối cảnh di căn và ER+ được xem là đề kháng nội tiết và mang lại lợi ích 6,1 tháng về OS trung vị và 4,6 tháng về PFS trung vị, khiến trở thành một lựa chọn điều trị được ưu tiên trong bối cảnh này. Điểm ESMO – MCBS 1.1: 4
Điều trị bằng T-DXd có liên quan đến ILD/viêm phổi (bao gồm cả tử vong do độc tính), tăng độc tính trên đường tiêu hóa và mệt mỏi. ILD/Viêm phổi có thể gây tử vong và cần được theo dõi hình ảnh học tích cực bằng chụp cắt lớp vi tính không cản quang và quản lý phù hợp. Buồn nôn và nôn ói cần được điều trị dự phòng đầy đủ. (LoE/GoR: I/A) (100%)
Có rất ít dữ liệu liên quan đến trình tự sử dụng ADC tốt nhất cho ABC ER+/HER2 thấp. Dựa trên dân số được điều trị và kết quả thử nghiệm T-DXd và Sacituzumab govitecan, hội đồng tin rằng T-DXd nên được sử dụng sớm hơn Sacituzumab govitecan. (LoE/GoR: Expert opinion/B) (95%)
Sự kết hợp giữa AI không steroid và Fulvestrant như liệu pháp bước 1 cho BN hậu mãn kinh đã cải thiện đáng kể về cả PFS và OS so với AI đơn độc trong một thử nghiệm pha III và không có lợi ích trong thử nghiệm thứ hai với thiết kế tương tự. Đáng chú ý, liều Fulvestrant dưới mức tối ưu đã được sử dụng trong nghiên cứu chứng minh được lợi ích. Phân tích dưới nhóm cho thấy lợi ích chỉ giới hạn trên BN chưa từng điều trị với ET hỗ trợ (Tamoxifen).
Dựa trên những dữ liệu này, kết hợp ET có thể được chỉ định cho một số BN ABC chưa điều trị ET trước đó, khi đó sẽ không sử dụng CDK4/6i. Điểm ESMO – MCBS 1.1: 2
Không có dữ liệu so sánh giữa sự kết hợp này và một CDK4/6i với ET. (LoE/GoR: II/D) (Yes: 38%; No: 60%; Abstain: 2%)
Trình tự tối ưu của liệu pháp dựa trên nội tiết là không chắc chắn. Điều này phụ thuộc vào các tác nhân đã được sử dụng trước đó [trong bối cảnh (tân) hỗ trợ hoặc tiến triển], thời gian đáp ứng với các tác nhân đó, gánh nặng bệnh, sở thích của BN và tính sẵn có. (LoE/GoR: I/A) (100%)
Các lựa chọn điều trị cho bệnh ER+ ở các bước sau bước 2 bao gồm các tác nhân đơn chất chưa được sử dụng trước đó (NSAI, SAI, Tamoxifen, Fulvestrant, Megesterol acetate, Estrogen liều thấp). Abemaciclib đơn độc cũng là một lựa chọn tiềm năng. Việc sử dụng lại một tác nhân mà bệnh đã tiến triển trước đó cho BN, sau khi có đáp ứng ban đầu, đôi khi được xem xét, nhưng không có dữ liệu chắc chắn nào hỗ trợ cho tiếp cận này. Điều này áp dụng cho phụ nữ tiền và chu mãn kinh với OFS/OFA, nam giới (tốt nhất là dùng LHRHa) và phụ nữ hậu mãn kinh. (LoE/GoR: II/B) (98%)
Kết hợp HT và ET không cho thấy lợi ích sống còn và không nên chỉ định ngoài thử nghiệm lâm sàng. (LoE/GoR: II/D) (100%)
Điều trị ET sau HT (ET duy trì) để duy trì lợi ích là một lựa chọn hợp lý, mặc dù chưa được đánh giá đúng trong các thử nghiệm ngẫu nhiên. (LoE/GoR: III/B) (88%)
TÀI LIỆU THAM KHẢO
Cardoso F., Paluch-Shimon S., Schumacher-Wulf E. et al (2024), 6th and 7th International consensus guidelines for the management of advanced breast cancer (ABC guidelines 6 and 7), The Breast 76 (2024) 103756.
BS. TRẦN KIẾN BÌNH