Tác giả: David Henry, MD
Lược dịch: BS. Nguyễn Minh Nhật – BS. Trần Trung Bách
Nhờ những tiến bộ trong sàng lọc, nhiều bệnh nhân ung thư vú, phổi và đại trực tràng đã được chẩn đoán sớm và có cơ hội điều trị hiệu quả bằng phẫu thuật triệt căn. Sau phẫu thuật, giai đoạn lâm sàng-mô bệnh học thường là yếu tố quyết định trường hợp nào cần được chỉ định điều trị bổ trợ. Một số chỉ số có giá trị tiên lượng kết cục xấu hơn ở những người bệnh không được điều trị bổ trợ so với khi được điều trị bổ trợ. Tuy nhiên, bạn có thường xuyên nhận được câu hỏi: “Điều trị này liệu có hiệu quả với tôi?”. Tất nhiên, câu trả lời của chúng ta thường là “Chúng tôi không thể khẳng định được! Sau mổ, chúng ta không còn thấy bằng chứng của bệnh, sau điều trị bổ trợ có thể cũng vậy, do đó, chúng tôi không thể nói liệu trình bổ trợ chắc chắn có hiệu quả với trường hợp của bạn”.
Trong thực hành lâm sàng ung thư những năm gần đây, DNA tự do ngoại bào (cell-free DNA) nói chung và DNA khối u lưu hành (circulating tumor DNA – ctDNA) nói riêng đã nổi lên như một dấu ấn sinh học đầy hứa hẹn trong theo dõi bệnh nhân trước, trong và sau điều trị. Lấy ví dụ trong ung thư đại tràng, hãy quan sát những dữ liệu dưới đây.
Hầu hết bệnh nhân ung thư đại tràng giai đoạn II sau phẫu thuật không cần điều trị bổ trợ bằng hóa trị. Tuy nhiên, khoảng 15-20% bệnh nhân còn lại có tồn dư bệnh sau phẫu thuật. Việc xác định nhóm bệnh nhân này để điều trị bổ trợ có thể giúp giảm nguy cơ tái phát. Năm 2022, thử nghiệm DINAMIC1 đăng trên The New England Journal of Medicine đã phân tích giá trị của ctDNA sau phẫu thuật ung thư đại tràng giai đoạn II. 455 bệnh nhân được chia ngẫu nhiên vào 2 nhóm với tỷ lệ 2:1: nhóm 1 (N=294) được chỉ định điều trị bổ trợ dựa theo kết quả của ctDNA và nhóm 2 (n=147) điều trị bổ trợ theo những đặc điểm lâm sàng-mô bệnh học tiêu chuẩn. Ở nhóm 1, các bệnh nhân sẽ được điều trị bổ trợ nếu ctDNA dương tính và ngược lại, theo dõi nếu ctDNA âm tính. Trong nhóm ctDNA dương tính, sau khi kết thúc liệu trình bổ trợ, 80% bệnh nhân có ctDNA trở về âm tính. Tỷ lệ sống thêm không tái phát (recurrence-free survival) 3 năm ở nhóm ctDNA dương tính có điều trị bổ trợ là 84,6% và nhóm ctDNA âm tính không được điều trị bổ trợ là 92,5%.
Thử nghiệm PEGASUS2 phân tích giá trị của ctDNA sau phẫu thuật ở 135 bệnh nhân ung thư đại tràng giai đoạn III và giai đoạn II nguy cơ cao. Kết quả cho thấy việc lựa chọn điều trị khởi đầu, leo thang, xuống thang phác đồ hóa trị bổ trợ (theo dõi/capecitabine đơn trị/CAPOX (capecitabine, oxaliplatin)/FOLFIRI (irinotecan, leucouvorin, 5-FU) có thể dựa vào tình trạng ctDNA dương tính hay âm tính, từ đó giảm độc tính không cần thiết so với điều trị hóa trị tiêu chuẩn.
Nghiên cứu GALAXY3 trên 2280 bênh nhân ung thư đại trực tràng cho thấy ctDNA sau phẫu thuật có thể là thông số có giá trị tốt cho quyết định điều trị hóa trị bổ trợ. Ngoài ra, thử nghiệm lâm sàng pha III ASCOLT4 đã chứng minh ctDNA dương tính trong vòng 1 năm sau điều trị phẫu thuật kết hợp với hóa trị bổ trợ là yếu tố tiên lượng độc lập cho tình trạng tát phát bệnh.
Nồng độ của ctDNA trong máu ngoại vi thường rất thấp (< 0,1-1% cfDNA), đặc biệt là sau phẫu thuật hay điều trị hóa chất dẫn đầu. Việc phát hiện các biến thể có thể âm tính giả do sai số của phương pháp xét nghiệm hoặc do các tín hiệu không phải từ khối u của các dòng tế bào máu. Do vậy, làm thế nào để xác định ctDNA là dương tính hay âm tính? ctDNA được định nghĩa là dương tính khi tần số allen biến thể (variant allele frequency – VAF) lớn hơn hoặc bằng giới hạn phát hiện (limit of detection – LOD) của xét nghiệm. Trong đó, VAF được định nghĩa là phần trăm phân tử đột biến trên tổng số phân tử “hoang dã” (wild-type) tại một vị trí cụ thể trong hệ gen: VAF (%) = Nmut/(Nmut+NWT) x 100%. Bên cạnh đó, LOD là giới hạn thấp nhất của dấu ấn cần phân tích mà xét nghiệm có thể phát hiện được nhưng chưa định lượng được, gía trị LOD do nhà sản xuất cung cấp.5
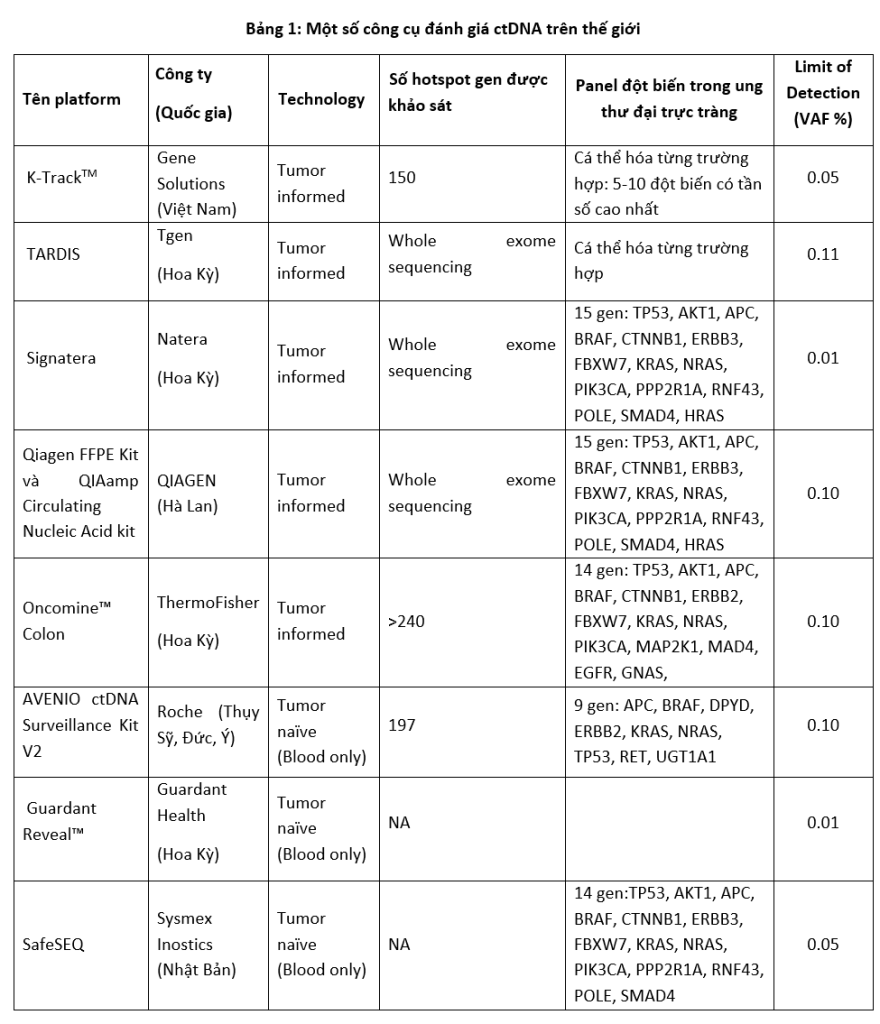
Ngoài ra, việc chọn ra nhóm các gen để khảo sát VAF là một việc làm quan trọng, tùy thuộc vào từng loại ung thư và thiết kế của bộ xét nghiệm, tuy nhiên nhìn chung vẫn dựa trên 2 phương pháp chính: panel cố định và cá thể hóa. Trong phương pháp chọn panel cố định, các gen trong panel thường là những gen có tần suất đột biến cao trên bản đồ gen của quần thể. Với phương pháp chọn panel gen cá thể hóa (tumor-guided personalized), trên mỗi bệnh nhân sẽ chọn ra một vài đột biến có tần suất cao nhất. Một số nền tảng đánh giá ctDNA trong ung thư đại tràng đang được sử dụng trên thế giới và VAF của chúng được trình bày trong Bảng 1.
Nhìn chung, những nghiên cứu trên có thể cho bạn câu trả lời cho câu hỏi: ”Có cần điều trị bổ trợ hay không? Điều trị có hiệu quả gì hay không?”. Các thử nghiệm tương tự đang được thực hiện trên các bệnh nhân ung thư phổi và ung thư vú. Các nghiên cứu trên khá thú vị, tuy nhiên chúng ta vẫn cần những thử nghiệm tiếp theo để quyết định nhóm bệnh nhân nào cần điều trị bổ trợ và cần làm gì khi có kết quả ctDNA dương tính hoặc âm tính sau phẫu thuật triệt căn.
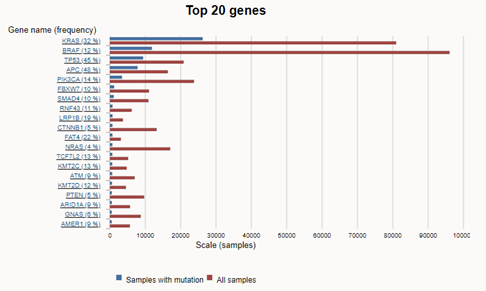
Hình 1: 20 đột biến gen thường gặp nhất trong ung thư đại tràng theo COSMIC v99 28/11/2023 (https://cancer.sanger.ac.uk/cosmic)6
TÀI LIỆU THAM KHẢO
1. Tie J, Cohen JD, Lahouel K, et al. Circulating Tumor DNA Analysis Guiding Adjuvant Therapy in Stage II Colon Cancer. New England Journal of Medicine. 2022;386(24):2261-2272. doi:10.1056/NEJMoa2200075
2. Lonardi S, Montagut C, Pietrantonio F, et al. The PEGASUS trial: Post-surgical liquid biopsy-guided treatment of stage III and high-risk stage II colon cancer patients. Journal of Clinical Oncology. 2020;38:TPS4124-TPS4124. doi:10.1200/JCO.2020.38.15_suppl.TPS4124
3. Nakamura Y, Kotani D, Saori M, et al. 558MO Circulating tumor (ct)DNA as a prognostic biomarker in patients (pts) with resected colorectal cancer (CRC): An updated 24 months (mos) disease-free survival (DFS) analysis from GALAXY study (CIRCULATE-Japan). Annals of Oncology. 2023;34:S415-S416. doi:10.1016/j.annonc.2023.09.1749
4. Day D, Starus A, Gebski V, et al. 586P Minimal residual disease (MRD) detection using a tumor naïve circulating tumor DNA (ctDNA) assay in patients (pts) with resected colorectal cancer (CRC) in the phase III ASCOLT trial. Annals of Oncology. 2023;34:S426-S427. doi:10.1016/j.annonc.2023.09.1777
5. Kroll M. Protocols for Determination of Limits of Detection and Limits of Quantitation: Approved Guideline. Published online January 1, 2004. Accessed January 9, 2024. https://www.academia.edu/110674305/Protocols_for_Determination_of_Limits_of_Detection_and_Limits_of_Quantitation_Approved_Guideline
6. COSMIC – Catalogue of Somatic Mutations in Cancer, version 99, released 28-NOV-2023. https://cancer.sanger.ac.uk/cosmic