Nội dung chính
GIỚI THIỆU
EGFR (Epidermal Growth Factor Receptor – thụ thể với yếu tố tăng trưởng biểu bì, tên gọi khác: ErbB-1 hay HER1 ở người) là 1 thành viên của gia đình các thụ thể yếu tố tăng trưởng biểu bì (EGF family) gồm 4 loại thụ thể Tyrosine Kinases đã được biết đến hiện nay: HER1 (EGFR – ErbB-1), HER2/neu (ErbB-2), HER3 và HER4.
Yếu tố tăng trưởng biểu bì cùng với các thụ thể của nó được phát hiện bởi nhà khoa học Stanley Cohen (Đại học Vanderbilt – Mỹ), đã mang lại cho ông cùng với Rita Levi-Motalcini (người phát hiện yếu tố tăng trưởng thần kinh – NGF) giải thưởng Nobel Y học danh giá năm 1986.


Suy giảm hoạt động dẫn truyền tín hiệu qua EGFR có mối liên quan với một số tình trạng bệnh lý như Alzheimer, ngược lại, các bất thường gây ra tăng bộc lộ hay hoạt động quá mức của EGFR đã được chứng minh kết hợp với sự phát sinh và tiến triển của nhiều căn bệnh ung thư ở người.
1. Cấu trúc và chức năng của EGFR
EGFR có bản chất là 1 protein xuyên màng đơn chuỗi (Single-chain transmembrane protein) với: Phần ngoại bào mang vùng gắn với các phối tử (Ligants) đặc hiệu – yếu tố tăng trưởng biểu bì và TGFα (Transforming Growth Factor α), 1 đoạn ngắn xuyên màng và phần nội bào được tạo nên mới vùng hoạt tính tyrosine kinase và vùng phosphoryl hoá đầu tận C. EGFR được mã hoá bởi gen nằm trên nhiễm sắc thể số 7 ở người.
Gia đình các thụ thể EGF

Sau khi được gắn với các phối tử, EGFR chuyển đổi từ trạng thái đơn phân(Monomeric form) sang trạng thái hoạt hoá dạng nhị phân (Dimers) bằng cách ghép cặp với 1 phân tử EGFR khác (Homodimers) hoặc với 1 thành viên khác của gia đình EGF như HER2/neu (Heterodimer).
Ở trạng thái nhị phân, chức năng enzym tyrosine kinase ở phần nội bào của EGFR được kích hoạt, cụ thể là hiện tượng tự phosphoryl hoá một số acid amin tyrosine ở đầu tận C của EGFR xảy ra làm khởi phát dòng thác tín hiệu nội bào (Như chúng ta đã biết, cơ chế dẫn truyền tín hiệu nội bào được thực hiện chủ yếu thông qua hoạt hoá chuỗi các protein trên con đường dẫn truyền bằng phản ứng phosphoryl hoá).
Tín hiệu từ các yếu tố tăng trưởng (các phối tử) qua điểm tiếp nhận EGFR và được truyền đạt đến nhân tế bào qua một số con đường dẫn truyền tín hiệu, trong đó chủ yếu là con đường MAPK/ERK (Mitogen-Activated Protein Kinases/Extracellular signal-Regulated Kinases), AKT và JNK dẫn đến hiệu ứng kích thích tổng hợp DNA và tăng sinh tế bào cùng với ức chế con đường chết tế bào theo chương trình (Apoptosis).
2. EGFR và bệnh ung thư
Giả thuyết cho rằng rối loạn con đường tín hiệu EGFR có thể góp phần dẫn đến những biến đổi ác tính của tế bào bắt đầu được đặt ra từ những năm đầu thập kỷ 80 sau nghiên cứu của De Larco, Reynolds, Carlberg và cộng sự (1980). Nghiên cứu chỉ ra gen EGFR có vai trò tương tự với 1 oncogene v-erbB của virus gây bệnh hồng cầu ở gia cầm. V-erbB mã hoá cho protein xuyên màng có cấu trúc tương đồng chặt chẽ với EGFR bao gồm phần xuyên màng và phần nội bào tham gia vào cơ chế kích thích tăng sinh tế bào. Những nghiên cứu sau đó tiếp tục cho thấy các rối loạn dẫn đến tăng hoạt động dẫn truyền tín hiệu qua con đường EGFR xuất hiện trong một phổ rộng các bệnh lý ung thư ở người [1],[2]. Những rối loạn đó có thể do:
– Tăng bộc lộ EGFR trên màng tế bào do nhiều cơ chế khác nhau bao gồm tăng sản suất các phối tử của EGFR, tăng hoạt động phiên mã của gen EGFR, hiện tượng khuyếch đại gen (Tăng số lượng bản sao của gen trong nhân tế bào) EGFR.
– Đột biến gen EGFR dẫn đến tự hoạt hoá vùng tyrosine kinase.


Nhờ những hiểu biết sâu sắc hơn về các con đường dẫn truyền tín hiệu tăng sinh tế bào, vai trò của EGFR trong cơ chế bệnh sinh và tiến triển của ung thư ngày càng lộ diện rõ nét. Các con đường dẫn truyền tín hiệu nội bào khởi phát từ EGFR ở tế bào ung thư dẫn đến kích thích tăng sinh tế bào, ngăn cản tế bào đi vào cơ chế apoptosis – Chết tế bào theo chương trình (Con đường MAPK, AKT và JNK) và thúc đẩy hiện tượng di căn của tế bào ung thư khi kích thích con đường tín hiệu thông qua yếu tố tăng trưởng nội mô mạch máu (VEGF).
3. Cơ sở của các liệu pháp điều trị ung thư nhắm đích EGFR
Các liệu pháp nhắm đích EGFR đều nhằm mục tiêu ức chế hay cắt đứt các con đường tín hiệu nội bào kể trên ngay tại vị trí khởi phát → phân tử EGFR, theo một trong hai cơ chế chính:
– Ức chế chức năng tiếp nhận phối tử (Các yếu tố tăng trưởng EGF) của phần ngoại bào với các kháng thể đơn dòng (MAbs)
– Ức chế vùng hoạt tính tyrosine kinase của vùng EGFR nội bào với các thuốc EGFR TKIs (Tyrosine Kinase Inhibitors)
3.1. Các kháng thể đơn dòng (Monoclonal Antibodys – MAbs)
– Có ái lực mạnh với vị trí gắn phối tử ở phần ngoại bào EGFR → Cạnh tranh với các yếu tố tăng trưởng, ngăn cản chúng gắn và hoạt hoá EGFR, hay nói cách khác, không thể làm khởi phát các con đường tín hiệu nội bào thông qua EGFR, trong đó bao gồm các tín hiệu kích thích tăng sinh tế bào, ngăn cản chết tế bào theo chương trình và thúc đẩy hiện tượng xâm lấn, di căn của tế bào ung thư (qua VEGF).
– Phần hằng định Fc của kháng thể gắn vào thụ thể Fc trên bề mặt các tế bào hiệu ứng (Effector Cells) của hệ miễn dịch (VD: bạch cầu đơn nhân, đại thực bào). Quá trình tìm kiếm kháng nguyên tương ứng của kháng thể “vô tình” lôi cuốn và tập trung các tế bào miễn dịch đến vị trí khối u, nhận diện và tiêu diệt tế bào ung thư nhờ cơ chế gây độc tế bào qua trung gian tế bào phụ thuộc kháng thể (Antibody-Dependent Cell mediated Cytotoxicity – ADCC).
– Các thuốc nổi bật trong nhóm này: Cetuximab (Kháng thể IgG1, “dạng khảm” với phần biến đổi gắn kháng khuyên có nguồn gốc chuột), Nimotuzumab (Humanize antibody, chỉ có một tỷ lệ nhỏ protein nguồn gốc chuột), Panitumumab (IgG2, thuần tuý 100% protein người).
– Các yếu tố phản ánh tình trạng hoạt động của EGFR có thể có ý nghĩa dự báo khả năng đáp ứng với liệu pháp kháng thể đơn dòng kháng EGFR:
→ Mức độ bộc lộ EGFR trên bề mặt tế bào ung thư: xác định bởi xét nghiệm hoá mô miễn dịch
→ Số lượng bản sao gen EGFR trong nhân tế bào (Gene copy number): xác định bởi xét nghiệm FISH hoặc CISH
→ Giá trị dự báo của mỗi yếu tố trên thay đổi với các bệnh ung thư khác nhau
– Hiện tượng đề kháng với liệu pháp kháng thể đơn dòng kháng EGFR được giải thích dựa trên 3 cơ chế chính [3]:
→ Giảm tương tác giữa kháng thể với kháng nguyên: Do đột biến gen EGFR mã hoá phần ngoại bào gắn với kháng thể, tăng bộc lộ các yếu tố tăng trường (EGF, TGF α) cạnh tranh với kháng thể…
→ Tín hiệu nội bào vẫn được kích hoạt và dẫn truyền qua các con đường khác. Ví dụ: Con đường HER2, MET…
→ Đột biến gen mã hoá các protein “mắt xích” khác trên con đường tín hiệu qua EGFR dẫn đến hiện tượng tự hoạt hoá những mắt xích này không phụ thuộc nữa vào tín hiệu từ EGFR. Ví dụ: Đột biến KRAS tại codon 12 của exon 2, đột biến BRAF tại exon 15….
3.2. Các thuốc ức chế EGFR tyrosine kinase (EGFR TKIs)
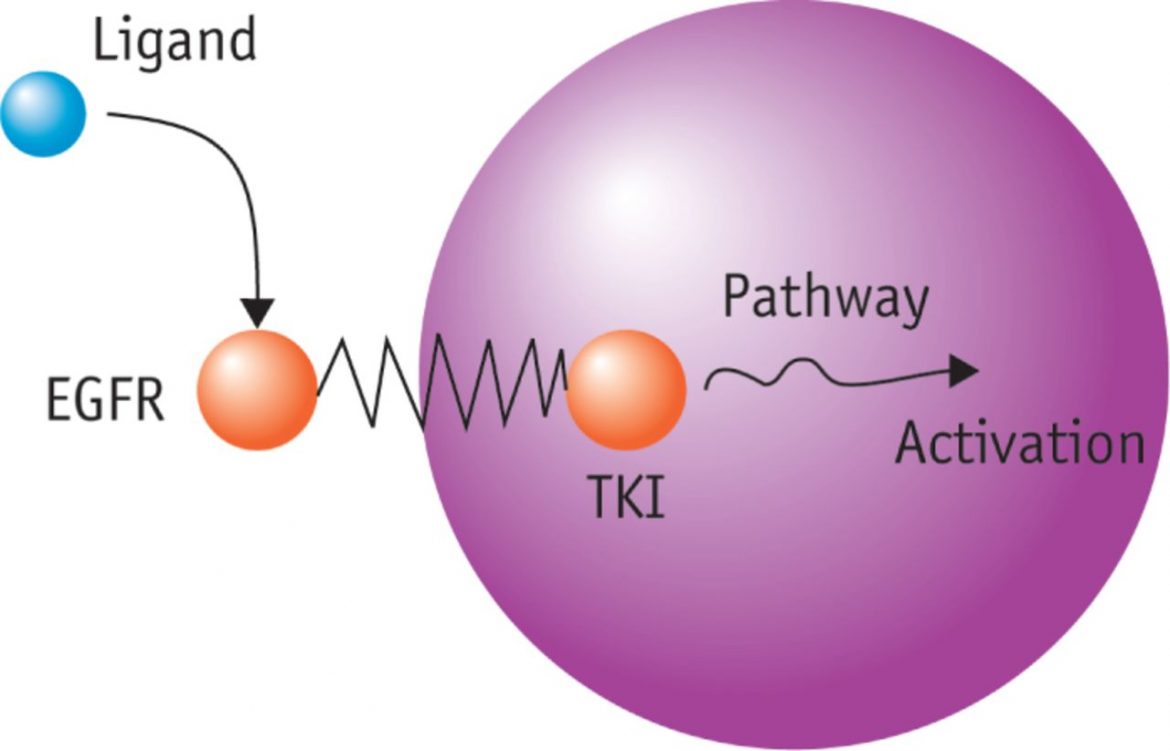
– Các phân tử nhỏ EGFR TKIs gắn vào vị trí đặc hiệu tại vùng nội bào (hoạt tính tyrosine kinase) của EGFR, cạnh tranh với ATP nhờ có ái lực mạnh hơn. Không có ATP, tyrosine kinase không thể thực hiện phản ứng phosphoryl hoá để khởi phát các dòng tín hiệu nội bào.
– Phần lớn đột biến gen EGFR xảy ra tại đoạn mã hoá cho vùng hoạt tính tyrosine kinase:
+ Trong đó, xấp xỉ 85% đột biến (Trong ung thư phổi) được xác định tại exon 19 (Mất hoặc thêm một số cặp base) và exon 21 (Thay thế Leucine bằng Arginine tại vị trí 858 – L858R) [4] tạo thuận lợi hơn cho các TKIs gắn vào và ức chế hoạt tính tyrosine kinase. Các đột biến này có ý nghĩa quan trọng dự báo nhạy cảm với điều trị TKIs trong ung thư phổi [5].
+ Đột biến tại exon 20 (Thay thế Threonine bởi Methionine tại vị trí 790) làm giảm ái tính với các phân tử TKIs bên cạnh phục hồi ái lực với ATP. Đột biến T790M là cơ chế kháng điều trị Gefitinib, Erlotinib (Các TKIs thế hệ 1) trong khoảng 50% các trường hợp.
– Các thế hệ EGFR TKIs [6]:
+ Thế hệ 1 (Erlotinib, Gefitinib): Gắn đặc hiệu vào vùng hoạt tính tyrosine kinase ở phần nội bào EGFR theo cơ chế thuận nghịch (Ức chế có thể hồi phục)
+ Thể hệ 2 (Afatinib, Dacomitinib): Được phát triển với mục đích điều trị những trường hợp kháng với TKIs thế hệ 1 do đột biến T790M, tuy nhiên tác động trên EGFR đột biến T790M không chọn lọc mà còn có tác dụng ức chế với các phân tử EGFR không đột biến.
+ Thế hệ 3 (Osimertinib): Tác động ức chế chọn lọc đối với các phân tử EGFR đột biến T790M và các đột biến tại exon 19 và 21.
– Các cơ chế kháng thuốc EGFR TKIs được ghi nhận trong ung thư phổi không tế bào nhỏ:
→ Đột biến T790M ở exon 20 (50%)
→ Đột biến PIK3CA (5%)
→ Hoạt hoá con đường tín hiệu qua HER2 (10%) hay MET (10%)
→ Chuyển dạng Ung thư phổi tế bào nhỏ (5%)
→ Các cơ chế chưa được hiểu biết rõ (20%).
Tài liệu tham khảo:
1. Bianco R, Gelardi T, Damiano V, Ciardiello F, Tortora G. Rational Bases for the Development of EGFR Inhibitors for Cancer Treatment. The International Journal of Biochemistry & Cell Biology. 2007;39:1416–1431.
2. Yarden Y (2001) The EGFR family and its ligands in human cancer. signalling mechanisms and therapeutic opportunities. Eur J Cancer 37: S3-8.
3. Andrea Bertotti and Francesco Sassi. Molecular Pathways: Sensitivity and Resistance to Anti-EGFR Antibodies. Clin Cancer Res August 1 2015 (21) (15) 3377-3383.
4. Rosell R, Moran T, Queralt C, et al. Screening for epidermal growth factor receptor mutations in lung cancer. N Engl J Med. 2009;361(10):958–967. doi: 10.1056/NEJMoa0904554.
5. Wang H, Huang J, Yu X, et al. Different efficacy of EGFR tyrosine kinase inhibitors and prognosis in patients with subtypes of EGFR-mutated advanced non-small cell lung cancer: a meta-analysis. Journal of Cancer Research and Clinical Oncology. 2014;140(11):1901-1909. doi:10.1007/s00432-014-1709-0.
6. Sullivan I. và Planchard D. (2017). Next-Generation EGFR Tyrosine Kinase Inhibitors for Treating EGFR-Mutant Lung Cancer beyond First Line. Front Med, 3.
BSNT. Hoàng Huy Hùng
BSNT. Trần Trung Bách